Химические свойства фенолов определяются наличием в молекуле гидроксильной группы и бензольного кольца.
I. Реакции с участием гидроксильной группы
Фенолы являются более сильными кислотами, чем спирты и вода, т.к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается.
Кислотные свойства
Фенолы в водных растворах диссоциируются по кислотному типу: на фенолят-ионы и ионы водорода:
Фенол диссоциирует обратимо, это слабая кислота. Однако его силы кислотных свойств достаточно, чтобы изменять окраску индикатора, имеющего в нейтральной среде фиолетовый цвет. В растворе фенола лакмус краснеет.

- 1) Взаимодействие с активными металлами с образованием фенолятов (сходство со спиртами)

- Видеоопыт «Взаимодействие фенола с металлическим натрием»
- 2) Взаимодействие со щелочами с образованием фенолятов (отличие от спиртов)

- Видеоопыт «Взаимодействие фенола с раствором щелочи»
Образующиеся в результате реакций феноляты легко разлагаются при действии кислот. Даже такая слабая кислота, как угольная, вытесняет фенол из фенолятов.
Следовательно, !Феноляты – соли слабой карболовой кислоты, разлагаются угольной кислотой:![]()
По кислотным свойствам фенол превосходит этанол в 106 раз. При этом во столько же раз уступает уксусной кислоте. В отличие от карбоновых кислот, фенол не может вытеснить угольную кислоту из её солей
- C6H5-OH + NaHCO3 = реакция не идёт – прекрасно растворяясь в водных растворах щелочей, он фактически не растворяется в водном растворе гидрокарбоната натрия.
- Кислотные свойства фенола усиливаются под влиянием связанных с бензольным кольцом электроноакцепторных групп (NO2- , Br- )

- 2,4,6-тринитрофенол или пикриновая кислота сильнее угольной.
- 3) Образование сложных и простых эфиров
Как и спирты, фенолы могут образовывать простые и сложные эфиры. Фенолы не образуют сложные эфиры в реакциях с кислотами. Сложные эфиры образуются при взаимодействии фенола с ангидридами или хлорангидридами карбоновых кислот:
Простые эфиры образуются при взаимодействии фенолятов с алкилгалогенидами:

II. Реакции, с участием бензольного кольца
- Взаимное влияние атомов в молекуле фенола проявляется не только в особенностях поведения гидроксигруппы, но и в большей реакционной способности бензольного ядра. Гидроксильная группа повышает электронную плотность в бензольном кольце, особенно, в орто- и пара- положениях (+М-эффект ОН-группы):

- Поэтому фенол значительно активнее бензола вступает в реакции электрофильного замещения в ароматическом кольце.
- Реакции замещения
- 1) Нитрование
- Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара- нитрофенолов:

- При использовании концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота):
У нее кислотные свойства выражены сильнее, чем у фенола, т.к. нитрогруппы оттягивают электронную плотность от бензольного кольца и делают связь О-Н еще более полярной.
- Пикриновая кислоты является взрывчатым веществом, в чистом виде представляет собой желтые кристаллы.
- 2) Галогенирование
- Фенол легко при комнатной температуре взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол!):
- Образуется белый осадок трибромфенола.
- Видеоопыт «Взаимодействие фенола с бромной водой»
- 3) Сульфирование
- Соотношение о- и п-изомеров определяется температурой реакции: при комнатной температуре в основном образуется о-фенолсульфокислота, при t=1000С – пара-изомер:Реакции присоединения
- 1) Гидрирование фенола
Эта реакция идет с разрушением ароматического кольца. Продукт реакции циклический одноатомный спирт — циклогексиловый спирт (циклогексанол).
- 2) Конденсация с альдегидами
- При нагревании фенола с формальдегидом в присутствии кислотных или основных катализаторов происходит реакция поликонденсации и образуется фенолформальдегидная смола.
- Данная реакция имеет большое практическое значение и используется при получении фенолформальдегидных смол.
III. Реакция окисления
Фенолы легко окисляются даже под действием кислорода воздуха. При стоянии на воздухе фенол постепенно окрашивается в розовато-красный цвет.
- 1) Горение (полное окисление)
- Фенолы, как и большинство органических веществ, сгорают до углекислого газа и воды.
- 2) Окисление хромовой смесью
При энергичном окислении фенола хромовой смесью основным продуктом окисления является хинон. Двухатомные фенолы окисляются еще легче. При окислении гидрохинона также образуется хинон:
IV. Качественная реакция! — обнаружение фенола
Для обнаружения фенолов используется качественная реакция с хлоридом железа (III). Одноатомные фенолы дают устойчивое сине-фиолетовое окрашивание, что связано с образованием комплексных соединений железа.
- Видеоопыт «Качественная реакция на фенол»
- Образование фиолетового окрашивания при добавлении раствора FeCl3 служит качественной реакцией на фенол:
- Для фенолов реакции по связям С-О не характерны, поскольку атом кислорода прочно связан с атомом углерода бензольного кольца за счет участия своей неподеленной электронной пары в системе сопряжения.
- Фенолы
Источник: https://himija-online.ru/organicheskaya-ximiya/fenol/ximicheskie-svojstva-fenolov.html
Фенолы
Фенолы — кислородсодержащие ароматические соединения, в молекулах которых содержится одна или несколько гидроксильных групп (OH), присоединенных к бензольному кольцу.
Номенклатура фенолов
Нумерацию атомов углерода в молекуле фенола начинают в такой последовательности, чтобы заместители получили наименьшие номера (идут кратчайшим путем). В основе названия принято сохранять тривиальное название «фенол».

Напомню, что гидроксильная группа является ориентантом I порядка (орто-, пара-ориентант). Поэтому реакции галогенирования, нитрования протекают в орто- и пара-положениях.
Получение фенолов
- Гидролиз галогенбензолов
- Кумольный способ
При гидролизе галогенбензолов происходит обмен: гидроксогруппа встает на место атома галогена. 
Этим способом получают 95% всего производимого фенола. В ходе этой реакции кумол (изопропилбензол) подвергают окислению, в результате получается фенол и ацетон. 
Химические свойства фенолов
- Кислотные свойства
- Галогенирование
- Реакции с кислотами
- Гидрирование
- Поликонденсация фенолов с формальдегидом
Щелочные металлы (Li, Na, K) способны вытеснять водород из спиртов с образованием солей — фенолятов. В отличие от алифатических одноатомных спиртов, фенолы способны вступать в реакцию с щелочами (KOH, LiOH, NaOH) 
Реакция фенола с бромной водой является качественной: в ходе нее выпадает белая взвесь — осадок трибромфенола. 
Реакция между фенолом и азотной кислотой происходит по типу замещения. В бензольном кольце появляется новый радикал — нитрогруппа. Важно учитывать, что OH группа фенола является ориентантом I порядка: замещение идет в орто-, пара-положении. 
При гидрировании разрываются двойные связи бензольного кольца, образуется циклогексанол. 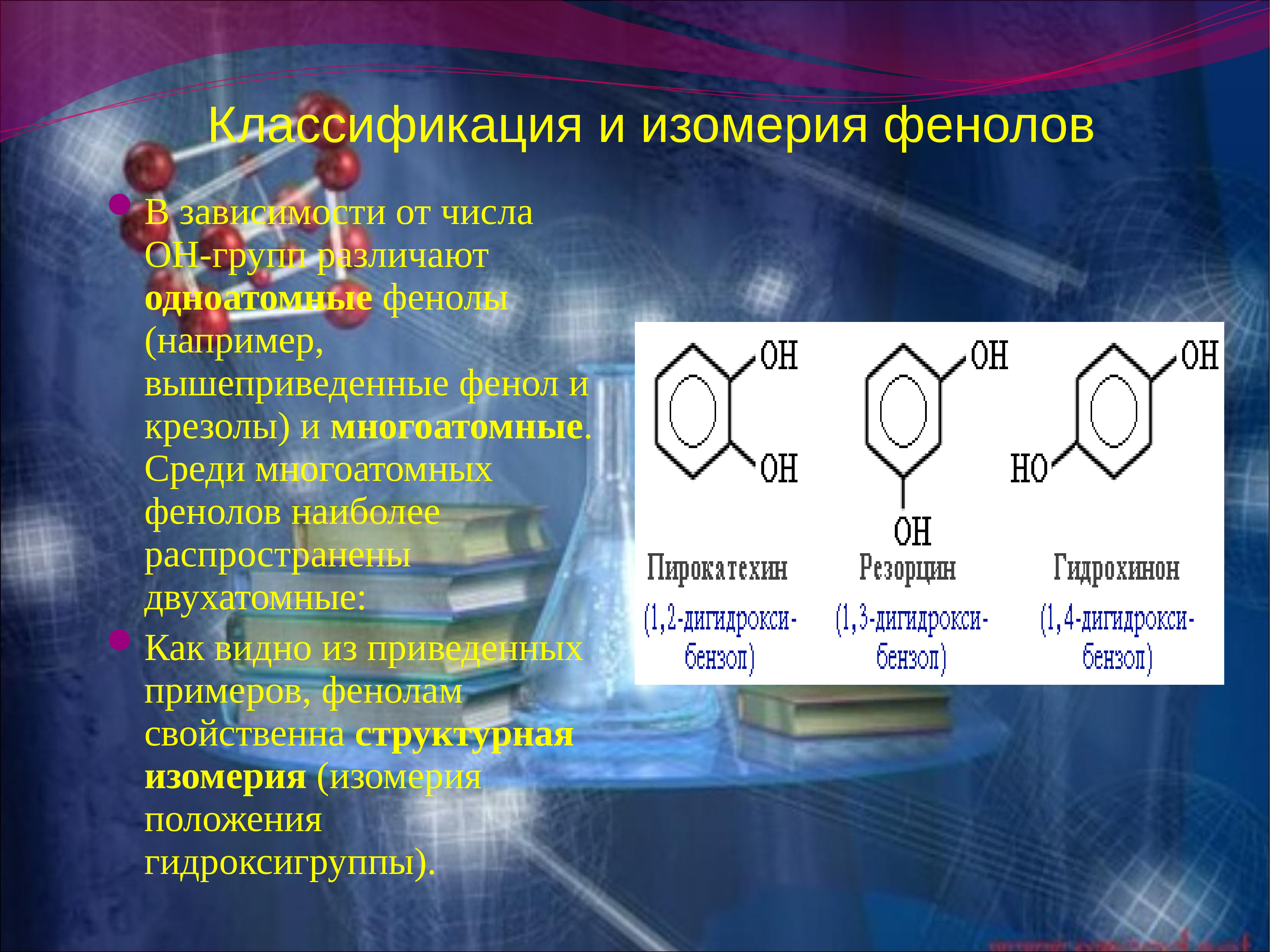
В промышленности получила широкое распространение реакция поликонденсации фенола с формальдегидом, приводящая к образованию смолообразных полимеров (фенолформальдегидные смолы) и воды. 
Источник: https://studarium.ru/article/188
Фенол
Гидроксибензол
Химические свойства
Что такое Фенол? Гидроксибензол, что это такое? Согласно Википедии – это один из простейших представителей своего класса ароматических соединений.
Фенолы – это органические ароматические соединения, в молекулах которых к гидроксильной группе присоединены атомы углерода из ароматического кольца. Общая формула Фенолов: С6Н6n(ОН)n.
Согласно стандартной номенклатуре, органические вещества этого ряда различают по числу ароматических ядер и ОН-групп. Различают одноатомные аренолы и гомологи, двухатомные арендиолы, терхатомные арентриолы и многоатомные формулы.
Также Фенолам свойственно иметь ряд пространственных изомеров. Например, 1,2-дигидроксибензол (пирокатехин), 1,4-дигидроксибензол (гидрохинон) являются изомерами.
Спирты и Фенолы отличаются друг от друга наличием ароматического кольца. Этанол является гомологом метанола. В отличие от Фенола, метанол взаимодействует с альдегидами и вступает в реакции этерификации. Утверждение, что гомологами являются метанол и Фенол неверно.
Его подробно рассмотреть структурную формулу Фенола, то можно отметить, что молекула представляет собой диполь. При этом бензольное кольцо – отрицательный конец, а группа ОН – положительный. Наличие гидроксильной группы обуславливает повышение электронной плотности в кольце.
Неподеленная пара электронов кислорода вступает в сопряжение с пи-системой кольца, а для атома кислорода характерна sp2 гибридизация. Атомы и атомные группы в молекуле обладают сильным взаимным влиянием друг на друга, и это отражается на физических и химических свойствах веществ.
Физические свойства. Химическое соединение имеет вид бесцветных игольчатых кристаллов, которые розовеют на воздухе, так как подвержены окислению. У вещества специфический химический запах, оно умеренно растворимо в воде, спиртах, щелочи, ацетоне и бензоле. Молярная масса = 94,1 грамм на моль. Плотность = 1,07 г на литр. Кристаллы плавятся при 40-41 градусах Цельсия.
С чем взаимодействует Фенол? Химические свойства Фенола. В связи с тем, что молекула соединения содержится, как ароматическое кольцо, так и гидроксильную группу, то оно проявляет некоторые свойства спиртов и ароматических углеводородов.
С чем реагирует группа ОН? Вещество не проявляет сильных кислотных свойств. Но является более активным окислителем, чем спирты, в отличие от этанола взаимодействует с щелочами образуя соли-феноляты. Реакция с гидроксидом натрия: С6Н5ОН + NaOH → C6H5ONa + H2O. Вещество вступает в реакцию с натрием (металлическим): 2C6H5OH + 2Na → 2C6H5ONa + H2.
Фенол не реагирует с карбоновыми кислотами. Эфиры получают при взаимодействии солей фенолятов с галогенангидридами или ангидридами кислот. Для химического соединения не характерны реакции образования простых эфиров.
Эфиры образуют феноляты при действии на них галогеналканов или галогенпроизводных аренов.
Гидроксибензол реагирует с цинковой пылью, при этом происходит замещение гидроксильной группы на Н, уравнение реакции выглядит следующим образом: C6H5OH + Zn → C6H6 + ZnO.
Химическое взаимодействие по ароматическому кольцу. Для вещества характерны реакции электрофильного замещения, алкилирования, галогенирования, ацилирования, нитрования и сульфирования.
Особое значение имеет реакций синтеза салициловой кислоты: C6H5OH + CO2 → C6H4OH(COONa), протекает в присутствии катализатора гидроксида натрия.
Затем при воздействии соляной кислоты образуется салициловая к-та.
Реакция взаимодействия с бромной водой является качественной реакцией на Фенол. C6H5OH + 3Br2 → C6H2Br2OH + 3HBr. При бромировании образуется твердое белое вещество — 2,4,6-трибромфенол. Еще одна качественная реакция – с хлоридом железа 3. Уравнение реакции выглядит следующим образом: 6C6H5OH + FeCl3 → (Fe(C6H5OH)6)Cl3.
Реакция нитрования Фенола: C6H5OH + 3HNO3 → C6H2(NO2)3OH + 3 H2O. Для вещества также характерна реакция присоединения (гидрирования) в присутствии металлических катализаторов, платины, оксида алюминия, хрома и так далее. В результате образуются циклогексанол и циклогексанон.
Химическое соединение подвергается окислению. Устойчивость вещества значительно ниже, чем у бензола. В зависимости от условий реакции и природы окислителя образуются разные продукты реакции. Под действием перекиси водорода в присутствии железа образуется двухатомный Фенол; при действии диоксида марганца, хромовой смеси в подкисленной среде – пара-хинон.
Фенол реагирует с кислородом, реакция горения: С6Н5ОН +7О2 → 6СО2 + 3Н2О. Также особое значение для промышленности имеет реакция поликонденсации с формальдегидом (например, метаналем).
Вещество вступает в реакцию поликонденсации до тех пор, пока не израсходуется полностью один из реагентов и не образуются огромные макромолекулы.
В результате образуются твердые полимеры, фенолформальдегидные или формальдегидные смолы. Фенол не взаимодействует с метаном.
Получение. На данный момент существуют и активно применяются несколько методов синтеза гидроксибензола. Кумольный способ получения Фенола является наиболее распространенным из них. Таким способом синтезируют порядка 95% всего объема производства вещества.
При этом некаталитическому окислению воздухом подвергается кумол и образуется гидропероксид кумола. Полученное соединение разлагается под действием серной кислоты на ацетон и Фенол.
Дополнительным побочным продуктом реакции является альфа-метилстирол.
Также соединение можно получить при окислении толуола, промежуточным продуктом реакции будет являться бензойная кислота. Таким образом, синтезируют около 5% вещества. Все остальное сырье для различных нужд выделяют из каменноугольной смолы.
Как получить из бензола? Фенол можно получить с помощью реакции прямого окисления бензола NO2 (закись азота) с дальнейшим кислотным разложением гидропероксида втор-бутилбензола.
Как из хлорбензола получить Фенол? Существует два варианта получения из хлорбензола данного химического соединения. Первый – реакция взаимодействия со щелочью, например, с гидроксидом натрия. В результате образуется Фенол и поваренная соль.
Второй – реакция с водяным паром. Уравнение реакции выглядит следующим образом: C6H5-Cl + H2O → C6H5-OH + HCl.
Получение бензола из Фенола. Для этого сначала требуется обработать бензол хлором (в присутствии катализатора), а затем прибавить к полученному соединению щелочь (например, NaOH). В итоге образуется Фенол и хлорид натрия.
Превращение метан — ацетилен — бензол — хлорбензол можно осуществить следующим образом.
Сначала проводится реакция разложения метана при высокой температуре 1500 градусов Цельсия до ацетилена (С2Н2) и водорода.
Затем ацетилен при особых условиях и высокой температуре переводят в бензол. К бензолу прибавляют хлор в присутствии катализатора FeCl3, получают хлорбензол и соляную кислоту: C6H6 + Cl2 → C6H5Cl + HCl.
Одним из структурных производных Фенола является аминокислота тирозин, которая имеет важное биологическое значение.
Данную аминокислоту можно рассмотреть в виде пара-замещенного Фенола или альфа-замещенного пара-крезола. Крезолы – достаточно распространены в природе на ряду с полифенолами.
Также свободную форму вещества можно обнаружить в некоторых микроорганизмах в равновесном состоянии с тирозином.
Гидроксибензол применяется:
- при производстве бисфенола А, эпоксидной смолы и поликарбоната;
- для синтеза фенолформальдегидных смол, капрона, нейлона;
- в нефтеперерабатывающей промышленности, при селективной очистке масел от ароматических соединений серы и смол;
- при производстве антиоксидантов, поверхностно-активных веществ, крезолов, лек. препаратов, аспирина, пестицидов и антисептических препаратов;
- в медицине в качестве антисептического и обезболивающего средства для местного использования;
- в качестве консерванта при изготовлении вакцин и копченых продуктов питания, в косметологии при проведении глубокого пилинга;
- для дезинфекции животных в скотоводстве.
Класс опасности. Фенол – крайне токсичное, ядовитое, едкое вещество.
При вдыхании летучего соединения нарушается работа центральной нервной системы, пары раздражают слизистую глаз, кожу, дыхательные пути и вызывают сильные химические ожоги.
При попадании на кожу вещество быстро всасывается в кровоток и достигает тканей мозга, вызывая паралич дыхательного центра. Смертельная доза при приеме внутрь для взрослого составляет от 1 до 10 грамм.
Фармакологическое действие
Антисептическое, прижигающее.
Фармакодинамика и фармакокинетика
Средство проявляет бактерицидную активность по отношению в аэробным бактериям, их вегетативным формам и грибам. Практически не оказывает влияния на споры грибов.
Вещество вступает во взаимодействие с белковыми молекулами микробов и приводит к их денатурации.
Таким образом, нарушается коллоидное состояние клетки, значительно повышается ее проницаемость, нарушаются окислительно-восстановительные реакции.
В водном растворе является отличным дезинфицирующим средством. При использовании 1,25% раствора практически микроорганизмы погибают в течение 5-10 минут. Фенол, в определенной концентрации оказывает прижигающее и раздражающее действие на слизистую оболочку. Бактерицидный эффект от применения средства усиливается с ростом температуры и кислотности.
При попадании на поверхность кожи, даже если она не повреждена, лекарство быстро всасывается, проникает в системный кровоток.
При системной абсорбции вещества наблюдается его токсическое действие, преимущественно на центральную нервную систему и дыхательный центр в головном мозге.
Порядка 20% от принятой дозы подвергается окислению, вещество и продукты его метаболизма выводятся с помощью почек.
Показания к применению
Применение Фенола:
- для дезинфекции инструментов и белья и дезинсекции;
- в качестве консерванта в некоторых лек. средствах, вакцинах, свечах и сыворотках;
- при поверхностных пиодермиях, фолликулите, фликтене, остиофолликулите, сикозе, стрептококковом импетиго;
- для лечения воспалительных заболеваний среднего уха, ротовой полости и глотки, ангины, фарингита, стоматита, пародонтита, генитальных остроконечных кондилом.
Противопоказания
Вещество не используют:
- при распространенных поражениях слизистой оболочки или кожи;
- для лечения детей;
- во время кормления грудью и беременности;
- при аллергии на Фенол.
Побочные действия
Иногда лекарственное средство может спровоцировать развитие аллергических реакций, зуд, раздражение в месте нанесения и чувство жжения.
Инструкция по применению (Способ и дозировка)
Консервацию лекарственных препаратов, сывороток и вакцин проводят с помощью 0,5% растворов Фенола.
Для наружного применения лекарство используют в виде мази. Препарат наносят тонким слоем на пораженные участки кожи несколько раз в сутки.
При лечении отита вещество используют в форме 5% раствора в глицерине. Препарат подогревают и закапывают по 10 капель в пораженное ухо на 10 минут. Затем необходимо удалить остатки лекарства с помощью ваты. Процедуру повторяют 2 раза в день в течение 4 суток.
Препараты Фенола для лечения ЛОР-заболеваний используют в соответствии с рекомендациями в инструкции. Продолжительность терапии – не более 5 дней.
Для ликвидации остроконечных кондилом их обрабатывают 60% раствором Фенола или 40% раствором трикрезола. Процедуру проводят один раз в 7 дней.
При дезинфекции белья применяют 1-2% растворы на основе мыла. С помощью мыльно-фенольного раствора обрабатывают помещение. При дезинсекции используются фенольно-скипидарные и керосиновые смеси.
Передозировка
При попадании вещества на кожу возникают жжение, покраснение кожи, анестезия пораженного участка. Поверхность обрабатывают растительным маслом или полиэтиленгликолем. Проводят симптоматическую терапию.
Симптомы отравления Фенолом при попадании внутрь. Наблюдаются сильные боли в животе, глотке, в ротовой полости, пострадавшего рвет бурой массой, бледность кожи, общая слабость и головокружение, миоз, коллапс, падение температуры тела, судороги, кома, острая печеночная недостаточность.
В качестве терапии желудок промывают растительным маслом с добавлением белков, затем дают пострадавшему 10% раствор глицерола и активированный уголь. Показан прием оксида магния и глюконата кальция, форсированный диурез, тиосульфат натрия капельно внутривенно, витамины группы В.
Проводят лечение токсического шока.
Взаимодействие
Лекарственное взаимодействие не происходит.
Особые указания
Фенол обладает способностью адсорбироваться пищевыми продуктами.
Средством нельзя обрабатывать обширные участки кожи.
Перед использованием вещества для дезинфекции предметов быта, их необходимо механически очистить, так как средство абсорбируется органическими соединениями. После обработки вещи могут еще длительное время сохранять специфический запах.
Химическое соединение нельзя использовать для обработки помещений для хранения и готовки пищевой продукции. Оно не влияет на окраску и структуру ткани. Повреждает поверхности, покрытые лаком.
Детям
Средство нельзя использовать в педиатрической практике.
При беременности и лактации
Фенол не назначают во время кормления грудью и при беременности.
Препараты, в которых содержится (Аналоги)
Совпадения по коду АТХ 4-го уровня: Этоксисклерол
Этоксисклерол
Фенол входит в состав следующих препаратов: Ферезол, Фукорцин, Фенола раствор в глицерине, Орасепт, Фармасептик. В качестве консерванта содержится в препаратах: Экстракт Белладонны, Набор для кожной диагностики медикаментозной аллергии, Постеризан и так далее.
Отзывы
Фенол – хорошее антисептическое средство, которое подходит, как для обработки инструментов и помещений, так и при лечении воспалительных ЛОР-заболеваний.
При соблюдении рекомендаций врача и инструкции по применению, необходимых мер безопасности при работе с такого рода веществами, средство хорошо переносится и не вызывает негативного влияния на организм.
Отзывы о применении препаратов Фенола, как правило, положительные. Особенно хорошие отзывы при лечении заболеваний горла.
Цена, где купить
Стоимость вещества для технического использования зависит от количества и производителя. Купить спрей для готовой полости Орасепт можно примерно за 400 рублей – флакон.
Источник: https://medside.ru/fenol
Фенолы — 1) Общая формула; 2) Представитель; 3) Физ.свойства 4) Изомерия 5) Качественная — Школьные Знания.com
Modric
18.03.2014

Фенолы1) Общая формула: вещества, содержащие радикал фенил C6H5-2) Представитель — фенол C6H5OH3) Физ.свойства — бесцветные кристаллические вещества с невысокой температурой плавления и характерным запахом, малорастворимы в воде, хорошо растворимы в органических растворителях, токсичны, при хранении на воздухе постепенно темнеют в результате окисления.4) Изомерия — Изомерия положения заместителей и ОН-группы5) Качественная реакция — с бромной водой, хлорид железа (многоатомные фенолы)
6) Применение —
фенол-альдегидные смолы, полиамиды, полиарилаты, полиариленсульфоны, эпоксидные смолы, антиоксиданты, бактерициды и пестицидыАльдегиды1) Общая формула CnH2n+1COH2) Представитель — HCOH формальдегид
3) Физ.свойства — н
изшие альдегиды — жидкости, первые члены ряда смешиваются с водой, а следующие растворимы в ней; высшие альдегиды — нерастворимые твердые вещества. Низшие альдегиды обладают резким запахом.4) Изомерия — Изомерия положения альдегидной группы и заместителей5) Качественная реакция — реакция «серебреного зеркала»
6) Применение —
производстве смол (бакелита, галалита (в сочетании с мочевиной, меламином и фенолом)), для дубления кож, протравливания зерна.
Также из него синтезируют лекарственные средства (уротропин) используют как консервант биологических препаратов1) Общая формула CnH2n+2CO2) Представитель — ацетон CH3C(O)CH33) Физ.
свойства — летучие жидкости или легкоплавкие твёрдые
вещества, низшие представители хорошо растворимы в воде и смешиваются с
органическими растворителями, некоторые (ацетон) смешиваются с водой в
любых соотношениях.
4) Изомерия — Изомерия положения кетонной группы и заместителей5) Качественная реакция — с сульфитом натрия6) Применение — В промышленности используют как растворители, фармацевтические
препараты и для изготовления различных полимеров.
Карбоновые кислоты1) Общая формула — CnH2n+1COOH
2) Представитель — уксусная кислота3) Физ.свойства — Низшие кислоты с числом атомов углерода до 3 — легкоподвижные бесцветные
жидкости с характерным резким запахом, смешиваются с водой в любых
соотношениях. Большинство кислот с 4-9 атомами углерода — маслянистые
жидкости с неприятным запахом. Кислоты с большим количеством атомов
углерода — твёрдые вещества, нерастворимые в воде. Температура кипения
возрастает по мере увеличения молекулярной массы, 4) Изомерия — Изомерия положения карбоксильной группы и заместителей5) Качественная реакция — с карбонатом натрия
6) Применение — получение промежуточных продуктов органического синтеза. Соли карбоновых кислот и щелочных металлов применяют как мыла, эмульгаторы, смазочные масла; соли тяжелых металлов — сиккативы, инсектициды и фунгициды, катализаторы. Эфиры кислот — пищевые добавки, растворители
Источник: https://znanija.com/task/5509424
Что такое фенол? Свойства и применение
- Свойства
- Получение
- Применение
- Опасность фенола
Фенол – это самое простое соединение из класса фенолов, производное аренов, в молекуле которого непосредственно реализуется связь гидроксильных групп и бензольного кольца. По сути, это слабая кислота, что и есть главным отличием между фенолами и спиртами, являющимися неэлектролитами. Выпускается мировой промышленностью в миллионах тонн ежегодно. По объемах среди всех хим. веществ занимает 33 место, среди органических – 17. Характеризуется токсичностью и достаточно большой едкостью, способно обжигать кожу и выступает мощным ирритантом. Может выполнять роль антисептика в виде 5 %-го водного раствора, и не просто может, а выполняет и активно с этой целью используется в медицине.
Названия-синонимы: гидроксибензол, карболовая кислота (устар.).
Свойства
Выглядит это вещество как бесцветная прозрачная твердая масса, сформированная игольчатыми кристаллами. Запах – специфический, у большинства ассоциируется с запахом гуаши, так как в ее составе присутствует фенол.
Растворяется в воде в стандартных условиях ограниченно: в соотношении 6,5 г на 100 мл. При температуре 66 °C и более смешивается с H2O в различных пропорциях. Именно к водным растворам чаще используют наименование «кислота карболовая». Кроме того, растворению поддается в щелочах, спиртах, бензене и диметилкетоне.
Пребывая на воздухе, данное соединение окисляется и приобретает розоватый окрас. Появление цветных компонентов объясняется промежуточным формированием хинонов.
Молярная масса – 94,11 г/моль, плотность – 1,07 г/см³. Термосвойства: t плавления – 40,9 °C, t кипения – 181,84 °C, t вспышки – 79/85 °C (в закрытом и открытом тигле, соответственно). Формула: C6H5OH.
Химическим свойствам гидроксибензола характерна двуплановость. С одной стороны, у них присутствует ароматическое кольцо, с другой – гидроксильная группа. Поэтому фенол обладает свойствами и спиртов, и аренов:
– по гидроксильной группе. Небольшие кислотные качества (сильнее, по сравнению со спиртами). Формирование солей, именуемых фенолятами, в частности натрия фенолята, при воздействии щелочей.
В виду очень слабых свойств кислоты, из фенолятов ее может вытеснить даже угольная к-та.
А более интенсивное разложение фенолятов характерно при влиянии сильных кислот, к примеру, H2SO4 (сульфатной кислоты).
Кроме того, C6H5OH реагирует с металлическим натрием. Этерификации карбоновыми кислотами не поддается. Для получения эфиров может задействоваться реакция между фенолятами и ангидридами/галогенангидридами кислот.
Этеры появляются тогда, когда на фенол воздействуют алкилгалогениды, либо же на феноляты – галогенпроизводные ароматических углеводородов. Итог первого варианта воздействия – сочетания жирных ароматических простых эфиров, второго – чисто-ароматические эфиры. Для обеспечения реакции необходимо присутствие катализатора, которым выступает медь в форме порошка.
Перегонка совокупности «фенол + цинковая пыль» приводит к тому, что гидроксильную группу замещает водород.
– по ароматическому кольцу. Данному соединению свойственно вступление в реакции электрофильного замещения. Оно легко поддается таким воздействиям, как алкилирование, ацилирование, галогенирование, нитрование и сульфирование.
В этом ракурсе стоит упомянуть также реагирование с водным раствором брома, хлорным железом (качественные реакции на гидроксибензол) и концентрированной HNO3 (нитратной кислотой).
Гидрируя фенол в ходе присоединительной реакции и при условии наличия катализирующих металлических компонентов, создают гексалин и циклогексанон.
Что касается окисления карболовой к-ты, то так как в фенольной молекуле присутствует гидроксильная группа, стойкость к окислению значительно слабее, по сравнению с бензолом. Продукт на выходе зависит от природы окисляющего материала и условий, при которых проводилась реакция.
Получение
На сегодняшний день пром. изготовление фенола происходит 3-мя способами:
- Кумольный метод. Основной способ получения, на который приходится около 95 % мирового фенольного производства. Его разработка принадлежит советским ученым. А суть состоит вот в чем:
- – кумол (изопропилбензол) помещают в каскад барботажных колонн и выполняют некаталитическое окисление с помощью воздуха, при этом формируется гидропероксид кумола (2-гидроксипропан-2-илбензол);
- – полученный ГПК при воздействии H2SO4 катализируется и разлагается на фенол и диметилкетон.
- Кстати, в ходе данного процесса в качестве побочного продукта выделяется еще одно ценное вещество, а именно α-метилстирол (изопренилбензол).
- Окисление метилбензола. На этот способ приходится всего примерно 3 % производства. Особенностью является промежуточное образование бензойной кислоты.
- Третий способ основывается на использовании в качестве исходного сырья такого продукта, как каменноугольная смола. Остальной фенол получают именно так.
Кстати, сейчас подвергаются испытаниям установки, с помощью которых предполагается синтез фенола в ходе прямого окисления бензола оксид диазотом и кислотного разложения гидропероксида втор-бутилбензола. Кроме того, это вещество может быть получено при восстановлении хинона.
Применение
Рассматриваемый материал имеет очень широкий спектр использования. Без него не обходятся в разноплановых процессах, о которых не помешает знать.
Фенол – это соединение, которое было выведено искусственным путем. Ему характерна низкая t плавления, растворение в средах и органической, и неорганической природы. Оно – ценная основа для создания различных материалов, важных в пром. масштабах.
Ввиду антисептических свойств, применяется для дезинфекционных мероприятий, направленных на белье, помещения и т.д. Но если раньше для этих целей вещество использовалось активно, то сегодня его задействование ограничено, из-за высокотоксичности.
- Сферы применения фенола:
- – изготовление красителей (указанную субстанцию берут для этого направления, поскольку она под влиянием воздуха способна менять свой окрас);
- – производство пластических масс, а именно фенолформальдегидных смол и ДФП, используемого, в свою очередь, при создании поликарбонатов и эпоксидных смол;
- – переработка нефти (селективное маслоочищение, очистка ортокрезола и создание присадок для масел). Фенол характеризуется значительной эффективностью, если нужно удалить смолистые вещества, серосодержащие соединения и прочее из масел;
- – молекулярная биология и генная инженерия (участие в очищении ДНК и в выделении ДНК из клетки совместно с метилтрихлоридом);
– медицина и фармацевтика, а именно создание популярных и востребованных медикаментов, в частности производных фенольной к-ты. Это, прежде всего, аспирин, или ацетилсалициловая кислота – средство для понижения жара.
Это также салол – дезинфицирующий препарат, используемый при болезнях кишечника и мочевой системы.
Это и ПАСК, показанная при туберкулезе, и хорошо известный пурген (фенолфталеин) – лекарство со слабительным эффектом, и орасепт – препарат для обезболивания и антисептической обработки;
- – химия, а если быть точнее, то производство искусственного волокна, в частности капрона и нейлона;
- – легкая промышленность (дезинфекционная обработка шкур животных в составе кожно-меховых дубителей);
- – производство пластифицирующих составов для полимеров;
- – парфюмерная отрасль (изготовление парфюмерии);
- – косметология (задействуется как средство для глубокого хим. пилинга);
- – аналитическая химия (служит реагентом);
- – обработка с/х насаждений (выступает защитным средством для растений, входит в состав пестицидов);
- – скотоводство (дезинфекционные мероприятия, направленные на животных).
Мы перечислили много направлений, где не обходятся без фенола, но и это еще не все.
Из него создают антиоксиданты, неионогенные поверхностно-активные вещества, иные вещества фенольного класса, антисептики, взрывчатку, краски (гуашь), фотореактивы (проявляющие композиции для черно-белой бумаги), различные синтетические материалы. Благодаря ему, коптильный дым обретает консервирующие качества. Кроме того, консервантом гидроксибензол служит и для вакцин.
Раньше фенол активно использовали при изготовлении стройматериалов, товаров бытового назначения, пластика для различных изделий, в том числе игрушек.
Сегодня же это либо максимально сокращено, либо вообще запрещено, ввиду опасного воздействия на человеческий организм, в частности на нервную систему, сердце и сосуды, почки и печень, а также на иные внутренние органы.
Хотя до сих пор есть производители, которые, не смотря на все запреты и ограничения, используют фенол даже при создании игрушек для детей.
На заметку! Фенол как отдельное соединение используется в разных сферах, но еще в больших объемах в работу берутся его различные производные.
Опасность фенола
Данный реактив токсичен (принадлежит ко 2-му классу опасности хим. продуктов), является одним из пром. загрязнителей, способен наносить вред людям и животным. Кроме того, губительно воздействует на большое число микроорганизмов, как результат – биоочистка промышленных стоков, содержащих много фенола, сопровождается немалыми сложностями.
Контактируя с кожей, не только обжигает (а ожоги после могут еще и трансформироваться в язвы), но и всасывается внутрь, провоцируя отравления и пагубное воздействие на головной мозг. Попадая в организм сквозь органы дыхания, раздражает и опять же обжигает. Если площадь хим. ожога будет составлять 25 % и более, не исключен летальный исход.
Негативное воздействие фенола на организм может заключаться также в следующем: кашле, чихании, мигренях и головокружениях, побледнении, тошноте, потере сил, мышечной атрофии, язве желудка и двенадцатиперстной кишки.
Это не значит, что указанное вещество следует полностью вычеркнуть из жизни. Нужно правильно с ним обращаться, чтобы минимизировать риски, и тогда эффект, который с его помощью можно получить, порадует во всех смыслах. Используйте фенол правильно, соблюдая нормы, правила и технику безопасности, чтобы ни вам, ни другим людям, ни окружающей среде не было нанесено ни малейшего вреда.
Источник: https://www.systopt.com.ua/ru/chto-takoe-fenol-svojstva-y-prymenenye/
фенол, физические, химические свойства и применение фенола
Фенол (гидроксибензол, устар. карболовая кислота) C6H5OH — простейший представитель класса фенолов. Мировое производство фенола на 2006 год составляет 8,3 млн тонн/год. По объёму производства фенол занимает 33-е место среди всех выпускаемых химической промышленностью веществ и 17-е место среди органических веществ.
Получение, производство фенола
В настоящее время производство фенола в промышленном масштабе осуществляется следующими способами способами:
Кумольный метод получение фенола
Кумольный метод. Этим способом получают более 95 % всего производимого в мире фенола. В каскаде барботажных колонн кумол подвергают некаталитическому окислению воздухом с образованием гидропероксида кумола (ГПК). Полученный ГПК, при катализе серной кислотой, разлагают с образованием фенола и ацетона. Кроме того, ценным побочным продуктом этого процесса является α-метилстирол.
Окисление толуола, с промежуточным образованием бензойной кислоты
- Около 3 % всего фенола получают окислением толуола, с промежуточным образованием бензойной кислоты.
- Весь остальной фенол выделяют из каменноугольной смолы.
- Ведутся пилотные испытания установок получения фенола прямым окислением бензола закисью азота и кислотным разложением гидропероксида втор-бутилбензола.
- Фенол также можно получить восстановлением хинона.
Физические свойства
Представляет собой бесцветные игольчатые кристаллы, розовеющие на воздухе из-за окисления, приводящего к образованию окрашенных веществ (это связано с промежуточным образованием хинонов).
Обладает специфическим запахом (таким, как запах гуаши, так как в состав гуаши входит фенол). Умеренно растворим в воде (6 г на 100 г воды), в растворах щелочей, в спирте, в бензоле, в ацетоне.
5 % раствор в воде — антисептик, широко применяемый в медицине.
Химические свойства
Из-за наличия ароматического кольца и гидроксильной группы фенол проявляет химические свойства, характерные как для спиртов, так и для ароматических углеводородов.
По гидроксильной группе:
- Обладает слабыми кислотными свойствами (более сильными, чем у спиртов), при действии щелочей образует соли — феноляты (например, фенолят натрия — C6H5ONa):
- mathsf{C_6H_5OH + NaOH
ightarrow C_6H_5ONa + H_2O} - Фенол — очень слабая кислота; даже угольная кислота вытесняет его из фенолятов:
- {displaystyle {mathsf {C_{6}H_{5}ONa+H_{2}CO_{3}
ightarrow C_{6}H_{5}OH+NaHCO_{3)))) - Более интенсивно феноляты разлагаются под действием сильных кислот, например, серной:
- {displaystyle {mathsf {C_{6}H_{5}ONa+H_{2}SO_{4}
ightarrow C_{6}H_{5}OH+NaHSO_{4))))
Взаимодействие с металлическим натрием:
- mathsf{2C_6H_5OH + 2Na
ightarrow 2C_6H_5ONa + H_2uparrow} - Фенол непосредственно не этерифицируется карбоновыми кислотами, эфиры можно получить при взаимодействии фенолятов с ангидридами или галогенангидридами кислот:
- {displaystyle {mathsf {C_{6}H_{5}ONa+CH_{3}COCl
ightarrow C_{6}H_{5}OCOCH_{3}+NaCl))} - {displaystyle {mathsf {C_{6}H_{5}ONa+(CH_{3}CO)_{2}O
ightarrow C_{6}H_{5}OCOCH_{3}+CH_{3}COONa))}
Образование простых эфиров
Для получения простых эфиров фенола действуют галогеналканами или галогенпроизводными аренов на феноляты. В первом случае получают смешанные жирно-ароматические простые эфиры:
{displaystyle {mathsf {C_{6}H_{5}ONa+CH_{3}I
ightarrow C_{6}H_{5}OCH_{3}+NaI))}
Во втором случае получают чисто-ароматические простые эфиры:
- {displaystyle {mathsf {C_{6}H_{5}ONa+C_{6}H_{5}Cl{xrightarrow[{}]{Cu))C_{6}H_{5}OC_{6}H_{5}+NaCl))}
- Реакция проводится в присутствии порошкообразной меди, которая служит катализатором.
- При перегонке фенола с цинковой пылью происходит замещение гидроксильной группы водородом:
- {displaystyle {mathsf {C_{6}H_{5}OH+Zn
ightarrow C_{6}H_{6}+ZnO))}
По ароматическому кольцу:
Вступает в реакции электрофильного замещения по ароматическому кольцу.
Гидрокси-группа, являясь одной из самых сильных донорных групп (вследствие уменьшении электронной плотности на функциональной группе), увеличивает реакционную способность кольца к этим реакциям и направляет замещение в орто- и пара-положения. Фенол с лёгкостью алкилируется, ацилируется, галогенируется, нитруется и сульфируется.
- Реакция Кольбе — Шмитта служит для синтеза салициловой кислоты и её производных (ацетилсалициловой кислоты и других).
- {displaystyle {mathsf {C_{6}H_{5}OH+CO_{2}{xrightarrow[{}]{NaOH))C_{6}H_{4}OH(COONa)))}
- {displaystyle {mathsf {C_{6}H_{4}OH(COONa)+H_{2}SO_{4}
ightarrow C_{6}H_{4}OH(COOH)+NaHSO_{4)))) - Взаимодействие с бромной водой (качественная реакция на фенол):
- mathsf{C_6H_5OH + 3Br_2
ightarrow C_6H_2Br_3OH + 3HBr} - образуется 2,4,6-трибромфенол — твёрдое вещество белого цвета.
Взаимодействие с концентрированной азотной кислотой:
- mathsf{C_6H_5OH + 3HNO_3
ightarrow C_6H_2(NO_2)_3OH + 3H_2O} - Взаимодействие с хлоридом железа(III) (качественная реакция на фенол):
- mathsf{6C_6H_5OH + FeCl_3
ightarrow [Fe(C_6H_5OH)_6]Cl_3}
Реакция присоединения
- Гидрированием фенола в присутствии металлических катализаторов получают циклогексанол и циклогексанон:
- {displaystyle {mathsf {2C_{6}H_{5}OH+5H_{2}{xrightarrow {t,p,kat:Pt/Pd,Pd/Ni,Pd/Al_{2}O_{3},Ni/Cr/Al_{2}O_{3))}C_{6}H_{11}OH+C_{6}H_{10}O))}
- Окисление фенола
Вследствие наличия гидроксильной группы в молекуле фенола устойчивость к окислению намного ниже, чем у бензола. В зависимости от природы окислителя и условия проведения реакции получаются различные продукты.
- Так, под действием пероксида водорода в присутствии железного катализатора образуется небольшое количество двухатомного фенола — пирокатехина:
- {displaystyle {mathsf {C_{6}H_{5}OH+2H_{2}O_{2}{xrightarrow[{-H_{2}O}]{kat:Fe))C_{6}H_{4}(OH)_{2))))
- При взаимодействии более сильных окислителей (хромовая смесь, диоксид марганца в кислой среде) образуется пара-хинон.
Биологическая роль и значение
Протеиногенная аминокислота тирозин является структурным производным фенола и может быть рассмотрена как пара-замещённый фенол или α-замещённый пара-крезол.
В природе распространены и другие фенольные соединения, в том числе полифенолы. В свободном виде фенол встречается у некоторых микроорганизмов и находится в равновесии с тирозином.
Равновесие поддерживает фермент тирозин-фенол-лиаза (КФ 4.1.99.2).
Биологическое значение фенола обычно рассматривается в рамках его воздействия на окружающую среду. Фенол — один из промышленных загрязнителей. Фенол довольно токсичен для животных и человека. Фенол губителен для многих микроорганизмов, поэтому промышленные сточные воды с высоким содержанием фенола плохо поддаются биологической очистке.
Применение
- Ммировое потребление фенола имеет следующую структуру (данные 2006 г.):
- 44 % фенола расходуется на производство бисфенола А, который, в свою очередь, используется для производства поликарбонатов и эпоксидных смол;
- 30 % фенола расходуется на производство фенолформальдегидных смол;
- 12 % фенола гидрированием превращается в циклогексанол, используемый для получения искусственных волокон — нейлона и капрона;
- в России большое количество фенола используется в нефтепереработке, в частности для селективной очистки масел на технологических установках типа 37/1 и А-37/1. Фенол проявляет высокую селективность и эффективность при удалении из масел смолистых веществ, различных полициклических ароматических углеводородов с короткими боковыми цепями, а также соединений, содержащих серу;
остальной фенол расходуется на другие нужды, в том числе на производство антиоксидантов (ионол), неионогенных ПАВ — полиоксиэтилированных алкилфенолов (неонолы), других фенолов (крезолов), лекарственных препаратов (аспирин), антисептиков (ксероформа) и пестицидов. Раствор 1,4 % фенола применяется в медицине (орасепт) как обезболивающее и антисептическое средство.
Фенол и его производные обусловливают консервирующие свойства коптильного дыма. Также фенол используют в качестве консерванта в вакцинах. Пример использования, в качестве антисептика — препарат «Орасепт» и «Фукорцин». В косметологии как химический пилинг (токсично).
в скотоводстве: дезинфекция животных растворами фенола и его производных.
в косметологии для проведения глубокого пилинга.
Токсические свойства
Фенол ядовит. Относится к высокоопасным веществам (Класс опасности II). При вдыхании вызывает нарушение функций нервной системы. Пыль, пары и раствор фенола раздражают слизистые оболочки глаз, дыхательных путей, кожу, вызывая химические ожоги. Доказательства канцерогенности фенола для людей отсутствуют.
Предельно допустимые концентрации (ПДК) фенола:
- ПДКр.з. = 1 мг/м³
- ПДКр.с. = 0,3 мг/м³
- ПДКм.р. = 0,01 мг/м³
- ПДКс.с. = 0,003 мг/м³
- ПДКв. = 0,001 мг/л.
Попадая на кожу, фенол очень быстро всасывается даже через неповреждённые участки и уже через несколько минут начинает воздействовать на ткани головного мозга. Сначала возникает кратковременное возбуждение, а потом и паралич дыхательного центра.
Даже при воздействии минимальных доз фенола наблюдается чихание, кашель, головная боль, головокружение, бледность, тошнота, упадок сил.
Тяжелые случаи отравления характеризуются бессознательным состоянием, синюшностью, затруднением дыхания, нечувствительностью роговицы, скорым, едва ощутимым пульсом, холодным потом, нередко судорогами. Смертельная доза для человека при попадании внутрь 1—10 г, для детей 0,05—0,5 г[9].
Фенольная катастрофа в Уфе
Наглядный пример воздействия фенола на окружающую среду был продемонстрирован весной 1990 года в Уфе.
В результате техногенной аварии на предприятии ПО «Уфахимпром» произошла утечка большого количества фенола в речку Шугуровка, впадающую в более крупную реку Уфу, являющуюся источником хозяйственно-питьевого водоснабжения города Уфы. Загрязнение воды в районе Южного водозабора превышало ПДК более чем в 100 раз.
Опасность загрязнения питьевой воды фенолом проявляется в том, что при очистке вод использовался хлор, который, взаимодействуя с фенолом, образовывал хлорпроизводные (смесь хлорфенолов) — более токсичные вещества (некоторые в 100—250 раз превышают токсичность самого фенола). Было оповещено население Уфы об опасности употребления водопроводной воды для питья. Общая численность населения, потреблявшего питьевую воду, загрязненную фенолом из Южного водозабора Уфы, составила 672 876 человек
Источник: http://himsnab-spb.ru/articles/chemical_compounds/phenol_physical_chemical_properties_and_applications_of_phenol/




