Азот — неметаллический элемент Va группы периодической таблицы Д.И. Менделеева. Составляет 78% воздуха. Входит в состав белков, являющихся важной частью живых организмов.
Температура кипения азота составляет -195,8 °C. Однако быстрого замораживания объектов, которое часто демонстрируют в кинофильмах, не происходит. Даже для заморозки растения нужно продолжительное время, это связано с низкой теплоемкостью азота.

Общая характеристика элементов Va группы
От N к Bi (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Азот, фосфор и мышьяк являются неметаллами, сурьма — полуметалл, висмут — металл.

Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns2np3:
- N — 2s22p3
- P — 3s23p3
- As — 4s24p3
- Sb — 5s25p3
- Bi — 6s26p3
Основное и возбужденное состояние азота
При возбуждении атома азота электроны на s-подуровне распариваются и переходят на p-подуровень. Поскольку азот находится во втором периоде, то 3ий уровень у него отсутствует, что проявляется в особенностях электронной конфигурации возбужденного состояния.
Сравнивая возможности перемещения электронов у азота и фосфора, разница становится очевидна.

Природные соединения
В природе азот встречается в виде следующих соединений:
- Воздух — во вдыхаемом нами воздухе содержится 78% азота
- Азот входит в состав нуклеиновых кислот, белков
- KNO3 — индийская селитра, калиевая селитра
- NaNO3 — чилийская селитра, натриевая селитра
- NH4NO3 — аммиачная селитра (искусственный продукт, в природе не встречается)
Селитры являются распространенными азотными удобрениями, которые обеспечивают быстрый рост и развитие растений, повышают урожайность. Однако, следует строго соблюдать правила их применения, чтобы не превысить допустимые концентрации.

Получение
В промышленности азот получают путем сжижения воздуха. В дальнейшем путем испарения их сжиженного воздуха получают азот.
Применяют и метод мембранного разделения, при котором через специальный фильтр из сжатого воздуха удаляют кислород.

- В лаборатории методы не столь экзотичны. Чаще всего получают азот разложением нитрита аммония
- NH4NO2 → (t) N2 + H2O
- Также азот можно получить путем восстановления азотной кислоты активными металлами.
- HNO3(разб.) + Zn → Zn(NO3)3 + N2 + H2O

Химические свойства
Азот восхищает — он принимает все возможные для себя степени окисления от -3 до +5.
Молекула азота отличается большой прочностью из-за наличия тройной связи. Вследствие этого многие реакции эндотермичны: даже горение азота в кислороде сопровождается поглощением тепла, а не выделением, как обычно бывает при горении.
- Реакция с металлами
- N2 + Li → Li3N (нитрид лития)
- N2 + Mg → (t) Mg3N2
- N2 + Al → (t) AlN
- Реакция с неметаллами
Без нагревания азот взаимодействует только с литием. При нагревании реагирует и с другими металлами.
Важное практическое значение имеет синтез аммиака, который применяется в дальнейшим при изготовлении удобрений, красителей, лекарств. N2 + H2 ⇄ (t, p) NH3
Аммиак
Бесцветный газ с резким едким запахом, раздражающим слизистые оболочки. Раствор концентрацией 10% аммиака применяется в медицинских целях, называется нашатырным спиртом.

- Получение
- В промышленности аммиак получают прямым взаимодействием азота и водорода.
- N2 + H2 ⇄ (t, p) NH3
- В лабораторных условиях сильными щелочами действуют на соли аммония.
- NH4Cl + NaOH → NH3 + NaCl + H2O
- Химические свойства
- Аммиак проявляет основные свойства, окрашивает лакмусовую бумажку в синий цвет.
- Реакция с водой
- Основные свойства
- Как основание аммиак способен реагировать с кислотами с образованием солей.
- NH3 + HCl → NH4Cl (хлорид аммония)
- NH3 + HNO3 → NH4NO3 (нитрат аммония)
- Восстановительные свойства
Образует нестойкое соединение — гидроксид аммония, слабое основание. Оно сразу же распадается на воду и аммиак. NH3 + H2O ⇄ NH4OH
Поскольку азот в аммиаке находится в минимальной степени окисления -3 и способен только ее повышать, то аммиак проявляет выраженные восстановительные свойства. Его используют для восстановления металлов из их оксидов. NH3 + FeO → N2↑ + Fe + H2O NH3 + CuO → N2↑ + Cu + H2O Горение аммиака без катализатора приводит к образованию азота в молекулярном виде. Окисление в присутствии катализатора сопровождается выделением NO. NH3 + O2 → (t) N2 + H2O NH3 + O2 → (t, кат) NO + H2O
Соли аммония
- Получение
- NH3 + H2SO4 → NH4HSO4 (гидросульфат аммония, избыток кислоты)
- 3NH3 + H3PO4 → (NH4)3PO4
- Химические свойства
- Помните, что по правилам общей химии, если по итогам реакции выпадает осадок, выделяется газ или образуется вода — реакция идет.
- Реакции с кислотами
- Реакции с щелочами
- Реакции с солями
- Реакция гидролиза
- В воде ион аммония подвергается гидролизу с образованием нестойкого гидроксида аммония.
- NH4+ + H2O ⇄ NH4OH + H+
- NH4OH ⇄ NH3 + H2O
- Реакции разложения
- NH4Cl → (t) NH3↑ + HCl↑
- (NH4)2CO3 → (t) NH3↑ + H2O + CO2↑
- NH4NO2 → (t) N2↑ + H2O
- NH4NO3 → (t) N2O↑ + H2O
- (NH4)3PO4 → (t) NH3↑ + H3PO4
NH4Cl + H2SO4 → (NH4)2SO4 + HCl↑
В реакциях с щелочами образуется гидроксид аммония — NH4OH. Нестойкое основание, которое легко распадается на воду и аммиак. NH4Cl + KOH → KCl + NH3 + H2O
(NH4)2SO4 + BaCl2 = BaSO4↓ + NH4Cl
Оксид азота I — N2O
Закись азота, веселящий газ — N2O — обладает опьяняющим эффектом. Несолеобразующий оксид. При н.у. является бесцветным газом с приятным сладковатым запахом и привкусом. В медицине применяется в больших концентрациях для ингаляционного наркоза.
- Получают N2O разложением нитрата аммония при нагревании:
- NH4NO3 → N2O + H2O
- Оксид азота I разлагается на азот и кислород:
- N2O → (t) N2 + O2
Оксид азота II — NO
Окись азота — NO. Несолеобразующий оксид. При н.у. бесцветный газ, на воздухе быстро окисляется до оксида азота IV.
- Получение
- В промышленных масштабах оксид азота II получают при каталитическом окислении аммиака.
- NH3 + O2 → (t, кат) NO + H2O
- В лабораторных условиях — в ходе реакции малоактивных металлов с разбавленной азотной кислотой.
- Cu + HNO3(разб.) → Cu(NO3)2 + NO + H2O
- Химические свойства
- На воздухе быстро окисляется с образованием бурого газа — оксида азота IV — NO2.
- NO + O2 → NO2
Оксид азота III — N2O3
При н.у. жидкость синего цвета, в газообразной форме бесцветен. Высокотоксичный, приводит к тяжелым ожогам кожи.
- Получение
- Получают N2O3 в две стадии: сначала реакцией оксида мышьяка III с азотной кислотой, затем охлаждением полученной смеси газов до температуры — 36 °C.
- As2O3 + HNO3 → H3AsO 3 + NO↑ + NO2↑
- При охлаждении газов образуется оксид азота III.
- NO + NO2 → N2O3
- Химические свойства
Является кислотным оксидом. соответствует азотистой кислота — HNO2, соли которой называются нитриты (NO2-). Реагирует с водой, основаниями.
H2O + N2O3 → HNO2
NaOH + N2O3 → NaNO2 + H2O
Оксид азота IV — NO2
Бурый газ, имеет острый запах. Ядовит.
Получение
В лабораторных условиях данный оксид получают в ходе реакции меди с концентрированной азотной кислотой. Также NO2 выделяется при разложении нитратов.
Cu + HNO3(конц) → Cu(NO3)2 + NO2 + H2O
- Cu(NO3)2 → (t) CuO + NO2 + O2
- Pb(NO3)2 → (t) PbO + NO2 + O2
- Химические свойства
- Проявляет высокую химическую активность, кислотный оксид.
- Окислительные свойства
- Как окислитель NO2 ведет себя в реакциях с фосфором, углеродом и серой, которые сгорают в нем.
- NO2 + C → CO2 + N2
- NO2 + P → P2O5 + N2
- Окисляет SO2 в SO3 — на этой реакции основана одна из стадий получения серной кислоты.
- SO2 + NO2 → SO3 + NO
- Реакции с водой и щелочами
- NO2 + H2O → HNO3 + HNO2
- NO2 + LiOH → LiNO3 + LiNO2 + H2O
- Если растворение в воде оксида проводить в избытке кислорода, образуется азотная кислота.
- NO2 + H2O + O2 → HNO3
Оксид азота IV соответствует сразу двум кислотам — азотистой HNO2 и азотной HNO3. Реакции с водой и щелочами протекают по одной схеме.
Источник: https://studarium.ru/article/168
Урок 14. Азот и фосфор – HIMI4KA
Самоучитель по химии › Неорганическая химия
Азот — элемент пятой группы второго периода Периодической системы Менделеева.
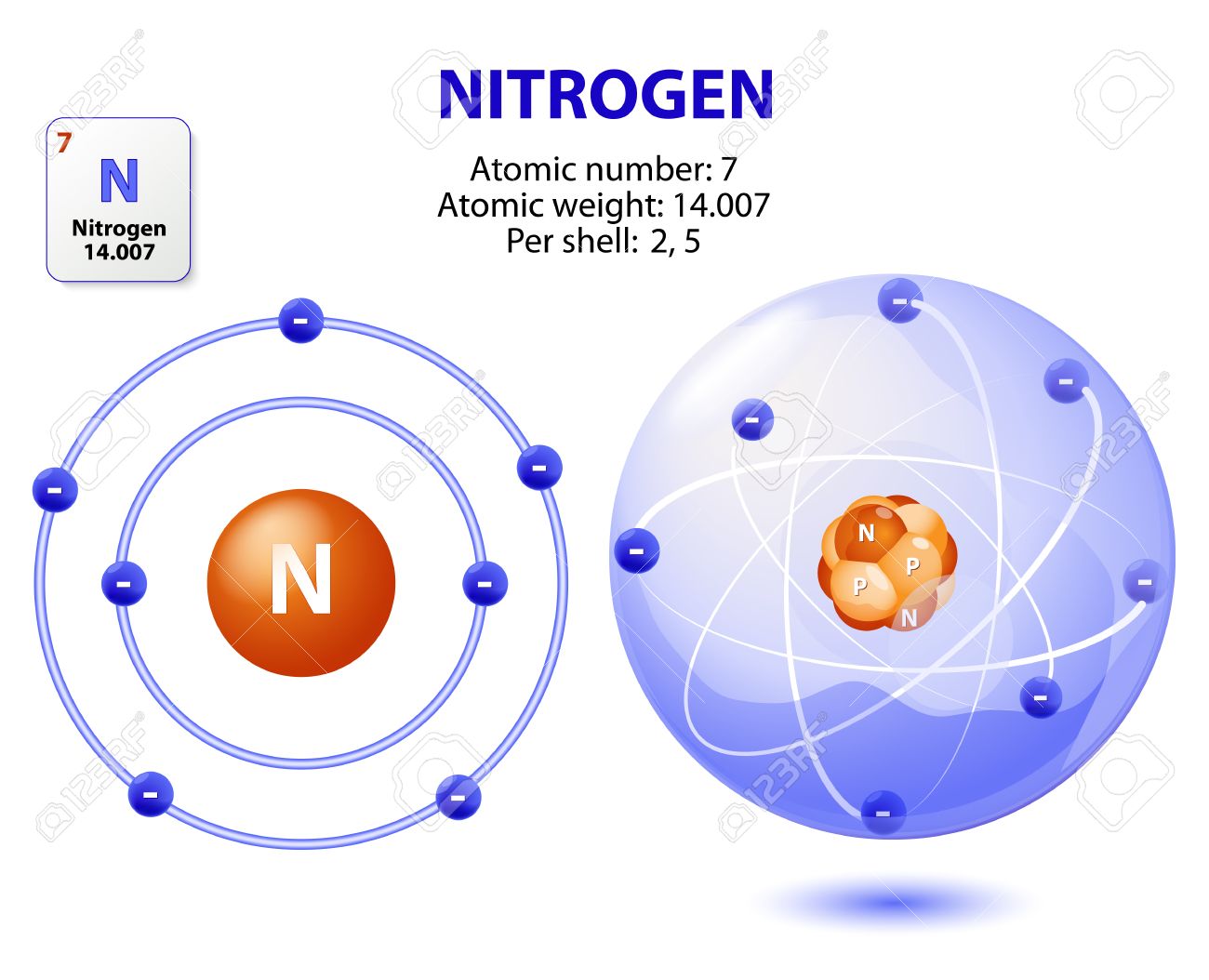
Задание 14.1. Опишите строение атома этого элемента.
Имея на внешнем энергетическом уровне пять электронов, азот является типичным неметаллом, т. е. способен и принимать и отдавать электроны:

Задание 14.2. Составьте формулы простейших соединений азота с высшей (+5) и низшей (–3) степенями окисления (в случае затруднений см. урок 3).
Задание 14.3. Определите степени окисления азота в соединениях:
![]()
В своих соединениях атом азота может проявлять любые степени окисления от –3 до +5. Свойства некоторых из этих соединений будут рассмотрены ниже.
Простое вещество — азот N2 — составляет 4/5 Земной атмосферы. Азот в виде соединений (белков) входит в состав всех живых существ. Неорганических соединений азота в земной коре очень мало: 0,002 % по массе.
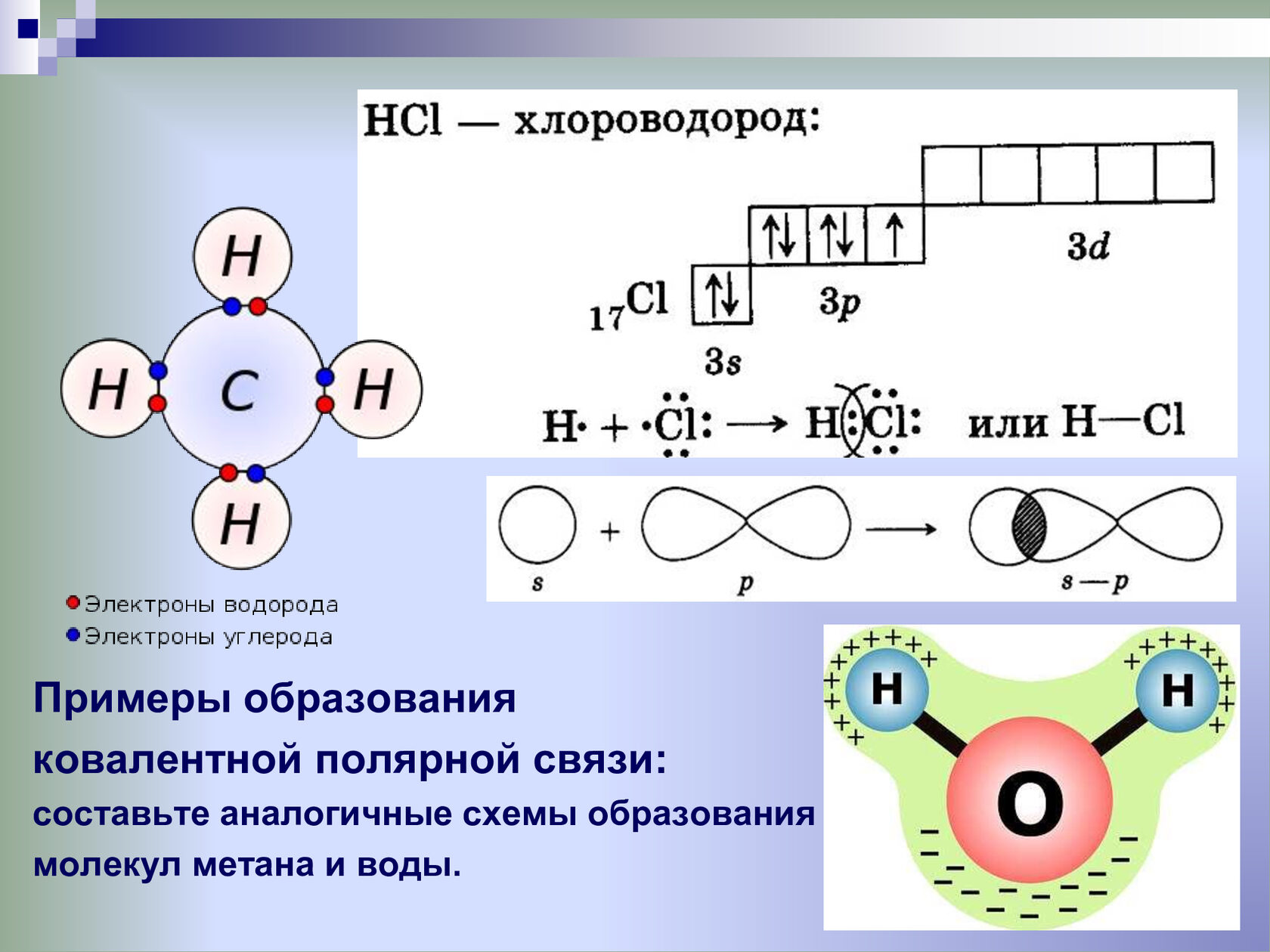
Вопрос. Какой тип химической связи соединяет атомы азота в его молекуле N2?
Поскольку в этой молекуле объединяются одинаковые атомы — связь ковалентная неполярная:

Кроме того, это — тройная связь, на разрыв которой требуется затратить очень много энергии. Поэтому при нормальных условиях азот не реагирует ни с одним веществом, кроме лития. При определённых условиях (нагревание, присутствие катализатора) азот реагирует с некоторыми металлами и неметаллами:

Задание 14.4. Расставьте коэффициенты. Определите, какие свойства (окислителя или восстановителя) проявляет азот в этих реакциях.
Поскольку атом азота в молекуле азота N2 имеет промежуточную степень окисления 0, в химических реакциях он может быть и окислителем и восстановителем:

Так как азот с трудом вступает в химические реакции, он относится к инертным газам и используется там, где нужно изолировать что-либо от окислительного действия кислорода: внутри баллона лампочки накаливания, атмосфера нефтехранилища и т. д.
Очень низкая температура кипения жидкого азота (–195,8 °C) позволяет быстро замораживать пищевые продукты и сохранять их в таком виде длительное время.
Важнейшими органическими соединениями азота являются белки, которые входят в состав любого живого организма. Но большинство живых существ не могут получать белки из атмосферного азота (связывать азот). Для этого нужны его соединения. Важнейшими неорганическими соединениями азота являются аммиак, азотная кислота и их соли.
Аммиак и соли аммония
Аммиак NH3 — бесцветный газ с резким запахом, ядовит.
Задание 14.5. Составьте электронную и графическую формулы аммиака и определите тип химической связи в этой молекуле.
Поскольку связь N-Н сильно полярна, аммиак очень хорошо растворяется в полярном растворителе (воде) и реагирует с нею:

Вопрос. Какую реакцию среды имеет полученный раствор?
В результате этой реакции в растворе появляется избыток ионов ОН–, поэтому раствор аммиака в воде (аммиачная вода, нашатырный спирт) имеет щелочную среду и проявляет свойства слабого основания.
Называется это основание «гидроксид аммония», и ему приписывают формулу NH4OH. Поскольку это щёлочь (растворимое основание), получаемая из летучего вещества (газа), её называют «летучей щёлочью».
Вопрос. Будет ли аммиак, а также его водный раствор реагировать с кислотами? щелочами?
Проявляя основные свойства, аммиак реагирует только с кислотами и не реагирует со щелочами:

В результате таких реакций образуются соли аммония, в которых вместо катиона металла имеется одновалентный катион аммония NH4+. Соли аммония имеют ряд особенностей:
1. Соли аммония, как соли слабого основания, реагируют со щелочами:
![]()
Задание 14.6. Составьте уравнение этой реакции в ионномолекулярном виде. Не забудьте, что гидроксид аммония — слабое основание.
Если такая реакция идёт при нагревании, то получается аммиак в виде газа. Это лабораторный способ получения аммиака:
Кроме того, появляется характерный запах — качественный признак присутствия солей аммония в смеси. Эту реакцию используют для получения аммиака в лаборатории.
Вопрос. Будут ли соли аммония подвергаться гидролизу?
2. Соли аммония, как соли слабого основания, подвергаются гидролизу:
Вопрос. Какая реакция среды получается в результате данного процесса?
Задание 14.7. Составьте уравнение реакции гидролиза нитрата аммония. Какой цвет имеет лакмус в этом растворе?
3. Соли аммония, как соли летучего основания, разлагаются при нагревании. При этом может выделяться аммиак:
- Но если соль образована кислотой, анион которой является сильным окислителем, аммиак не выделяется:
- Почему в этом случае не выделяется аммиак? Возможно, что сначала процесс идёт как обычно:
- Но поскольку азотная кислота — окислитель, а аммиак — восстановитель, они тут же реагируют друг с другом. При разложении нитрата аммония возможны и другие продукты реакции:
Задание 14.8. Составьте электронный баланс для реакций (1) и (2), укажите окислитель и восстановитель.
Вопрос. Почему атом азота в аммиаке проявляет восстановительные свойства? Может ли этот атом принимать электроны?
Атом азота в молекуле аммиака имеет низшую степень окисления –3 и поэтому способен только отдавать электроны и проявлять восстановительные свойства. Поэтому аммиак легко реагирует с окислителями, например с кислородом, и горит:
Реакция (3) практического смысла не имеет: зачем возвращать в атмосферу азот, который только что с таким трудом был превращён в аммиак? Зато реакция (4) каталитического окисления аммиака используется при получении азотной кислоты. Кроме того, аммиак и его соли применяются как азотные удобрения, а нитрат аммония входит в состав взрывчатых смесей.
Азотная кислота и её соли
Азотную кислоту получают в три стадии. Первая — каталитическое окисление аммиака. Полученный бесцветный газ NO окисляют в бурый газ NO2:
Эта реакция идёт даже при нормальных условиях. Полученный бурый газ NO2 очень ядовит, имеет резкий запах. Растворением его в воде в присутствии кислорода получают азотную кислоту:
- Азотная кислота — очень сильный электролит, в растворе полностью диссоциирует на ионы:
Вопрос. Какие свойства проявляет атом азота азотной кислоты в окислительно-восстановительных реакциях?
- Поскольку атом азота в азотной кислоте находится в высшей степени окисления +5, азотная кислота — сильный окислитель. Она окисляет и простые и сложные вещества:
- Органические вещества, входящие в состав бумаги, хлопка, скипидара, могут загореться при соприкосновении с концентрированной азотной кислотой. Не удивительно поэтому, что при взаимодействии металлов с азотной кислотой не удаётся получить водород в качестве продукта реакции:
- Действительно, водород — восстановитель, а азотная кислота — окислитель, и они легко реагируют друг с другом в момент выделения водорода. В результате таких реакций образуются оксиды азота или аммиак, который образует с азотной кислотой соль аммония:
- Обратите внимание.
- Концентрированная азотная кислота не реагирует с алюминием, хромом и железом, так как образует на их поверхности прочную оксидную плёнку, которая предохраняет металл от дальнейшего окисления (пассивирует его).
- Азотная кислота реагирует даже с теми металлами, которые стоят в ряду напряжений после водорода (водород и здесь НЕ выделяется!).
- Продукт реакции зависит и от активности металла и от разбавления кислоты: чем активнее металл и чем разбавленнее кислота, тем сильнее восстанавливается кислота, т. е. сильнее изменяется степень окисления атома азота (вплоть до –3).
Задание 14.9. Расставьте коэффициенты в этих уравнениях реакций, пользуясь методом электронного баланса.
В любой из этих реакций образуется соль азотной кислоты — нитрат. Нитраты — это хорошо растворимые соли, применяемые часто в качестве удобрений (KNO3, NH4NO3).
Соединения азота используются в качестве удобрений, поскольку растения, как и человек, не способны усваивать азот воздуха, т. е. не способны превращать N2 в органические соединения азота.
А без этих соединений — аминокислот, белков, нуклеиновых кислот — жизнь в принципе невозможна.
- При использовании таких удобрений следует помнить, что избыток нитратов в почве и растениях опасен для жизни, так как нитраты ядовиты!
- Нитраты легко разлагаются при нагревании, причём продукты разложения зависят от активности металла. Так, нитраты очень активных металлов — селитры — разлагаются по схеме:
Задание 14.10. Составьте уравнение реакции разложения нитрата натрия.
Селитры входят в состав взрывчатых веществ. Так, нитрат калия входит в состав чёрного пороха. Действием на сухие нитраты концентрированной серной кислотой можно получить азотную кислоту.
Строение атома и свойства фосфора
Фосфор был получен и назван алхимиком Брандом*, который пытался найти философский камень.
* БРАНД Хённинг (ок. 1630–после 1710) — немецкий алхимик без специального образования, профессиональный военный.
Этот камень, по убеждению алхимиков, мог превращать металлы в золото, обладал магическими свойствами. В 1669 году Бранд из остатков прозаической мочи выделил вещество, которое светилось в темноте.
Безусловно, такими свойствами мог обладать только философский камень! Увы, никакими чудодейственными свойствами это вещество не обладало, но способность свечения в темноте подарило веществу и химическому элементу имя: его назвали фосфор, что означает «несущий свет».
Задание 14.11. Составьте электронную схему строения атома фосфора, укажите распределение валентных электронов, возможные степени окисления.
- Распределение валентных электронов атома фосфора:
- Поэтому фосфор проявляет в соединениях степени окисления –3, +3 и +5.
Задание 14.12. Составьте формулы водородных соединений, оксидов и гидроксидов фосфора, которые соответствуют этим степеням окисления.
Ниже мы рассмотрим свойства этих соединений, но вначале следует описать свойства простого вещества.
Как и для углерода, для фосфора характерно несколько аллотропных модификаций. В природе они не встречаются ввиду высокой активности этого неметалла.
Почему, собственно, светился фосфор, полученный алхимиком? Потому что это был белый фосфор. Он имеет состав Р4.
Это неполярное вещество, легко испаряется (возгоняется), причём пары белого фосфора окисляются на воздухе. При этом энергия химической реакции переходит в световую:
Появляется свечение.
Полученный оксид проявляет ярко выраженный кислотные свойства, так как фосфор — активный неметалл, а степень окисления атома фосфора — высшая. Поэтому при попадании на кожу белого фосфора появляются глубокие, плохо заживающие ожоги. Кроме того, белый фосфор, его пары — токсичное вещество. Белый фосфор — желтоватое мягкое вещество, растворимое в неполярных растворителях.
В противоположность ему — красный фосфор достаточно инертное вещество, безвредное для человека, но при условии, что оно — абсолютно чистое. Примеси белого фосфора, которые довольно часто встречаются, делают его ядовитым.
В чём причина такого разительного изменения свойств? В том, что красный фосфор и другие аллотропные модификации фосфора — являются неорганическими полимерами. И чем выше степень полимеризации, тем инертнее вещество, тем темнее цвет.
В настоящее время кроме чёрного фосфора описаны свойства жёлтого, алого, фиолетового, коричневого и даже стеклообразного.
Чаще всего встречаются и используются белый, красный и чёрный фосфор. Рассмотрим свойства красного фосфора.
Красный фосфор — это красно-бурый аморфный порошок практически нерастворимый в воде и неполярных растворителях, поскольку это полимер. Степень полимеризации установить невозможно, поэтому химическая формула Р. В зависимости от того, происходит ли горение в избытке или недостатке кислорода, образуются разные оксиды:
- Кроме того, фосфор реагирует с активными металлами и неметаллами:
Задание 14.13. Составить уравнение реакции фосфора с кальцием. Назвать полученное вещество.
Фосфиды, как и нитриды, силициды, разлагаются водой и кислотами. В результате образуется фосфин — ядовитый газ с неприятным чесночным запахом. Он способен самовоспламеняться на воздухе:
Именно огоньки-вспышки этого газа пугают прохожих на кладбищах, поскольку фосфин образуется при гниении белковых тел. А это означает, что фосфор, как и азот, — биогенный элемент. Биологические свойства соединений фосфора будут рассмотрены ниже.
Вышеперечисленные реакции подтверждают ранее установленное правило: атомы с промежуточной степенью окисления проявляют свойства и окислителя, и восстановителя. Восстановительные свойства фосфора проявляются при взаимодействии с бертолетовой солью KClO3:
Эта реакция начинается при лёгком нагревании, трении, а иногда и без причин. В результате может произойти сильная вспышка. Мы её наблюдаем всякий раз, как только чиркаем спичкой о спичечный коробок. В состав спичечной головки входит бертолетова соль KClO3 и сера, а в состав намазки — красный фосфор и толчёное стекло.
Свойства и значение соединений фосфора
Как уже было показано выше, фосфор образует два вида оксидов Р2О3 и Р2О5. Это кислотные оксиды, образующие с водой фосфористую кислоту Н3РО3 и несколько фосфорных кислот. Состав фосфорных кислот отражает формула х Р2О5 · у Н2О:
- Метафосфорная кислота неустойчива и, присоединяя воду, превращается в более устойчивую кислоту:
- Или в суммарном виде:
- Ортофосфорная кислота диссоциирует в три стадии:
Поэтому она образует три вида солей: КН2РО4 — дигидрофосфат, К2НРО4 — гидрофосфат, К3РО4 — фосфат. Эти соли, их растворы имеют разные свойства. Так, если большинство фосфатов нерастворимы в воде, кислые фосфаты имеют бОльшую растворимость.
Поскольку фосфор химически активен, в природе встречаются только нерастворимые соединения фосфора, в основном фосфаты. Они составляют основу таких минералов как апатиты и фосфориты. Основу фосфоритов составляет фосфат кальция, а в состав апатитов кроме него входят хлориды и фториды кальция.
Аналогичный состав имеют наши кости (фосфориты) и зубы (фторапатиты). В теле взрослого человека до 1,5 кг этого химического элемента. Таким образом, фосфор — биогенный элемент.
Атомы фосфора входят в состав ДНК и РНК (нуклеиновых кислот), которые хранят и воспроизводят генетическую информацию.
Кроме того, атомы фосфора входят в состав АТФ (аденозинтрифосфорной кислоты), при гидролизе которой выделяется аккумулированная в этой молекуле энергия.
- Фосфор в чистом виде получают при нагревании измельчённых фосфоритов с песком и коксом:
- Полученный фосфор используется при изготовлении спичек и пиротехнических составов, ядохимикатов, СМС (синтетических моющих средств) и многого другого.
Выводы
Азот — это элемент жизни, поскольку он входит в состав любого живого организма в виде белков, нуклеиновых кислот. С другой стороны, газ азот обладает инертными свойствами, с трудом вступает в химические реакции, составляет основу атмосферы Земли. Фосфор совместно с азотом входит в состав ДНК, РНК, АТФ. Многочисленные соединения фосфора незаменимы в быту.
Источник: https://himi4ka.ru/samouchitel-po-himii/urok-14-azot-i-fosfor.html
Презентация " Азот. Строение атома"









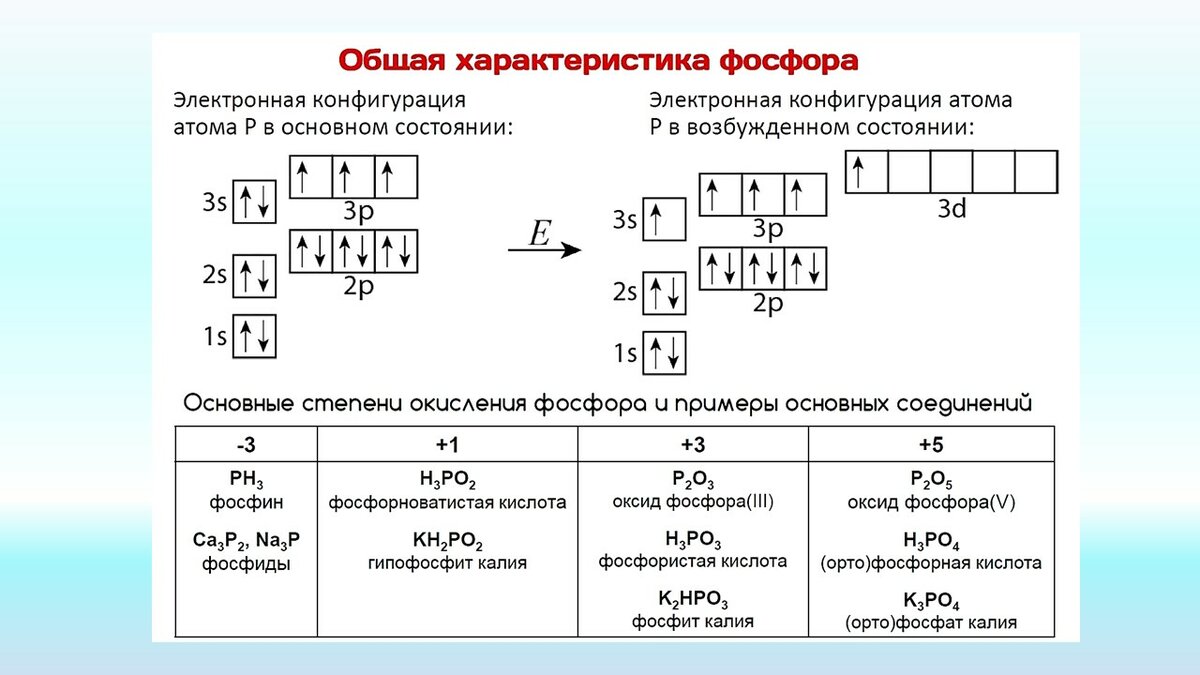
Описание презентации по отдельным слайдам:
1 слайд Описание слайда:
Урок химии 8 класс Учитель химии Феньшина Ольга Сергеевна
2 слайд Описание слайда:
Азот: положение в П.С.Э., строение атома, нахождение в природе, получение и свойства. Применение азота.
3 слайд Описание слайда:
ЦЕЛИ : Сформировать представление о строении атома и молекулы азота. Рассмотреть физические и химические свойства азота в свете ОВР. Показать значение азота как биогенного элемента.
4 слайд Описание слайда:
ПЛАН УРОКА История открытия Нахождение в природе Строение и свойства атома и молекулы Физические и химические свойства Получение и применение
5 слайд Описание слайда:
ДЕВИЗ УРОКА : «Нет жизни без азота, ибо он является непременной составной частью белков.» Д.Н.Прянишников
6 слайд Описание слайда:
ИСТОРИЯ ОТКРЫТИЯ 1772г. К.Шееле и Г.Кавендиш получили азот Д.Резерфорд описал получение и свойства 1787г. Лавуазье предложил название азот – «безжизненный» (а – нет, зоэ – жизнь) Многочисленные названия: нечистый гас, удушливый гас, септон, испорченный воздух, огорюченный воздух, селитрород, гнилотвор, смертельный гас, нитроген и др.
7 слайд Описание слайда:
НАХОЖДЕНИЕ В ПРИРОДЕ: 1)в свободном состоянии в атмосфере (78%), 2)в связанном состоянии (смотри таблицу) Природная форма Оболочка Земли Соли аммония и азотной кислоты Литосфера, гидросфера Азот Атмосфера Азот и аммиак вулканов Литосфера Соединения в некоторых видах топлива (нефть, уголь) Литосфера Нуклеиновые кислоты, белковые вещества Биосфера
8 слайд
9 слайд Описание слайда:
Вот, что писали знаменитые учёные об Азоте: Ф. Энгельс – «Жизнь есть способ существования белковых тел на Земле» Д. Резерфорд – «Удушливый воздух» К. Шееле – «Дурной возух» А. Лавуазье – «Безжизненный воздух» Д.И. Прянишников – «Нет жизни без азота, ибо он является важнейшей составляющей частью белковой молекулы».
10 слайд Описание слайда:
Постановка проблемы: Азот – «безжизненный» элемент или важная составная часть жизни на Земле?
11 слайд Описание слайда:
СТРОЕНИЕ И СВОЙСТВА АТОМА ? период, ? группа, ? подгруппа Содержит на внешнем энергетическом уровне ? электронов +7 ) ) ? ? ? N0 + 3e- N-3 * Составьте формулы соединений N с Li, Са, Al. ? N0 –1,2,3,4,5e- N+1,N+2,N+3,N+4,N+5 * Составьте формулы оксидов 3 1 2 4
12 слайд Описание слайда:
СТРОЕНИЕ И СВОЙСТВА АТОМА 2 период, 5 группа, главная подгруппа Содержит на внешнем энергетическом уровне 5 электронов +7 ) ) 2 5 Окислитель N0 + 3e- N-3 * Составьте формулы соединений N с Li, Са, Al. Восстановитель N0 –1,2,3,4,5e- N+1,N+2,N+3,N+4,N+5 * Составьте формулы оксидов 3 1 2 4
13 слайд Описание слайда:
N +7 2е- 5е- 1s 2s 2p 2 2 3 1s 2s 2p
14 слайд Описание слайда:
Проверь себя Li3N, Ca3N2, AlN, H3N N2O, NO, N2O3, NO2, N2O5.
15 слайд Описание слайда:
Возможные степени окисления 0 +1 +2 +3 +4 +5 -3 N2 N2O3 NO2 N2O5 NH3 NO N2O
16 слайд Описание слайда:
Цель урока: На примере сведений об азоте, привести аргументы в пользу двух точек зрения об элементе: Азот – «безжизненный». 2. Азот – главный элемент жизни на Земле.
17 слайд Описание слайда:
План изучения азота: Строение молекулы Физические свойства Химические свойства Способы получения Применение азота и его значение
18 слайд Описание слайда:
СТРОЕНИЕ МОЛЕКУЛЫ N N N N СВЯЗЬ: -КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ -ТРОЙНАЯ -ПРОЧНАЯ МОЛЕКУЛА: -ОЧЕНЬ УСТОЙЧИВАЯ -НИЗКАЯ РЕАКЦИОННАЯ СПОСОБНОСТЬ 1 3 4 2
19 слайд Описание слайда:
N2 молекулярная формула N N электронная формула структурная формула Ковалентная неполярная связь
20 слайд Описание слайда:
ФИЗИЧЕСКИЕ СВОЙСТВА. Газ без цвета, запаха и вкуса Плохо растворим в воде Немного легче воздуха Tºпл.= -210ºС Tºкип.= -196ºС
21 слайд Описание слайда:
азот — простое вещество , В, Ц, З, М N2 Ткип = — 195 С Тпл = — 210 С 0 0
22 слайд Описание слайда:
ХИМИЧЕСКИЕ СВОЙСТВА Задание: дать полную характеристику реакциям *; при каких условиях (с, t, р) равновесие сместится вправо. Окислительные N20 2N-3 При нагревании с другими металлами(Ca, Al, Fe) При комнатной tº только с Li *При высокой tº, р, kat (Fe, оксиды Al, K) с H2 Восстановительные N20 2N+2 *При tº электрической дуги (3000 — 4000ºС) с О2
23 слайд Описание слайда:
ПРОВЕРЬ СЕБЯ N2+3H2 ═ 2NH3 +Q Обратимая Соединения Экзотермическая Гомогенная Каталитическая с N2 и H2 увеличить tº уменьшить р увеличить N2+O2 ═ 2NO –Q Обратимая Соединения Эндотермическая Гомогенная Некаталитическая с N2 и O2 увеличить tº увеличить р не влияет
24 слайд Описание слайда:
получение в лаборатории в промышленности NH4NO2 → N2 + 2H2 t Выделение из сжиженного воздуха
25 слайд Описание слайда:
Применение Получение аммиака Создание инертной атмосферы Создание низких температур Насыщение поверхности стали для повышения прочности Жидкий азот в медицине Синтез аммиака Производство удобрений Синтез азотной кислоты Создание инертной среды N2
26 слайд Описание слайда:
Вопросы для самоконтроля Газ без цвета , вкуса и запаха Молекула двухатомна Содержание в воздухе 78 % В лаборатории получают разложением KMnO4 и H2O2 В промышленности – из жидкого воздуха Химически малоактивен Взаимодействует почти со всеми простыми веществами С ним связаны процессы дыхания и фотосинтеза Является составной частью белков Участвует в круговороте веществ в природе
27 слайд Описание слайда:
ПРОВЕРЬ СЕБЯ O2 1, 2, 4, 5, 7, 8, 10. « 5 » N2 1, 2, 3, 5, 6, 9, 10. « 5 » 1-2 ошибки « 4 » 3-4 ошибки « 3 » 5 ошибок и более « 2 » На примере сведений об азоте, приведите аргументы в пользу двух точек зрения: 1. Азот – «безжизненный» 2. Азот – главный элемент жизни на Земле.
28 слайд Описание слайда:
Домашнее задание Параграф №23 , выполнить задания 1,3 на странице 111 Составить рассказ на тему: «Путешествие азота в природе»
Скрыть
Важно! Узнайте, чем закончилась проверка учебного центра «Инфоурок»?
Общая информация
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Источник: https://infourok.ru/prezentaciya-azot-stroenie-atoma-1596464.html
Соединения азота образованные связью по донорно-акцепторному механизму. Электронное строение молекулы N2 с позиций методов ВС и МО
Задача 880. Привести примеры соединений азота, в молекулах которых имеются связи, образованные по донорно-акцепторному механизму.Решение:Связь по донорно-акцепторному механизму (координационная связь) образуется за счёт обобществления электронной пары одного атома (донор) и вакантной орбитали другого атома (акцептор).
Несвязывающая электронная пара атома азота способна с ионом водорода, имеющим свободную атомную орбиталь , образовывать ковалентную связь по донорно-акцепторному механизму. Так образуется катион аммония NH4+ из молекулы аммиака и иона водорода:
![]()
В результате образования донорно-акцепторной связи несвязывающая электронная пара атома азота становится связывающей, образуется четыре связи между одним атомом азота и четырьмя атомами водорода:
Все четыре связи равнозначны и по длине, и по энергии.
Такая связь идентична ковалентной связи, образованной по обычному механизму, обобществлению неспаренных электронов двух атомов.
У аммиака и его производных, за исключением тригалогенидов азота, сильно выражена электроно-донорная способность. Поэтому аммиак, также практически все соединения, имеющие аминогруппы и группы: являются N-донорными лигандами, образующими комплексные соединения с катионами многих металлов. Имеются комплексы со следующими группами:  глицианат-ион:
глицианат-ион: ![]() глицилглицилцианат-ион:
глицилглицилцианат-ион:![]() , этилендиамин:
, этилендиамин:![]() диэтилентриамин:
диэтилентриамин:
и др.. Связь в комплексных соединениях можно объяснить координационной связью между несвязывающими электронными парами атома азота лиганда и свободными орбиталями атома комплексообразователя, например, [Ag(NH3)2]Cl2, [Ni(en)2(NH3)2]Cl2 и др.
В аммиаке Н3 и аминах как производных аммиака.
Атом азота может образовывать координационную связь, например: хлорид аммония NH4Cl, гидроксид метиламмония CH3—NH3—OH, иодид тетраметиламмония (CH3)4NI, гидроксид тетраэтиламмония (С2Н5)4NOH, гидроксид аммония NH4OH, хлорид фениламина С6Н5NH3+Cl. Некоторые
производные аммиака, например: гидразин: , гидроксиламин: , а также хлорид гидразония N2H5Cl (+1), гидроксид гидразония N2H5(ОН)2 (+2), гидроксид гидроксиламмония [NH3OH]OH, гидроксид гидразония (+2) N2H6(OH)2, хлорид гидразония (+2) N2H6Cl2, хлорид гидроксиламмония NH3OHCl.
Задача 881. Описать электронное строение молекулы N2 с позиций методов ВС и МО.Решение:
а) Электронное строение молекулы N2 с позиций метода валентных связей
Атом азота на внешнем электронном слое содержит два спаренных электрона на 2s-подуровне и три неспаренных электрона на 2р-подуровне, по одному на каждой 2р-орбитали. Между двумя атомами азота образуется ковалентная связь тремя электронными парами за счёт спаривания трёх неспаренных электронов каждого атома.
Спаренные электроны 2s-орбиталей каждого атома азота не участвуют в образовании связей. Поэтому молекулу N2 в соответствии с теорией валентных связей можно изобразить как имеющую несвязывающие электронные пары у каждого атома азота: — = — , но в действительности электронная плотность сосредоточена в основном между атомами. Молекула N2 имеет линейное строение.
Так как атомы азота в молекуле N2 одинаковы, то дипольный момент молекулы равен нулю.
б) Электронное строение молекулы N2 с позиций метода Молекулярных орбиталей
- Электронное строение молекулы N2 можно объяснить с позиций метода молекулярных орбиталей.
- С позиций метода МО электронное строение молекулы N2 можно представить так:
- Молекула имеет электронную конфигурацию:
- KK(σ[2s)2(σ2s)2(π2ру)2π2рz)2(π2рx)2
Десять электронов 2s- и 2р-подуровней двух атомов азота заполняют пять молекулярных орбиталей.
Расположенные ниже остальныхσ 2s- и σ*2s-орбитали (связывающая и разрыхляющая) из-за компенсации своих энергетических вкладов практически ничего не вносят в энергию образования молекулы N2. Заполнение трёх последующих связывающих орбиталей соответствует образованию σ2р- и двух π2р-связей.
Суммарная энергия тройной связи в молекуле N2 очень велика (941 кДж/моль). Разрыхляющие орбитали π*2рz- и π*2ру, расположены гораздо выше, чем верхняя связывающая σ2рх-орбиталь.
Поэтому переход электрона с верхней связывающей орбитали на одну из разрыхляющих орбиталей требует затраты значительной энергии (примерно 100 кДж/моль). По этой причине возбуждение молекулы N2 – трудный (энергоёмкий) процесс. Этим и объясняется высокая химическая инертность молекулы N2. Энергии фотона недостаточно для возбуждения молекулы N2, поэтому азот не имеет цвета во всех состояниях.
В молекуле N2 порядок связи равен разности чисел электронов на связывающих и разрыхляющих орбиталях, делённой на 2:
ω= (6 — 0)/2 = 3
Отсутствие не спаренных электронов в молекуле N2 придаёт ей диамагнитные свойства (в магнитном поле диамагнитные молекулы приобретают небольшой магнитный момент, направленный против внешнего поля, и поэтому слабо выталкиваются из поля).
Итак, с позиций метода ВС можно объяснить линейное строение молекулы N2, отсутствие дипольного момента. Из-за отсутствия электрического дипольного момента между молекулами N2 возникают дисперсионные силы межмолекулярного взаимодействия (силы Ван-дер-Ваальса).
По этой же причине у азота малая растворимость в полярных растворителях, например, в воде; очень низкие температуры кипения и плавления. Диамагнитность молекулы N2 можно объяснить только с позиции метода МО – наличие неспаренных электронов на молекулярных орбиталях.
Валентность (ковалентность) атомов азота объясняется с позиций метода ВС как равная 3 (число неспаренных электронов атома азота, участвующих в образовании трёх ковалентных связей), то в методе МО вместо понятия «валентность» используется понятие «порядок связи» (в молекуле N2 равный 3).
Физические свойства азота (температуры кипения и плавления, цвет, диамагнитность и др.) лучше объясняются с позиций метода МО, равно как и химическая инертность.
Задача 882. Привести примеры реакций, в которых азот играет роль окислителя, и пример реакции, в которой он является восстановителем.Решение:а) Реакции, в которых азот играет роль окислителя:
В данных реакциях атом азота понижает свою степень окисления, т. е. проявляет свойства окислителя.
- б) Пример реакции, в которой азот проявляет свойства восстановителя:
- Атом азота в данной реакции повышает свою степень окисления от +3 до +5.
Источник: http://buzani.ru/zadachi/khimiya-glinka/1287-elektronnoe-stroenie-azota-zadachi-880-882
Азот N
Азот в таблице менделеева занимает 7 место, в 2 периоде.
| Символ | N |
| Номер | 7 |
| Атомный вес | 14.0064300 |
| Латинское название | Nitrogenium |
| Русское название | Азот |
Как самостоятельно построить электронную конфигурацию? Ответ здесь N: 1s2 2s2 2p3 Короткая запись:
N: 1s2 2s2 2p3
- Одинаковую электронную конфигурацию имеют атом азота и C-1, O+1
- Порядок заполнения оболочек атома азота (N) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
- На подуровне ‘s’ может находиться до 2 электронов, на ‘s’ — до 6, на ‘d’ — до 10 и на ‘f’ до 14
- Азот имеет 7 электронов, заполним электронные оболочки в описанном выше порядке:
- 2 электрона на 1s-подуровне
- 2 электрона на 2s-подуровне
- 3 электрона на 2p-подуровне
Степень окисления азота
Атомы азота в соединениях имеют степени окисления 5, 4, 3, 2, 1, 0, -1, -2, -3.
Степень окисления — это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается, то степень окисления положительная.
Ионы азота
N 0
Валентность N
Атомы азота в соединениях проявляют валентность V, IV, III, II, I.
Валентность азота характеризует способность атома N к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа N
Квантовые числа определяются последним электроном в конфигурации, для атома N эти числа имеют значение N = 2, L = 1, Ml = 1, Ms = ½
Видео заполнения электронной конфигурации (gif): 

Источник: https://k-tree.ru/tools/chemistry/periodic.php?element=N&oxidation=2
Азот — характеристика элемента, физические и химические свойства простого вещества. Аммиак, соли аммония
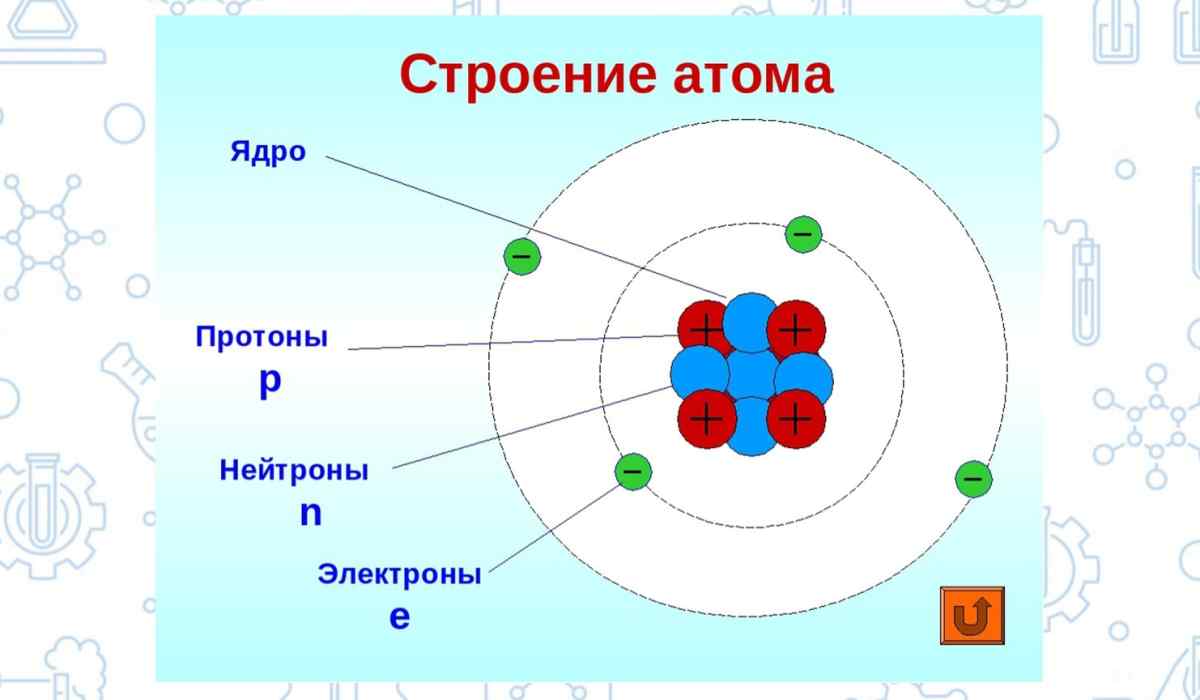 Азот (N) находится во втором периоде, пятой группе главной подгруппы. Порядковый номер – 7, Ar – 14,008.
Азот (N) находится во втором периоде, пятой группе главной подгруппы. Порядковый номер – 7, Ar – 14,008.
Молекула N2 – самая прочная из всех двухатомных за счет наличия тройной связи малой длины (энергия связи – 946 кДж). Связь в молекуле ковалентная неполярная.
Физические свойства: бесцветный газ, без запаха и вкуса; малорастворим в воде: в 1 л H2O растворяется 15,4 мл N2 при t° = 20 °C и p = 1 атм; t кипения =-196 °C; t плавления =-210 °C. Природный азот состоит из двух изотопов с атомными массами: 14 и 15.
Химические свойства азота: Атом азота имеет 7 электронов, из них 5 на внешнем уровне (5 валентных электронов). Он является одним из самых электроотрицательных элементов (3,04 по шкале Полинга), уступая лишь хлору (3.16), кислороду (3,44) и фтору (3,98).
Характерная валентность – 3 и 4.
Наиболее характерные степени окисления: -3, -2, -1, +2, +3, +4, +5, 0. В обычных условиях азот подобен инертному газу.
В обычных условиях азот непосредственно взаимодействует лишь с литием с образованием Li3N. При нагревании (то есть активации молекул N2) или воздействии электрического разряда вступает в реакцию со многими веществами, обычно выступает как окислитель (азот по электроотрицательности на 3 месте после кислорода и фтора) и лишь при взаимодействии со фтором и кислородом – как восстановитель.
N2 + 3H2 ↔ 2NH3
N2 + 2B → 2BN
3Si + 2N2 → Si3N4
3Ca + N2 → Ca3N2
N2 + O2 → 2NO.
Получение азота. В промышленности азот получают путем сжижения воздуха с последующим испарением и отделением азота от других газовых фракций воздуха (перегонка). Полученный азот содержит примеси благородных газов (аргона).
- В лабораториях обычно используется азот, доставляемый с производства в стальных баллонах под повышенным давлением или жидкий азот в сосудах Дьюара. Можно получать азот разложением некоторых его соединений:
- NH4NO2 → N2 + 2H2O (при to)
- (NH4)2Cr2O7 → N2 + Cr2O3 + 4H2O (при to)
- 2N2O → 2N2 + O2 (при to)
- Особо чистый азот получают термическим разложением азида натрия:
- 2NaN3 → 2Na + 3N2 (при to)
Нахождение в природе: в природе азот встречается в основном в свободном состоянии. Содержание азота в воздухе — его объемная доля 78,09 %.
В небольшом количество соединения азота находится в почве; азот входит в состав аминокислот, образующих через посредство пептидных связей белки; содержится в молекулах нуклеиновых кислот – ДНК и РНК – в составе азотистых оснований (нуклеотидов): гуанина, аденила, тимидила, цитизила и уридила. Общее содержание азота в земной коре – 0,01 %.
Из минералов промышленное значение имеют чилийская селитра NaNO3 и индийская селитра KNO3.

Источник: http://himege.ru/azot-ximicheskie-svojstva/
Строение атома азота
Азот (N) – газ, содержание которого в атмосфере составляет около 78 %. Азот входит в состав аминокислот и нуклеотидов. Строение атома азота определяет физические и химические свойства элемента.

Азот – седьмой элемент периодической таблицы, расположенный в пятой группе и втором периоде. Относительная атомная масса равна 14. В природных условиях встречаются два изотопа азота – 14N и 15N.
Рис. 1. Азот в таблице Менделеева.
Азот состоит из ядра с зарядом +7 и семи электронов, распределённых по двум энергетическим уровням. Нахождение элемента в пятой группе указывает на количество электронов на внешнем уровне и высшую валентность. В невозбуждённом состоянии на внешнем энергетическом уровне находится три электрона, поэтому азот может проявлять две валентности – III и V.
Запись электронного строения атома азота – 1s22s22p3 или +7 N)2)5.
Азот – двухатомный (N2) газ без запаха и вкуса, плохо растворимый в воде. Азот может находиться в газообразном, жидком и твёрдом состояниях. В сжиженной форме азот имеет температуру кипения -196°С. При -209,86°C азот становится твёрдым. Под влиянием разных температур кристаллическая решётка твёрдого азота может изменяться, создавая модификации элемента.
Рис. 2. Жидкий и твёрдый азот.
Атомы азота соединены тройной связью (N ≡ N), что обеспечивает максимальную прочность. Даже при нагревании азота до 3000°C наблюдается незначительное разложение молекул (до 0,1 % от взятого количества газа). Именно поэтому азот – химически малоактивный элемент. В соединениях при нагревании азот легко расстаётся с другими элементами.
Основные химические свойства азота приведены в таблице.
| Взаимодействие | Продукт реакции | Пример |
| С металлами (реагирует с сильными восстановителями) | Соль | 6Li + N2 → 2Li3N |
| Окисление под действием электрического тока | Оксид азота | O2 + N2 → 2NO |
| С водородом в присутствии катализатора (Fe), под действием температуры (400 °С) и давления (200 атм) | Аммиак | 3H2 + N2 → 2NH3 |
| С неметаллами при высоких температурах | Соль | 2B + N2 → 2BN |
Соединения азота с металлами и неметаллами называются нитридами.
Азот не реагирует с кислотами, водой и основаниями. Невозможно непосредственное взаимодействие молекул азота с серой и галогенами. Более активно с этими веществами при нормальных условиях реагирует атомарный азот.
Несмотря на пассивность азота, элемент широко применяется в промышленности. Кроме того, азот входит в состав клеток, без него невозможно построение белка и ДНК.
Рис. 3. Азот в составе ДНК.
Азот используется при производстве:
- удобрений;
- взрывчатых веществ;
- медикаментов;
- красителей;
- пластмассы;
- искусственных волокон;
- аммиака.
Жидкий азот используется для охлаждения, заморозки, а также для окисления двигателей ракет. Оксид азота применяется в качестве наркоза и для производства аэрозолей.
Рассмотрели схему строения азота, его физические, химические свойства, применение. Азот состоит из положительно заряженного ядра и двух электронных оболочек, на которых находится семь электронов. Азот – малоактивный газ.
Молекула азота состоит из двух атомов элемента, соединённых тройной связью. Азот может находиться в трёх агрегатных состояниях. Элемент реагирует с некоторыми металлами, неметаллами и кислородом. Азот используется в промышленности, медицине, сельском хозяйстве.
Кроме того, азот входит в состав живых организмов.
Средняя оценка: 4.7. Всего получено оценок: 267.
Источник: https://obrazovaka.ru/himiya/stroenie-atoma-azota.html
Азот — урок. Химия, 8–9 класс
Азот — химический элемент № (7). Он расположен в VА группе Периодической системы химических элементов.
N7+7)2e)5e
На внешнем слое атома азота содержатся пять валентных электронов, до его завершения не хватает трёх электронов. Поэтому в соединениях с металлами и водородом азоту характерна степень окисления (–3), а при взаимодействии с более электроотрицательными кислородом и фтором он проявляет положительные степени окисления от (+1) до (+5).
Азот в виде простого вещества содержится в воздухе. Его объёмная доля составляет (78) %. В земной коре соединения азота встречаются редко. Известно месторождение нитрата натрия NaNO3 (чилийская селитра).
Азот относится к жизненно важным элементам, так как входит в состав молекул белков и нуклеиновых кислот.
Молекулы простого вещества состоят из двух атомов, связанных прочной тройной связью:
N:::N…., N≡N.
- При обычных условиях азот — бесцветный газ без запаха и вкуса, малорастворимый в воде.
- Не ядовит.
- Азот химически малоактивен из-за прочной тройной связи и в химические реакции вступает только при высоких температурах.
- При комнатной температуре он реагирует только с литием с образованием нитрида лития:
- 6Li0+N20=2Li+13N−3.
- При нагревании образует нитриды и с некоторыми другими металлами:
- 3Ca+N2=tCa3N2.
- С водородом азот реагирует только при высоком давлении, повышенной температуре и в присутствии катализатора. В реакции образуется аммиак:
- N20+3H20⇄t,p,k2N−3H3+1.
- В реакциях с металлами и водородом азот проявляет окислительные свойства.
- Восстановительные свойства азота проявляются в реакции с кислородом:
- N20+O20⇄t2N+2O−2.
Реакция возможна только при очень высокой температуре ((3000) °С) и частично протекает в атмосфере во время грозы. Образуется оксид азота((II)).
Большое количество азота используется для получения аммиака и азотных удобрений.
Применяется он для создания инертной среды при проведении химических реакций. Жидкий азот находит применение в медицине, используется для охлаждения в химических и физических исследованиях.
Чистый азот получают из воздуха.
Источник: https://www.yaklass.ru/p/himija/89-klass/khimiia-nemetallov-157456/azot-i-ego-soedineniia-161796/re-c79e2cf3-4588-479f-88f0-348ec0688712




