![]()
![]()
![]()
![]()
- Нитрат кальция – неорганическое вещество, имеет химическую формулу Ca(NO3)2.
- Краткая характеристика нитрата кальция
- Физические свойства нитрата кальция
- Получение нитрата кальция
- Химические свойства нитрата кальция
- Химические реакции нитрата кальция
- Применение и использование нитрата кальция
Краткая характеристика нитрата кальция:
- Нитрат кальция – неорганическое вещество белого цвета.
- Химическая формула нитрата кальция Ca(NO3)2.
- Нитрат кальция – неорганическое химическое соединение, соль азотной кислоты и кальция.
- Хорошо растворяется в воде, жидком аммиаке, ацетоне, метаноле, этаноле, пропаноле, жидком аммиаке.
- Обладает высокой гигроскопичностью, поэтому его хранят без доступа влаги.
- С водой нитрат кальция образует кристаллогидрат – тетрагидрат Ca(NO3)2·4H2O.
- Негорюч, пожаро- и взрывобезопасен.
Физические свойства нитрата кальция:
| Наименование параметра: | Значение: |
| Химическая формула | Ca(NO3)2 |
| Синонимы и названия иностранном языке | calcium nitrate (англ.) кальций азотнокислый (рус.) кальциевая селитра (рус.) |
| Тип вещества | неорганическое |
| Внешний вид | бесцветные кубические кристаллы |
| Цвет | белый, бесцветный, светло-серый, светло-бежевый |
| Вкус | —* |
| Запах | — |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество |
| Плотность (состояние вещества – твердое вещество, при 20 °C), кг/м3 | 2504 |
| Плотность (состояние вещества – твердое вещество, при 20 °C), г/см3 | 2,504 |
| Температура разложения, °C | 561 |
| Температура плавления, °C | 561 |
| Молярная масса, г/моль | 164,088 |
| Гигроскопичность | сильно гигроскопичен |
| Растворимость в воде (20 oС), г/100 г | 128,8 |
* Примечание:
— нет данных.
Получение нитрата кальция:
Нитрат кальция получают в результате следующих химических реакций:
- 1. взаимодействия хлорида кальция и нитрата серебра:
CaCl2 + 2AgNO3 → Ca(NO3)2 + 2AgCl.
- 2. взаимодействия гидроксида кальция и азотной кислоты:
Ca(OH)2 + 2HNO3 → Ca(NO3)2 + 2H2O.
- 3. взаимодействия оксида кальция и азотной кислоты:
CaO + 2HNO3 → Ca(NO3)2 + H2O.
- 4. взаимодействия оксида кальция и тетраоксида диазота:
CaO + 2N2O4 → Ca(NO3)2 + N2O3.
Реакция протекает в жидком тетраоксиде диазота.
- 5. взаимодействия оксида кальция, оксида азота (IV) и кислорода:
2Ca(OH)2 + 4NO2 + O2 → 2Ca(NO3)2 + 2H2O.
В ходе реакции гидроксид кальция используется в виде суспензии. Реакция представляет собой поглощение оксида азота (IV) известковым молоком.
- 6. взаимодействия сульфита кальция и азотной кислоты:
CaSO3 + 2HNO3 → Ca(NO3)2 + SO2 + H2O.
Химические свойства нитрата кальция. Химические реакции нитрата кальция:
- Химические свойства нитрата кальция аналогичны свойствам нитратов других металлов. Поэтому для него характерны следующие химические реакции:
- 1. реакция взаимодействия нитрата кальция и атомарного водорода:
- Ca(NO3)2 + 2H2 → Ca(NO2)2 + 2H2O.
- В результате реакции образуются нитрит кальция и вода.
- 2. реакция взаимодействия нитрата кальция и кислорода:
- 2Ca(NO3)2 + O2 → 2CaO + 4NO2.
- В результате реакции образуются оксид кальция и оксид азота (IV).
- 3. реакция взаимодействия нитрата кальция и гидроксида натрия:
- Ca(NO3)2 + 2NaOH → Ca(OH)2 + 2NaNO3.
В результате реакции образуются нитрат натрия и гидроксид кальция. В ходе реакции используется концентрированный раствор гидроксида натрия.
- 4. реакция взаимодействия нитрата кальция и сульфата меди:
- Ca(NO3)2 + CuSO4 → CaSO4 + Cu(NO3)2.
- В результате реакции образуются сульфат кальция и нитрат меди.
- 5. реакция взаимодействия нитрата кальция и молибдата натрия:
- Na2MoO4 + Ca(NO3)2 → CaMoO4 + 2NaNO3.
- В результате реакции образуются молибдат кальция и нитрат натрия.
- реакция взаимодействия нитрата кальция и гидроортофосфата натрия:
- 3Ca(NO3)2 + 2Na2HPO4 → Ca3(PO4)2 + 4NaNO3 + 2HNO3 (t°).
В результате реакции образуются фосфат кальция, нитрат натрия и азотная кислота. Реакция протекает при кипении.
- реакция взаимодействия нитрата кальция и вольфрамата натрия:
- Na2WO4 + Ca(NO3)2 → CaWO4 + 2NaNO3.
- В результате реакции образуются вольфрамат кальция и нитрат натрия.
- реакция термического разложения нитрата кальция:
- Ca(NO3)2 → Ca(NO2)2 + O2 (t = 450-500°C),
- 2Ca(NO3)2 → 2CaO + 4NO2 + O2 (t > 600°C).
- В результате реакции образуются в первом случае – нитрит кальция и кислород, во втором – оксид кальция, оксид азота (IV) и вода.
- реакция термического разложения тетрагидрата нитрата кальция:
- Ca(NO3)2•4H2O → Ca(NO3)2 + 4H2O (t = 60-170 °C).
- В результате реакции образуются нитрат натрия и вода.
Применение и использование нитрата кальция:
- Нитрат кальция используется во множестве отраслей промышленности и для бытовых нужд:
- – в сельском хозяйстве в качестве азотного удобрения. Наиболее эффективен на кислых почвах;
- – в строительстве как добавка в бетон;
- – в производстве стеклопластиков.
Примечание: © Фото https://www.pexels.com, https://pixabay.com
-




- карта сайта
- нитрат кальция реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие нитрата кальция
реакции
Источник: https://xn--80aaafltebbc3auk2aepkhr3ewjpa.xn--p1ai/nitrat-kaltsiya-harakteristika-svoystva-i-poluchenie-himicheskie-reaktsii/
Селитра кальциевая как удобрение: формула, применение нитрата кальция на огороде для рассады, помидоров
Для нормального развития растениям нужны минеральные удобрения. Питательные вещества влияют на формирование зеленой массы и корневой системы, защищают от вредителей и болезней. Чтобы применение кальциевой селитры в огороде, саду не навредило, надо знать правила ее использования.
Состав и формула селитры кальциевой
Щелочной препарат быстро растворяется в воде. Средство имеет химическую формулу: Ca (NO3)2. В состав селитры кальциевой входят (в %):
- кальций – 19;
- азот – от 13 до 16.
Азотнокислый кальций почти не закисляет грунт, поэтому показывает отличные результаты на дерново-подзолистых участках. Активные вещества нейтрализуют кислоту, вытягивают из верхнего слоя лишние компоненты (железо, марганец). Нитратное удобрение качественно работает на любых почвах и во всех климатических условиях. Подкормка поддерживает растения в засушливых зонах.
Разновидности препарата
Нитрат кальция выпускают в 2 формах: в виде белых гранул и полупрозрачной кристаллической соли. Популярное средство производят разные заводы. Бренд «Фертика» ориентирован на средние и крупные фермерские хозяйства, упаковывает продукцию в килограммовые мешки. Торговая марка «Буйские удобрения» предлагает три вида фасовки:
Производители указывают гарантийный срок годности – 2 года. Гранулы практически не впитывают влаги. Химикат в упаковке не слеживается, со временем не теряет первоначальных характеристик. Кристаллы расплываются, сыреют, поэтому их надо держать только в фирменном запаянном мешке или в сухом помещении.

Полезные свойства для растений
Селитра или кальций азотнокислый увеличивает урожайность на 15% у многих огородных и плодовых культур. При правильной дозировке вещества не накапливаются, не трансформируются в опасные соединения. Минеральное удобрение положительно воздействует на растения:
- Повышается иммунитет: укрепляет клеточные мембраны, улучшает устойчивость к температурным перепадам, болезням и вредителям. Корневые, верхушечные гнили меньше поражают томаты и перец, а кила – капусту, редьку.
- Ускоряется фотосинтез. Вещество способствует развитию и росту корней, листвы.
- Стимулирует пробуждение: обработанные семена, клубни и луковицы быстрее проклевываются.
- Улучшает качество грунта. Нейтрализует кислотность в почве, поглощает металлы, не допускает образования опасных химических соединений.
- Позитивно влияет на товарные характеристики. В результате применения агросредства увеличивается сахаристость овощей, плодов, их вкус меняется в положительную сторону. Урожай быстрее созревает, продлевается лежкость продукции.
Дефицит кальция негативно отражается на способности растений поглощать питательные компоненты и воду. Сбалансированный состав быстро поступает в грунт, обогащает почву важными элементами. Подкормка кальциевой селитрой оживляет корни, способствует здоровой вегетации и не допускает опасных трансформаций.
Преимущества и недостатки препарата
Растения плохо усваивают азот в земле с кислой реакцией. Мочевина и аммиачная селитра увеличивают кислотность участка.
Азотнокислый кальций, наоборот, способствует ощелачиванию почвы и обладает комплексным воздействием, поэтому преимущества использования заметны через 2-3 недели.
В грунте активно развиваются полезные бактерии, которые улучшают его структуру. Средство нейтрализует поступление вредных солей, металлов в ткани посадок.
Превышение дозировки препарата или неправильно выбранные сроки обработки опасны негативными реакциями. Избыток удобрения разрушает корни, ботву. Подземные части перестают поглощать воду, питательные компоненты. Поступающая жидкость провоцирует появление гнилей.
Особенности использования на приусадебном участке
Применение удобрения нитрат кальция важно осуществлять по правилам. Средство не является универсальным, существуют ограничения по срокам внесений и требования к грунту. Если придерживаться инструкции, то легко избежать ошибок.
Потребность различных культур в подкормках
Не все растения одинаково положительно отзываются на внесения кальциевой селитры. Запрещена подкормка видам, развивающимся в кислом грунте:
- болотным ягодам (бруснике, голубике, клюкве);
- хвойникам;
- вереску;
- азалии;
- папоротникам;
- гортензии.

Культуры, предпочитающие слегка подкисленный грунт, могут погибнуть от нитрата кальция. Регулярное удобрение противопоказано:
- ромашке;
- декоративному клену;
- акации;
- барбарису;
- жимолости;
- калине.
В садоводстве отзывчивы к внесениям плодовые косточковые деревья, виноград и яблоня. Чтобы клубника, земляника не мельчали, надо подкармливать их азотнокислым кальцием. Гладиолусы и весенние луковичные виды любят популярное удобрение. Обильным цветением порадуют:
- клематисы;
- флоксы;
- георгины;
- лилии.
Подкормка обязательна всем тыквенным и пасленовым культурам.
Сбалансированный состав положительно влияет на формирование головок у капусты, стручков у бобовых. На удобренном огороде пряные травы, лук и чеснок развиваются быстрее, чем на обычном участке.
Азотные удобрения: основные виды и правила использования
Применение на разных типах почв
Лучшие результаты азотнокислый кальций показывает на дерново-подзолистых, слабокислых, кислых почвах. Повышается питательность и рыхлость земли, погибают болезнетворные бактерии, грибки. Тяжелый глинистый грунт и легкие супесчаники удобряют слабо концентрированным раствором. Противопоказан препарат на участках со щелочной реакцией.
Сроки внесения
Селитру кальцинированную используют весной при перекапывании грядок или вспашке участка. Если вносить средство осенью, то удобрение не принесет пользы: азот вымывается из земли с грунтовыми водами, остается только кальций. Из-за высокой концентрации химикат накапливается в растениях, уничтожая их подземные части.
Способы подкормок
Корневые внесения – это простой метод использования удобрений, который дает пролонгированный результат. Питательные вещества попадают в грунт, потом разлагаются в доступную для растений форму. Средство разводят в жидкости, поливают прикорневой круг культур. Гранулы высыпают в грунт во время перекопки, добавляют в лунки при посадке саженцев, рассады.

Если нужно быстрое действие, то прибегают к опрыскиванию слабым раствором по листу из пульверизатора. На 10 л воды понадобится 25 г азотнокислого кальция, расход жидкости на квадратный метр – 200 мл.
Зеленая масса быстро поглощает компоненты, не позволяя разрушаться или смываться с грунтовыми водами во время дождя. Внекорневые подкормки повышают сахаристость ягод винограда, плодов сливы и яблок.
Инструкция по применению
Чтобы нитрат кальция принес пользу, надо правильно развести гранулы. Нормы зависят от вида и возраста растений. Данное удобрение, применяемое согласно инструкции, защитит растения от болезней, позаботится об их иммунитете.
Чтобы не обжечь корни, надо перед процедурой обязательно полить грядку.
Для рассады
Азот и кальций помогают получить крепкую, здоровую рассаду. Первое внесение выполняют после формирования третьего взрослого листа, второе – спустя 10 дней после пикирования. Аккуратно орошают под корень, стараясь не попасть на ботву. На 5 л воды берут (в г):
- селитры кальциевой – 10;
- мочевины – 5;
- золы древесной – 50.
Для огурцов
У огурцов медленно развиваются подземные части, поэтому надо аккуратно проводить внесения. После появления трех взрослых листов опрыскивают рассаду нитратом кальция. Корневые подкормки повторяют до завязывания плодов каждые 8 дней. Чтобы не ошибиться с дозой, надо в 1 л воды развести 2 г средства.
Свойства и специфика применения удобрения «Виндзор»
Для томатов и перцев
Пасленовые овощные культуры любят удобрение. Внекорневое применение кальциевой селитры для томатов, перцев и картофеля оградит от слизней, клещей и черной гнили. Разовая обработка имеет пролонгированный характер и будет защищать насаждения до созревания плодов.
Помидоры и перцы можно подкормить и корневым способом. В ведре воды растворяют 20 г азотнокислого кальция. Первую процедуру проводят через 7 дней после высадки в открытый грунт. Повторяют каждую неделю до появления цветов.
Для капусты
Рассада любит селитру кальциевую, а зрелым экземплярам она противопоказана. В лунку перед высадкой добавляют 1 чайную ложку гранул, присыпают грунтом и сажают кустик. Нитрат кальция защитит молодые растения от болезней, вредителей и закручивания, улучшит рост.
Для клубники и малины
Землянику садовую подкармливают до начала цветения. Ягодные кусты кормят до распускания почек. В 10 л жидкости растворяют 30 г препарата, которым обильно поливают участок с посадками.
Для цветов
Если использовать для цветов кальциевую селитру, то можно защитить растения от гниения, улучшить формирование зелени. Корневые внесения проводят с начала сезона каждые 10 дней. Если бутоны мельчают, то прикорневую обработку чередуют с опрыскиванием по листу. На ведро воды используют 2 г кристаллической соли.
Совместимость с другими препаратами
Одновременно с туком можно применять измельченную древесную золу и карбамид. Противопоказаны все органические удобрения, опилки и солома. Запрещено смешивать кальциевую селитру с:
- известью;
- мелом;
- стимуляторами;
- химикатами на основе фосфора, серы.
Кальциевая селитра своими руками
Если удобрения нет под рукой, можно приготовить препарат в домашних условиях. На свежем воздухе сооружают конструкцию из кирпичей, разводят пламя. В алюминиевой кастрюле соединяют:
- воду — 500 мл;
- гашеную известь – 140 г;
- селитру аммиачную – 300 г.
Смесь греют до тех пор, пока не пропадет специфичный нашатырный запах. Огонь тушат, оставляют средство остывать. Для внесений используют чистую верхнюю жидкость, а темный нижний слой удаляют.
Минеральные подкормки помогают огородникам и садоводам вырастить обильный урожай, получить красивые цветы. Понимая, когда и для чего применяется кальциевая селитра, можно не переживать о том, подойдет подкормка конкретной культуре или нет. Если использовать высокую концентрацию, то раствор разрушит защитное покрытие корней, листвы.
Источник: https://SuperUrozhay.ru/mineralnye-udobreniya/kak-pravilno-primenyat-kalcievuyu-selitru.html
Структура нитрата кальция (Ca (NO3) 2), свойства, применение и применение / химия
нитрат кальция третичная неорганическая соль, химическая формула которой Ca (NO)3)2. Из его формулы известно, что его твердое вещество состоит из ионов Ca2+ и НЕТ3- в соотношении 1: 2. Следовательно, это соединение чисто ионной природы.
Одним из его свойств является его окислительный характер благодаря нитрат-аниону. Он не горючий, то есть не горит при высоких температурах. Будучи негорючим, он представляет собой надежный сейф, с которым можно обращаться без особой осторожности; однако, это может ускорить воспламенение горючих материалов..

Его внешний вид состоит из гранулированного твердого вещества, которое имеет белый или светло-серый цвет (верхнее изображение). Может быть безводным или тетрагидратированным, Ca (NO3)2· 4H2О. Он очень растворим в воде, метаноле и ацетоне.
Нитрат кальция широко используется в качестве удобрения, поскольку он легко перемещается во влажной почве и быстро усваивается корнями растений. Он обеспечивает два важных элемента для питания и роста растений: азот и кальций.
Азот является одним из трех важнейших элементов для развития растений (N, P и K), имеет важное значение в синтезе белков. Между тем, кальций необходим для поддержания структуры клеточной стенки растений. По этой причине Ca (НЕТ3)2 это предназначено много в сады.
С другой стороны, эта соль обладает токсическим действием, особенно при непосредственном контакте с кожей и глазами, а также при вдыхании ее пыли. Кроме того, он может разлагаться при нагревании.
индекс
- 1 Структура нитрата кальция
- 2 Физические и химические свойства
- 2.1 Химические названия
- 2.2 Молекулярная формула
- 2.3 Молекулярный вес
- 2.4 Внешний вид
- 2.5 Точка кипения
- 2.6 Точка плавления
- 2.7 Растворимость в воде
- 2.8 Растворимость в органических растворителях
- 2.9 Кислотность (пКа)
- 2.10 Плотность
- 2.11 Разложение
- 2.12 Реактивный профиль
- 3 использования
- 3.1 Сельское хозяйство
- 3.2 Бетон
- 3.3 Очистка сточных вод или сточных вод
- 3.4 Приготовление холодных компрессов
- 3.5 Латексная коагуляция
- 3.6 Передача и хранение тепла
- 4 анкеты
- 5 ссылок
Структура нитрата кальция
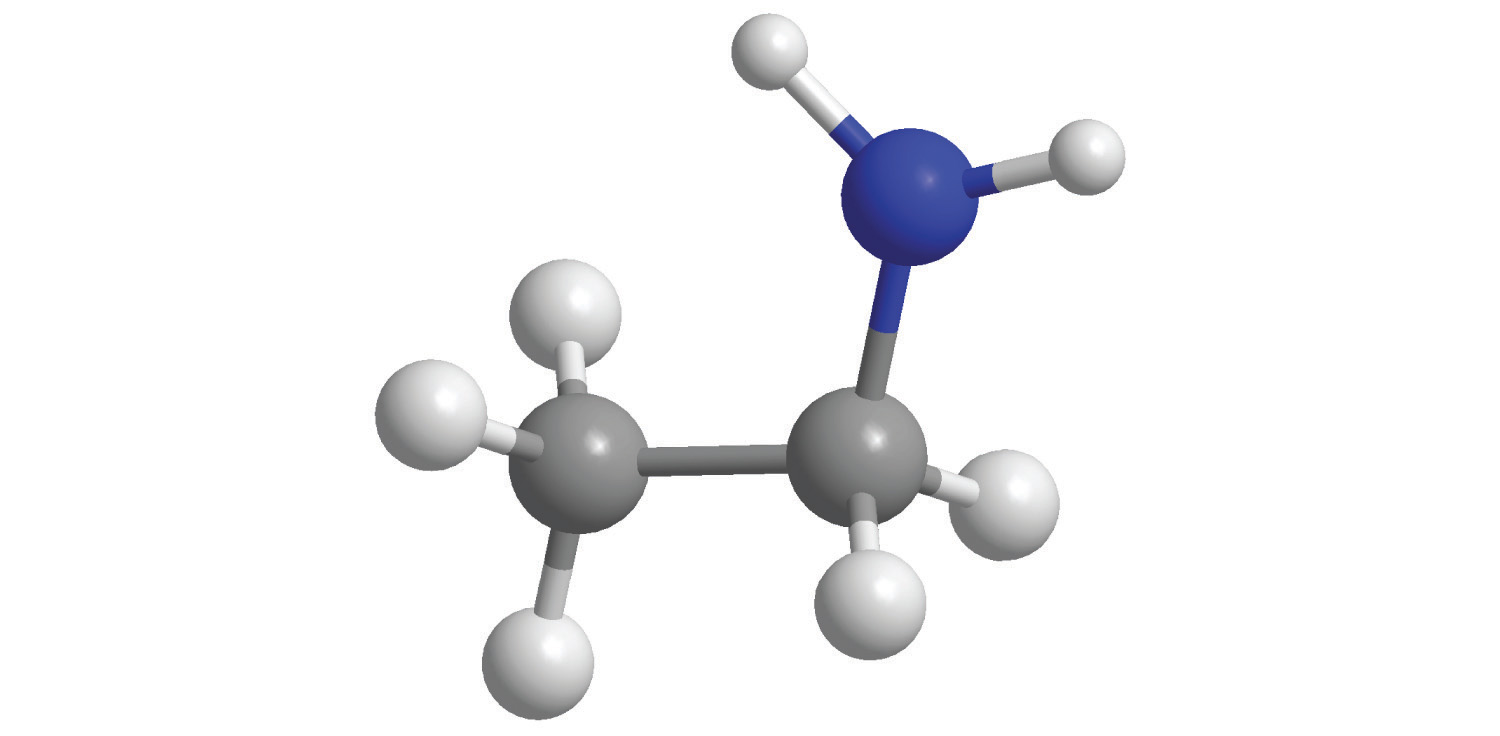
Структура Ca (NO) показана на изображении выше3)2 в модели сфер и баров. Здесь, однако, есть недостаток: предполагается существование ковалентных связей Ca-O, что противоречит его ионному характеру. Разъяснение этого, действительно взаимодействия имеют электростатический тип.
Катион Са2+ окружен двумя NO анионов3- в соответствии с его пропорциями в кристалле. Азот в форме нитрата преобладает в кристаллической структуре.
Ионы сгруппированы таким образом, что они устанавливают конфигурацию, минимальным выражением которой является элементарная ячейка; который для безводной соли является кубическим. Другими словами, из кубов, содержащих для этих ионов соотношение 1: 2, кристалл воспроизводится полностью.
С другой стороны, тетрагидратированная соль Ca (NO)3)2· 4H2Или это имеет четыре молекулы воды на комплект NO3- Калифорния2+ НЕТ3-. Это изменяет кристаллическую структуру, превращая ее в моноклинную элементарную ячейку.
Следовательно, ожидается, что кристаллы для обеих солей, безводной и тетрагидратированной, будут разными; различия, которые можно определить по их физическим свойствам, например, по точкам плавления.
Физико-химические свойства
Химические названия
- -Нитрат кальция
- -Динитрат кальция
- -Nitrocalcita
- -Норвежская селитра и известь сальпетро.
Молекулярная формула
Ca (НЕТ3)2 или CaN2О6
Молекулярный вес
Безводный 164,088 г / моль и тетрагидрат 236,15 г / моль. Обратите внимание на влияние воды на молекулярную массу, и им нельзя пренебрегать при соответствующем взвешивании..
Внешний вид
Твердые или гранулы белого или светло-серого цвета. Кубические белые кристаллы или распущенные гранулы; то есть они впитывают влагу до такой степени, что они растворяются из-за их высокой растворимости.
Точка кипения
Безводная форма разлагается при нагревании до температуры, которая не позволяет определить ее температуру кипения; в то время как тетрагидратированная форма соли имеет температуру кипения 132 ° С (270 ° F, 405 К).
Точка плавления
-Безводная форма: от 561 ºC до 760 мм рт. Ст. (1042 ºF, 834 K).
-Тетрагидратированная форма: 42,7 ºC (109 ºF, 316 K).
Это показывает, как молекулы воды вмешиваются в электростатические взаимодействия между Са2+ и НЕТ3- внутри кристаллов; и, следовательно, твердое вещество плавится при значительно более низкой температуре.
Растворимость в воде
- -Безводная форма: 1212 г / л при 20 ºC.
- -Тетрагидратированная форма: 1290 г / л при 20 ºC.
- Вода в кристаллах едва увеличивает растворимость соли.
Растворимость в органических растворителях
- -В этаноле, 51,42 г / 100 г при 20 ºC.
- -В метаноле 134 г / 100 г при 10 ºC.
- -В ацетоне, 168 г / 100 г при 20 ºC.
Кислотность (пКа)
6,0
плотность
2,5 г / см3 при 25 ° С (тетрагидрат).
разложение
Когда нитрат кальция нагревается до ламп накаливания, он разлагается на оксид кальция, оксид азота и кислород.
Реактивный профиль
Это сильно окисляющий агент, но он не горючий. Ускоряет воспламенение горючих материалов. Разделение нитрата кальция на мелкие частицы облегчает его взрыв, когда соединение подвергается длительному воздействию огня..
Смеси с алкиловыми эфирами становятся взрывоопасными при образовании алкилнитратных сложных эфиров. Комбинация нитрата кальция с фосфором, хлоридом олова (II) или другим восстановителем может реагировать взрывоопасно.
приложений
сельское хозяйство
Он используется в сельскохозяйственных культурах в качестве источника азота и кальция. Нитрат кальция очень хорошо растворяется в воде и легко усваивается корнями растений. Кроме того, он не окисляет почвы, потому что их ионы не могут значительно гидролизовать.
Избегайте смешивания с удобрениями, содержащими фосфор или сульфат, чтобы избежать образования нерастворимых солей. Вследствие своей гигроскопичности его следует хранить в сухом и прохладном месте..
Его использование имеет преимущество перед использованием аммиачной селитры в качестве удобрения. Хотя это последнее соединение вносит азот в растения, оно препятствует усвоению кальция, что может привести к дефициту кальция в растениях..
Кальций способствует поддержанию структуры клеточной стенки растений. При наличии дефицита кальция ткани, образующие растения, такие как кончики корней, молодые листья и кончики почек, часто демонстрируют искаженный рост..
Снижение содержания аммония
Нитрат кальция уменьшает накопление летучих жирных кислот и фенольных, фитотоксичных соединений, которые накапливаются вследствие разложения остатков соевых культур.
Кроме того, нитрат кальция имеет тенденцию к снижению концентрации аммония в почве, что увеличивает буферную емкость водорода.
бетон
Нитрат кальция используется для сокращения времени схватывания бетона. Это происходит в результате образования гидроксида кальция, возможно, в результате реакции двойного вытеснения..
Кроме того, нитрат кальция вызывает образование соединения гидроксида железа, защитное действие которого снижает его коррозию. То есть присутствующее железо может реагировать с основными компонентами бетона, такими как сам гидроксид кальция.
Нитрат кальция уменьшает время схватывания, а также прочность бетона, к которому был добавлен вулканический пепел. Для изучения влияния добавления нитрата кальция к бетону были использованы возрастающие концентрации нитрата кальция, от 2% до 10%..
Наблюдается большее уменьшение времени схватывания, а также увеличение прочности бетона, так как концентрация нитрата кальция увеличилась до 10%..
Сточные воды или очистка сточных вод
Нитрат кальция используется для уменьшения неприятных запахов из сточных вод за счет уменьшения образования сероводорода. Кроме того, органическое вещество, которое генерирует анаэробные условия, потребляется, что препятствует выживанию многих биологических видов..
Приготовление холодных компрессов
Тетрагидрат нитрата кальция является эндотермическим соединением, то есть обладает способностью поглощать тепло из окружающей среды. Это приводит к охлаждению тел, которые входят в контакт с контейнерами, которые его содержат.
Компрессы повышают их температуру, и для их регенерации достаточно поместить их в морозильник
Латексная коагуляция
Нитрат кальция используется в фазе коагуляции латекса. Он является частью иммерсионного раствора, и когда он вступает в контакт с раствором, содержащим латекс, он нарушает его стабилизацию и вызывает его коагуляцию.
Передача и хранение тепла
Бинарная смесь солей расплавленных нитратов, включая кальций с другими нитратами, используется вместо термального масла на солнечных электростанциях для передачи и хранения тепла..
Анкеты
-Применяется нитрат кальция в смеси с почвой в концентрации 1,59 кг на 30,48 м.2, с адекватным поливом. Нитрат кальция растворяется в воде, что позволяет его усвоению корнями растения. В гидропонных культурах растворяется в воде культуры.
-Нитрат кальция также используется в виде спрея для опрыскивания листьев и цветов, что является эффективным средством для предотвращения гниения цветка томата, пятна от пробки и горькой косточки яблока..
-К бетонообразующей смеси добавляется некоторое количество нитрата кальция (цемент, песок, камни и вода), и определяется влияние его добавления на конкретные свойства бетона; такие как установка скорости и сопротивления.
-Нитрат кальция добавляется в подходящей концентрации, чтобы уменьшить запахи из сточных вод или сточных вод до уровня, чтобы запахи были приемлемыми для людей.
ссылки
- Бонни Л. Грант. (2019). Удобрение нитрата кальция — что делает нитрат кальция для растений. Получено от: gardeningknowhow.com
- Farquharson, B.F., Vroney, R.P., Beauchamp, E.G. и Вин, Т.Дж. (1990). Использование нитрата кальция для снижения накопления фитотоксинов при разложении остатков в корп. Канадский журнал почвоведения 70 (4): 723-726.
- Огунбоде, Е. Б. и Хасан, И.О. (2011). Влияние добавления нитрата кальция на селективные свойства бетона, содержащего вулканический пепел. Леонардо Электронный журнал практик технологий 19: 29-38.
- Wikipedia. (2019). Нитрат кальция. Получено с: en.wikipedia.org
- Shiqi Dong & col. (2018). Ингибирование коррозии стали нитратом кальция в обогащенных галогенидами средах для заканчивания. npj Материалы для разложения тома 2, номер артикула: 32.
- Emaginationz Technologies. (2019). Спецификации нитрата кальция. Получено с: direct2farmer.com
- PubChem. (2019). Нитрат кальция. Получено из: pubchem.ncbi.nlm.nih.gov
Источник: https://ru.thpanorama.com/articles/qumica/nitrato-de-calcio-cano32-estructura-propiedades-usos-y-aplicaciones.html
Селитра кальциевая | справочник Пестициды.ru
Кальциевая селитра (безводная соль) – бесцветные кристаллы с кубической решеткой.
Физические характеристики
- Плотность – 2,36 г/см3.[5]
- Безводная соль плавится при температуре 561°C. При температуре 500°C начинается разложение с выделением O2 и образованием нитрита кальция Ca(NO2)2, который затем распадается на CaOи NO2.[4]
- При температуре до 42,7°C кристаллизуется четырехводный кристаллогидрат, выше 54,6°C – безводный нитрат кальция.
- Растворимость в воде:
- при 20°C – 56,3 %,
- при 51,6 °C – 78,2 %.[3]
- Как безводная соль, так и кристаллогидраты нитрата кальция сильно гигроскопичны и расплываются на воздухе.
- Давление пара над 50%-ным раствором азотнокислого кальция в диапазоне температур от 70 до 110°C возрастает от 135 до 730 мм рт. ст, а над 75%-ным раствором в диапазоне 90–140°C возрастает от 90 до 740 мм рт. ст.
- Раствор концентрацией 77,9 % Ca(NO3)2 кипит при 143,3 °C под нормальным давлением и при 117°C под давлением 300 мм рт. ст.
[4]
| Физико-химические свойства кальциевой селитры, согласно:[5][8] | ||||
| Наименование | Кальциевая селитра (безводная соль) | Кальцевая селитра гранулированная Марка «А» | Кальцевая селитра гранулированная Марка «Б» | Кальций азотнокислый 4-х водный |
| Внешний вид | бесцветные кристаллы | Гранулы полусферической формы белого цвета | Белые или прозрачные кристаллы. | |
| Плотность, г/см3 | 2,36 | — | — | — |
| Температура плавления, °C. | 561 | — | — | — |
| Растворимость %, при 20°C | 56,3 %, | — | — | — |
| Степень гигроскопичности | сильная | слабая | слабая | — |
| Массовая доля общего азота (N), %, не менее | 13 – 15 | 14,5 | 14,5 | 11,6 |
| Массовая доля кальция (CaO), %, не менее | — | 26,3 | 26,3 | 16,6 |
| Массовая доля азота нитратного (N-NO3), %, не менее | — | 13,8 | 13,8 | — |
| Массовая доля азота аммонийного (N-NH4), %, не менее | — | 0,7 | 0,7 | — |
| Массовая доля бора (B), %, не более | — | — | 0.3 | — |
| Показатель активности водородных ионов (pH) 1%-ного раствора, ед. | — | 0,1 | 0,1 | 6,0 – 6,5 |
| Массовая доля не растворимого в воде остатка. неболее.(%) | — | — | — | 0,1 |
Кальциевая селитра (безводная соль, гранулированная, четырехводная, жидкая и прочие формы) используется в качестве предпосевного удобрения и подкормок различных овощных, плодовых и декоративных культур.[4]
Строительство
Кальциевую селитру применяют как добавку в бетон для замедления процесса коррозии помещенной в бетон стали, в качестве ускорителя отвердения, а также для повышения прочности.[8]
Пищевая промышленность
Кальциевая селитра служит для приготовления рассола в холодильной технике.[8]
Химическая промышленность
Кальциевую селитру применяют при производстве различных реактивов. Она является одним из компонентов при производстве взрывчатых веществ.[8]
Кальциевая селитра – физиологически щелочное удобрение. Растения в большем количестве потребляют анионы NO3-, чем катионы Ca+. Последние, оставаясь в почве, сдвигают реакцию в сторону подщелачивания. (Изображение)
Катионы кальция быстро переходят в обменно-поглощенное состояние.
Анион NO3– образует с вытесненными из ППК комплексами азотную кислоту или различные растворимые соли. NO3-связывается в почве только путем биологического поглощения, что происходит исключительно в теплый период. Осенью и зимой биологическое поглощение отсутствует, и анион NO3– легко вымывается из почвы.[6]
Кальциевую селитру рекомендуется применять повсеместно на различных типах почв.
В результате применения кальциевой селитры кислотность нейтрализуется, реакция почвы сдвигается к нейтральной. Это особенно эффективно на кислых дерново-подзолистых почвах.[6]
Кальциевую селитру в форме безводной соли и кристаллогидратов нитрата кальция вносят в почву как в сухом виде, так и в качестве низкопроцентного раствора для некорневой, корневой подкормок, а также при фертигации в течение вегетационного периода. Концентрация раствора зависит от исходного состава и марки удобрения. При приготовлении раствора следует придерживаться рекомендаций производителя.
Кальциевая селитра гранулированная рекомендуется для корневых подкормок, некорневых подкормок и фертигации всех культур открытого и закрытого грунта как через системы капельного полива и дождевальные установки, так и для сухого внесения с использованием туковых сеялок и разбрасывателей. Некорневые подкормки проводят с применением опрыскивателей различной модификации.[7]
Кальциевая селитра является источником азота для растений в период вегетации. Применение данного удобрения способствует улучшению роста, сопротивляемости различным неблагоприятным факторам и повышению урожайности практически всех культурных растений.[6]
Хорошо использовать данное удобрение для подкормки озимых, пропашных и прочих культур.[1]
Кальциевую селитру получают:
- как побочный продукт при производстве азотной кислоты из аммиака путем насыщения известнякового молока нитрозными газами;
- при производстве комплексных удобрений по методу азотнокислого разложения фосфатного сырья.
- Уменьшение гигроскопичности достигается добавлением гидрофобных составляющих (гипса, парафинистого мазута).
- Физические свойства удобрения повышают, добавляя 4–7 % аммиачной селитры.
- Гранулированная кальциевая селитра получается путем добавления незначительного количества (4–7 %) нитрата аммония к предварительно упаренному раствору кальциевой селитры высокой концентрации с последующей грануляцией.[6]
Составитель: Григоровская П.И.
Страница внесена: 17.01.14 19:07
Источник: http://www.pesticidy.ru/active_compound/calcium_nitrate
ПОИСК
Кальциевая селитра хорошо растворяется в воде, причем ее растворимость мало зависит от повышения температуры. Так, например, при повышении температуры от 0° до 50° растворимость кальциевой селитры увеличивается примерно на 27%, а при дальнейшем повышении от 50 до 150°—всего на 3%. [c.
110]
Из последнего аппарата смесь маточного раствора и кристаллов подают на центрифугу непрерывного действия.
Отделенные от раствора кристаллы промывают охлажденной до минус 5—минус 10 °С азотной кислотой (для уменьшения растворимости кальциевой селитры), после чего промывную кислоту направляют в реакторы на разложение фосфата. [c.97]
Кальциевая селитра Са(МОз)2 — кальциевая соль азотной кислоты — бесцветные кристаллы, легко растворимые в воде и сильно гигроскопичные, содержит около 16% азота. Применяется для овощных, плодоягодных и цветочных культур. Средняя норма для внесения в почву весной 4—5 кг на 100 м2, для подкормки—15—20 г на 1 л воды. Расход раствора—1 л иа [c.98]
Кальциевая селитра хорошо растворима в воде (при 18°—129 г на 100 г воды) и. применяется как дешевое азотное удобрение. [c.329]
Еще с 1908 г. Д. Н. Прянишников начал заниматься переработкой отечественных фосфоритов на суперфосфат и преципитат. Он первый пробил брешь в распространенной тогда теории о непригодности этого сырья для получения полноценных растворимых фосфатов. Д.
Н. Прянишников уже тогда высказал предположение о целесообразности воздействия на фосфориты не серной, а азотной кислотой, полагая, что таким путем можно получить одновременно два ценных удобрения преципитат и кальциевую селитру. [c.
333]
Удаление кальциевой селитры из пульпы достигается и ее кристаллизацией при охлаждении. В оставшуюся массу [растворимые фосфаты и частично Са(КОз)г] прибавляют аммиак, серную кислоту, соль магния и хлористый калий.
Получают так называемую вымороженную нитрофоску, а выделенную кальциевую селитру гранулируют и применяют в качестве азотного удобрения.
При этом способе расход серной кислоты значительно меньше, чем для производства сернокислой нитрофоски, но возрастают затраты энергии на охлаждение пульпы при отделении нитрата кальция. В дальнейшем остаток приходится снова разогревать. [c.334]
Для извлечения окислов азота из газов, покидающих кислотные башни, вместо соды применяется также более дешевое известковое молоко. В этом случае получают кальциевую селитру. Известь, плохо растворимая в воде, может забивать насадку башни. Поглотительные башни заполняют хордовой насадкой. [c.363] Растворимость кальциевой селитры в воде очень велика, давление пара насыщенного раствора очень низкое. Поэтому нитрат кальция чрезвычайно гигроскопичен. Его физические свойства значительно улучшаются при добавлении нитрата аммония. К горячему концентрированному раствору нитрата кальция добавляют 5% концентрированного раствора нитрата аммония, что значительно увеличивает скорость кристаллизации. Смссь гранулируют, получают продукт с содержанием около 15,5% N. В слабокислый раствор нитрата кальция вводят также непосредственно аммиак. [c.195]
Нитратные удобрения. Растворимые в воде соли азотной кислоты NaNOa и a(N03)2 — натриевая и кальциевая селитры являются побочными продуктами производств азотной кислоты и сложных удобрений — нитрофосок.
Данные удобрения являются физиологически щелочными удобрениями. Растения в большем количестве потребляют анионы NOJ, чем катионы Na+ и Са +. Последние, оставаясь в почве, способствуют возникновению щелочной реакции среды.
При систематическом употреблении этих удобрений кислотность почв снижается. [c.695]
Нитрат кальция весьма гигроскопичен и хорошо растворяется в воде, табл. 11,23—11,29 приведены данные о гигроскопичности, растворимости в де нитрата кальция и других его свойствах. Прн производстве граиулиро-нион кальциевой селитры к ее рас- [c.201]
Нитрат кальция (известковая или кальциевая селитра) — бес-.щветное вещество, об разующее несколько кристаллогидратов (рис. 351). При обычной температуре из раствора кристаллизуется 1Стабильная а-форма тетрагидрата Са (ЫОз)г 4НгО. Растворимость [c.420]
Многие соединения кальция используют как минеральные удобрения, он входит в состав фосфоритной муки Саз(Р04)г, апатитового концентрата Саз(Р04)г СаГ2, суперфосфата Са(Н2Р04)2 + СаЗО , преципитата СаНР04 Н20, цианамида кальция СаСМг и кальциевой селитры Са(КОз)г.
Соединения кальция присутствуют в клетках всех животных 100 мл кровяной сыворотки содержат 9,2—11,3 мг Са. Фосфат и карбонат кальция входят в состав костей. Растворимый гидрокарбонат кальция находится в природных водах и сообщает им временную жесткость. [c.
132]
Разложение фосфатов азотной кислотой с вымораживанием кальциевой селитры. Выделение нитрата кальция из раствора основано по этой схеме на изменении растворимости Са(ЫОз)г в кислотном растворе.
Азотнокислотная вытяжка после отделения нерастворимого остатка поступает в кристаллизаторы, где раствор постепенно охлаждается до температуры минус 5—минус 10 °С. При этом выделяется осадок четырехводного нитрата кальция Са(ЫОз)2-4НгО.
Кристаллы кальциевой селитры отлагаются также на поверхности охлаждающих змеевиков, что значительно ухудшает условия теплопередачи, поэтому через каждые 2—3 ч в змеевики кристаллизаторов вводят пар.
При этом кристаллы плавятся на поверхности змеевиков в течение нескольких минут, благодаря чему быстро восстанавливается нормальный теплообмен. [c.593]
КАЛЬЦИЯ НИТРАТ (кальций азотнокислый, кальциевая селитра) — при обычных темп-рах выделяется в виде a(N0g)2 4HjO — бесцветных кристаллов, т. пл. 42,7°. Известны и другие кристаллогидраты К. н. Выше 51,6° кристаллизуется безводная соль— кристаллы кубич. системы, а = 7,62 А, плотность 2,36.
Безводная соль плавится при 561°, однако уже при 500° начинается ее разложение с потерей кислорода и образованием a(N02)2, к-рый далее распадается на СаО и NO. . Теплота образования безводной соли ДД°298 —224,0 ккал/моль. Растворимость в воде (г на 100 г НаО) 127 (20°), 355 (51,6°). Насыщенный р-р кипит при 151° и содержит 78,4% a(N03)2.
Криогидратная точка —28° [78,6 г a(N0g)2 на 100 г Н. О]. Как безводная соль, так и кристаллогидраты К. н. гигроскопичны, поэтому К. н. хранят без доступа влаги. Получают К. н. растворением известняка в азотной к-те или поглощением нитрозных газов известковым молоком.
Полученный р-р упаривают до концентрации a(N0g)2 73—82% и охлаждают, применяя в качестве затравки для кристаллизации немного азотнокислого аммония. Применяют К. н. как азотное удобрение. [c.190]
За рубежом независимо от средств, используемых для уменьшения слеживаемости соли, ее охлаждают перед упаковкой в тару.
В отечественной промышленности для уменьшения слеживаемости аммиачной селитры широко применяется добавление к соли продуктов азотнокислатпого разложения фосфатов или доломитов, а в некоторых случаях — растворов кальциевой селитры.
В присутствии таких добавок понижается растворимость нитрата аммония, следовательно, при охлаждении или подсушивании соли выпадает меньшее количество ее кристаллов из насыщенного раствора ЫН.Л Оз.
Добавки оказывают также влияние на температуру полиморфных превращений нитрата аммония, способствуют понижению давления паров насыщенного раствора ЫН ЫОз, изменению его вязкости и некоторых других физико-химических свойств нитрата аммония. Все эти сложные изменения приводят к уменьшению слеживаемости аммиачной селитры. [c.398]
Нитрат кальция (известковая или кальциевая селитра) образует несколько кристаллогидратов (рис. 103). При невысокой температуре из раствора кристаллизуется стабильная а-форма тетрагидрата a(N0s)a-4H20. Растворимость тетрагидрата характеризуется кривой АВС. Максимум на этой кривой в точке В соответствует плавлению тетрагидрата при 42,7 °С.
Линия А С — растворимость метастабильной -формы тетрагидрата. Кривая DE — растворимость Са(К0з)2-ЗН20 с максимумом в точке D при температуре плавления тригидрата 51,1 °С. Линия EF — растворимость метастабильного дигидрата Са(К0з)2-2Н20. Линия — растворимость безводной соли, почти не увеличивающаяся с повышением температуры.
Точка G соответствует температуре кипения насыщенного раствора (151 °С), содержащего 78,4% Са(К0з)2- Безводная соль плавится при 561 °С, однако уже при 500 °С начинается ее разложение с потерей кислорода и образованием нитрита кальция, который далее распадается на СаО и окислы азота.
Как безводная соль, так и кристаллогидраты нитрата кальция сильно гигроскопичны и на воздухе расплываются. [c.232]
Нитрат кальция (известковая или кальциевая селитра) образует несколько кристаллогидратов (рис. 76). При обычной температуре из раствора кристаллизуется стабильная а-форма тетрагидрата Са(ЫОз)г 4Н2О. Растворимость тетрагидрата характеризуется кривой АВС. [c.163]
Нитрат кальция относится к разряду хорошо растворимых солей. Он кристаллизуется в виде нескольких кристаллогидратов а- и Р-тетрагидратов Са(ЫОз)2-4Н2О, тригидрата Са(ЫОз)2 ЗН.2О и дигидрата Са(ЫОз)2-2Н2О.
При повышенных температурах азотнокислый кальций может переходить в твердую фазу в виде безводной соли. Как безводная соль, так и кристаллогидраты нитрата кальция гигроскопичны [1, 6].
Физические свойства кальциевой селитры предопределяют и особенности ее кристаллизации. [c.205]
Азотнокислый кальций (кальциевая селитра) известен не только в виде безводной соли, но и в виде нескольких кристаллогидратов a(N03)2 ЗН2О, Са(МОз)г 4Н2О и др. Несмотря на сравнительно низкое содержание азота (12,2—17,1% N) и высокую гигроскопичность, азотнокислый кальций в течение последних 20—30 лет широко, распространяется за рубежом в качестве удобрения.
Это объясняется тем, что азотнокислый кальций — быстродействующее удобрение, с которым, кроме того, вводится в растворимой форме полезная для многих почв известь. Путем смешения или сплавления азотнокислого кальция с другими солями гигроскопичность его может быть снижена. Применение азотнокислого кальция для промышленных целей незначительно. [c.
468]
В зависимости от метода связывания избыточного кальция классифицируют варианты получения нитрофосфатов.
По методу вымораживания четырехводной кальциевой селитры Са(Ы0д)2- 4Н2О выпавшие при охлаждении раствора кристаллы соли необходимо отделить, так как при нагревании они вновь растворятся и во время аммонизации будут взаимодействовать с фосфатами, снижая содержание не только водорастворимой, но и цитратно-растворимой Р2О5. [c.73]
Нитрат кальция (известковая или кальциевая селитра) — бесцветное вещество, образующее несколько кристаллогидратов (рис. 327). При обычной температуре из раствора кристаллизуется стабильная а-форма тетрагидрата Са(ЙОз)2 4НгО.
Растворимость тетрагидрата характеризуется кривой АВС. Максимум на этой кривой в точке В соответствует плавлению тетрагидрата при 42,7°. Линия А С — растворимость метастабильной р-формы тетрагидрата. Кривая СОЕ — рас [c.
802]
АММИАЧНЫЕ УДОБРЕНИЯ. Азотные удобрения, содержащие азот в аммиачной (аммонийной) форме. К ним относятся нитрат аммония, сульфат аммония, хлористый аммоний, карбонат и бикарбонат аммония, аммиак жидкий, аммиачная вода, сульфид аммония, а также фосфорно-азотные удобрения — аммофос и диаммофос, азотно-калийные удобрения — потазот.
В таких удобрениях, как аммиачная или кальциево-аммиачная селитра, сульфонит-рат аммония, половина содержащегося в них азота представлена аммиачной, а половина нитратной формой. Мочевина, содержащая азот в амидной форме, очень быстро, в течение 2—3 дней, превращается в почве в карбонат аммония, т. е. в аммиачную форму азота.
Все аммиачные удобрения хорошо растворимы в воде, и их азот быстро усваивается растенишли. В виде иона КН4 аммиачный азот поглощается почвой Поэтому А. у. в известной мере закрепляются почвами, значительно меньше подвержены вымыванию, чем нитратные удобрения. Поэтому А. у. более пригодны для осеннего внесения, особенно на легких почвах. Все А. у.
обладают потенциальной кислотностью, но количественное выражение кислотности для отдельных форм этих удобрений различно. А. у. в почве постепенно под воздействием нитрифицирующих бактерий окисляются в нитраты. Скорость нитрификации зависит от температуры, влажности, аэрации и реакции почвы, а также от вида А. у.
Наиболее интенсивно этот процесс идет при хорошей аэрации в теплую погоду. Осенью нитрификация резко ослабляется или приостанавливается. [c.24]
НИТРАТНЫЕ УДОБРЕНИЯ (селитры). Азотные удобрения, содержащие азот в форме нитратов. К ним относятся натриевая, кальциевая и калийная селитры. Селитры аммиачная и кальциевоаммиачная являются аммиачно-нитратными удобрениями, так как они содержат азот одновременно в нитратной и аммиачной форме.
Нитратные формы азота легко растворимы в воде, не поглощаются почвой, легко вымываются атмосферными осадками в нижние слои почвы и также легко в сухие периоды года выносятся с восходящими токами влаги в поверхностный слой почвы. Благодаря высокой подвижности в почве нитратный азот быстро усваивается растениями. Поэтому Н. у.
весьма пригодны для подкормок, когда требуется быстрое усиление азотного питания растений. Высокая подвижность Н.у. ограничивает возможность их использования для основного осеннего внесения под яровые культуры, особенно на легких почвах, где возможны значительные потери Н. у.
вследствие вымывания их осенними дождями и талыми водами. [c.200]
Основными формами азотных удобрений являются аммиачная (соли аммония — сульфат, хлорид, фосфаты и др.), нитратная (соли азотной кислоты — кальциевая, калиевая, натриевая селитры), аммиачно-нитратная (МН4МОз) и амидная (карбамид С0(ННг)2 и др.).
Все минеральные азотные удобрения (за исключением двойных солей типа МеМН4Р04, например, магнийаммонийфосфата MgNH4P04 НгО) хорошо растворимы в воде и быстро переходят в почвенный раствор, что обеспечивает легкую усвояемость азота растением. [c.
20]
Основными формами азотных удобрений являются аммиачная (аммонийные соли — сульфат, хлорид, фосфаты и др.
), нитратная (соли азотной кислоты — кальциевая, калиевая и натриевая селитры), амми-ачно-нитратная (NH4NOз) и амидная [мочевина O(NH2)2 и др.].
Все эти соединения хорошо растворимы в воде и быстро переходят в почвенный раствор, что обеспечивает легкую усвояемость азота растением. [c.2]
Источник: https://www.chem21.info/info/813148/




