
Что такое этиленгликоль, какая у него формула и физические свойства? Как его получают и где применяют? Чем опасен для организма человека этот спирт? В каких случаях происходит отравление им и что за симптомы беспокоят при этом? Как нужно действовать, чтобы помочь пострадавшему?
Что такое этиленгликоль
Этиленгликоль — это представитель спиртов с двумя метильными группами в своём составе. Но в отличие от других он имеет немного маслянистую консистенцию.
Несмотря на то что этиленгликоль был получен ещё в 1859 году, он не сразу занял свою нишу в химии и промышленности. Изначально он использовался во времена Первой мировой войны, как замена глицерина, который широко применялся при производстве взрывчатых веществ.
Химическая формула этиленгликоля — C2H6O2, рациональная — С2Н4(ОН)2. По своим физическим свойствам — это жидкость без запаха, но со сладким вкусом. Он легко соединяется с водой в любой консистенции, что успешно применяется в промышленности, ведь температура замерзания таких жидкостей очень низкая — это улучшает свойства «незамерзаек».

- гликоль;
- этандиол-1,2;
- 1,2-диоксиэтан.
Чаще других употребляется основное название.
К какому классу опасности относится этиленгликоль? — к умеренно токсичное легковоспламеняющееся вещество.
Способы получения
Производством этиленгликоля в промышленных масштабах занялись ещё в тридцатые годы прошлого века. Одним из способов его получения тогда было окисление этилена до его оксида. Около 20 лет такой метод оставался единственным.
Немного позже этиленгликоль стали получать с помощью насыщения оксида этилена водой, в присутствии серной и ортофосфорной кислот. Этот способ оказался выгодней предыдущего, так как на выходе производили более 90% этиленгликоля с минимальным количеством примесей.
Где применяется
В основном этиленгликоль используют в промышленности для обработки техники, что обусловлено его стоимостью — это недорогой и всем доступный продукт.

- более 50% вещества идёт на создание тормозных жидкостей и антифризов, так как смесь гликоля и воды способна сохранять жидкую консистенцию даже при 40º C ниже нуля;
- этиленгликоль входит в состав охлаждающей жидкости — тосола;
- он может устранять коррозию, поэтому гликоль добавляют в антикоррозийные химические соединения.
Где ещё используется этиленгликоль?
- Его можно обнаружить в составе антистатиков.
- Используют для производства средств защиты против обледенения.
- Служит смазкой в холодильных установках.
- Находит применение этиленгликоль как наполнитель в гидравлических системах.
- Гликоль нередко используют для дезинфекции больших помещений.
- Одно из ключевых применений вещества — это производство бытовых химических продуктов, к числу которых относится целлофан, полиуретан.
- Он используется не только при охлаждении автомобилей, но и компьютеров.
- Этиленгликоль или химические соединения в составе с ним применяется, как средство для чистки автомобильных стёкол и зеркал.
 В небольшом количестве присутствует в креме для обработки обуви.
В небольшом количестве присутствует в креме для обработки обуви.- Применяется этиленгликоль и в медицине, как составная часть криопротекторов для тканей и органов. То есть веществ, которые используют для заморозки.
- Это один из компонентов конденсаторов.
- Ключевым свойством этиленгликоля является поглощение воды, что успешно используется, чтобы предотвратить обледенение топлива в авиации и синтеза гидрата метана в трубопроводах, которые проходят в море.
- В органической химии его применяют как высокотемпературный растворитель.
- Без него не проходит синтез химических соединений.
- Где ещё используется этиленгликоль? — даже в наше время с его участием создают взрывчатые вещества.
За прошедшие десятилетия для этого двухатомного спирта нашлось множество применений, что, конечно же, обусловлено его свойствами. Но в медицине он известен не только как полезный и нужный продукт в быту, но и как средство, после контакта с которым человек может умереть.
Так что это такое этиленгликоль? — полезное химическое вещество, без которого не обходится производство большинства органических соединений или сильнодействующий яд с мощным отравляющим эффектом? Давайте узнаем, как может повлиять этиленгликоль на человека.
Влияние этиленгликоля на организм человека
Этот двухатомный спирт в основном входит в состав продуктов для ухода за помещениями, машинами и техникой.
По своим физическим свойствам он отличается от привычного спирта маслянистой консистенцией и отсутствием запаха, поэтому его сложно перепутать с этанолом или изопропанолом, которые нередко употребляют внутрь.
Возможны ли отравления этиленгликолем у людей? — да, несмотря на явные различия с другими спиртами отравиться им можно.
В каких случаях происходит отравление?
 Этиленгликоль является одним из средств обработки больших помещений. Во время нанесения моющих средств его пары вдыхаются, а при нарушении техники безопасности небольшое количество соединения может попасть в рот. Хотя для отравления этого недостаточно.
Этиленгликоль является одним из средств обработки больших помещений. Во время нанесения моющих средств его пары вдыхаются, а при нарушении техники безопасности небольшое количество соединения может попасть в рот. Хотя для отравления этого недостаточно.- Гликоль попадает внутрь при постоянной работе с ним, к примеру, если человек трудится на химическом производстве продуктов, содержащих этиленгликоль.
- Отравиться можно при случайном употреблении его внутрь.
- Так как это химическое соединение используется для обработки машин, то в группе риска находятся люди, регулярно сталкивающиеся с ним по долгу службы.
Этиленгликоль токсичен и относится к веществам третьего класса опасности. После поступления в организм человека он очень быстро всасывается в желудке и верхнем отделе тонкого кишечника. Не более 30% его выделяется в неизменном состоянии почками или в виде солей. Остальная же часть поступает в печень, где и происходит его преобразование.
В печени он разлагается до конечных продуктов:
- гликолевой кислоты;
- муравьиной и щавелевой кислоты;
- гликолевого альдегида.

Как влияет этиленгликоль на организм человека? Все эти конечные продукты распада действуют на кислотно-щелочное равновесие, что постепенно приводит к некрозу клеток головного мозга и почечной ткани.
В организме развивается ацидоз или увеличение кислотности. Смертельная доза для человека составляет всего 100–150 мл.
Но даже попадание небольшого количества этиленгликоля приведёт к развитию отравления, хотя и в лёгкой степени.
Симптомы отравления
В воспалительный процесс после употребления этиленгликоля вовлекаются не только почки и головной мозг. Спирт и его конечные продукты влияют на все системы органов. Скрытый период отравления этиленгликолем в среднем равен 12 часов, но он может укорачиваться или удлиняться в зависимости от количества употреблённого спирта.

- Первый период (начальный) проявляется всего несколько часов, не более 12, и характеризуется лёгким опьянением. Человека беспокоит незначительная слабость и невнятная речь, но в целом самочувствие нормальное. В это время на отравление этиленгликолем указывает только необычный сладковатый запах, исходящий от человека. В редких случаях беспокоит тошнота, периодическая рвота, боли в животе.
- Спустя 12 часов после периода мнимого благополучия, возникает головокружение, головные боли, жажда и тошнота.
- К симптомам отравления этиленгликолем в это время относятся рвота, сильнейшие боли в желудке, которые напоминают признаки острого живота, боль в пояснице и мышцах.
- Немного позже на первое место выходят признаки поражения нервной системы: возбуждение и потеря сознания, появляются многочисленные судороги, увеличивается температура тела.
- Отравление этиленгликолем проявляется ещё и нарушением работы сердца и сосудов: увеличивается частота биения, снижается артериальное давление.
- Нарушается работа дыхательной системы: постепенно появляется одышка, поверхностное дыхание и отёк лёгких.
 Тяжёлые больные теряют сознание.
Тяжёлые больные теряют сознание.- Приблизительно на пятые сутки развивается нарушение в работе почек и печени. Из-за почечной недостаточности летальный исход наблюдается в течение одной недели.
- Смерть наступает в первые дни острого отравления из-за паралича дыхательного центра, отёка лёгких и вследствие сердечно-сосудистой недостаточности.
Лёгкое отравление этиленгликолем наблюдается чаще при вдыхании его паров небольшой концентрации. Оно проявляется незначительными симптомами: слабостью, подташниванием, головокружением.
Первая помощь при отравлении
К сожалению, часто причиной запоздалой или несвоевременной помощи становится лёгкое течение отравления, хроническая интоксикация парами этого спирта или позднее обращение пострадавшего человека к медработникам. В этом случае продукты распада гликоля уже оказывают своё повреждающее действие на внутренние органы и наносят непоправимый ущерб здоровью.
 этанол — антидот при отравлении этиленгликолем
этанол — антидот при отравлении этиленгликолем
Что можно сделать на доврачебном этапе, чтобы помочь пострадавшему? Для этого необходимо быть уверенным в употреблении именно этого вещества. Если этиленгликоль был выпит недавно — нужно незамедлительно промыть желудок и ввести слабительное. Активированный уголь не окажет выраженного эффекта.
Быстро помочь при отравлении этиленгликолем, может, антидот — этанол. В этом случае применяется во внутрь его 30%-й раствор или 5%-й вводится внутривенно. А также в качестве антидота используется кальция хлорид или глюконат 10%-й раствор внутривенно или внутрь.
Не у всех под рукой могут оказаться нужные лекарства для оказания экстренных мероприятий. В этом случае неотложная помощь при отравлении этиленгликолем заключается во введении через зонд или рот обычной водки.
- Если человек без сознания — его нужно уложить набок и дать доступ кислорода — открыть окно, развязать галстук и освободить от стягивающей одежды.
- До момента начала активных действий нужно вызвать бригаду скорой помощи, так как пострадавшему понадобится госпитализация.
- При отравлении этиленгликолем у детей нужно действовать незамедлительно и как можно скорее доставить пострадавшего малыша в ближайшую больницу!
Лечение отравления в стационаре
После госпитализации больному человеку проводят курс интенсивной терапии. Если пострадавшему не был дан антидот бригадой скорой помощи, то по прибытии в стационар его вводят сразу же.
Дальше лечение заключается в применении симптоматических препаратов для коррекции работы жизненно важных органов и систем.
 При отравлении этиленгликолем пострадавшему обеспечивают физический покой, доступ кислорода.
При отравлении этиленгликолем пострадавшему обеспечивают физический покой, доступ кислорода.- Назначают витамины группы B и C, АТФ (аденозинтрифосфорная кислота).
- При необходимости вводят преднизолон.
- При отравлении этиленгликолем назначают в большом количестве фолиевую кислоту, чтобы связать продукты распада этого двухатомного спирта.
- Вводят солевые растворы.
Профилактика отравления
Какая должна быть профилактика отравления этиленгликолем?
- При работе с химическими веществами, содержащими этиленгликоль, нужно использовать индивидуальные средства защиты.
- Не стоит пить подозрительные жидкости.
- Хранить в недоступном для детей месте все химикаты для защиты и обработки машины, а также уборки помещений.
Этиленгликоль — насколько опасно это соединение? Нельзя недооценивать его негативное влияние на организм человека.
Симптомы отравления, при попадании спирта внутрь, развиваются практически молниеносно, а смерть может наступить, спустя всего 5 дней.
Отравление этиленгликолем очень легко предупредить и вылечить, если известно, что человек выпил. В противном случае терапия затягивается надолго.
Источник: https://otravleniya.net/ximicheskie-otravleniya/etilenglikol.html
Формула Этиленгликоля структурная химическая
Структурная формула
 |
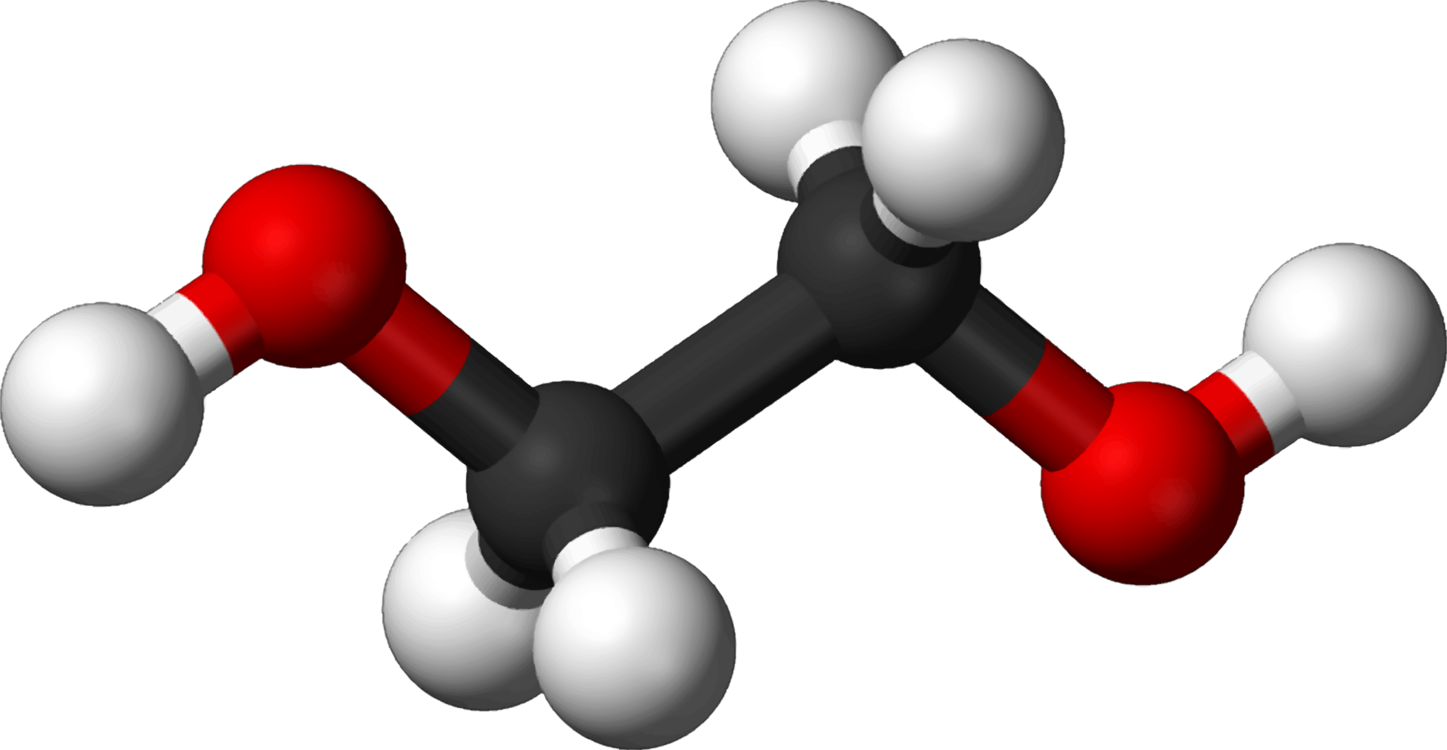 |
Истинная, эмпирическая, или брутто-формула: C2H6O2
Химический состав Этиленгликоля
| C | Углерод | 12,011 | 2 | 38,7% |
| H | Водород | 1,008 | 6 | 9,7% |
| O | Кислород | 15,999 | 2 | 51,6% |
Молекулярная масса: 62,068
Этиленглико́ль (гликоль; 1,2-диоксиэтан; этандиол-1,2), HO—CH2—CH2—OH — двухатомный спирт, простейший представитель полиолов (многоатомных спиртов).
В очищенном виде представляет собой прозрачную бесцветную жидкость слегка маслянистой консистенции. Не имеет запаха и обладает сладковатым вкусом. Токсичен.
Попадание этиленгликоля или его растворов в организм человека может привести к необратимым изменениям в организме и к летальному исходу.
История открытий и производства
Этиленгликоль впервые был получен в 1859 году французским химиком Вюрцем из диацетата этиленгликоля омылением гидроксидом калия и в 1860-м гидратацией этиленоксида.
Он не находил широкого применения до Первой мировой войны, когда в Германии его стали получать из дихлорэтана для использования в качестве замены глицерина при производстве взрывчатых веществ. В США полупромышленное производство начато в 1917 году через этиленхлоргидрин.
Первое крупномасштабное производство начато с возведением завода в 1925 году около Саут Чарлстона (Западная Вирджиния, США) компанией «Carbide and Carbon Chemicals Co.» (англ.). К 1929 году этиленгликоль использовался практически всеми производителями динамита.
В 1937 компания Carbide начала первое крупномасштабное производство, основанное на газофазном окислении этилена до этиленоксида. Монополия компании Carbide на данный процесс продолжалась до 1953 года.
Получение
В промышленности этиленгликоль получают путём гидратации оксида этилена при 10 атм и 190—200°С или при 1 атм и 50—100°С в присутствии 0,1—0,5 % серной или ортофосфорной кислоты, достигая 90 % выхода. Побочными продуктами при этом являются диэтиленгликоль, триэтиленгликоль и незначительное количество высших полимергомологов этиленгликоля.
Применение
Благодаря своей дешевизне этиленгликоль нашёл широкое применение в технике.
- Как компонент автомобильных антифризов и тормозных жидкостей, что составляет 60 % его потребления. Смесь 60 % этиленгликоля и 40 % воды замерзает при −49 °С. Коррозионно активен, поэтому применяется с ингибиторами коррозии;
- Используется как теплоноситель с содержанием не более 50 % в системах отопления (частные дома в основном)
- В качестве теплоносителя в виде раствора в автомобилях, в системах жидкостного охлаждения компьютеров;
- В производстве целлофана, полиуретанов и ряда других полимеров. Это второе основное применение;
- Как растворитель красящих веществ;
- В органическом синтезе:
- в качестве высокотемпературного растворителя.
- для защиты карбонильной группы путём получения 1,3-диоксолана. Обработкой вещества с карбонильной группой в бензоле или толуоле этиленгликолем в присутствии кислого катализатора (толуолсульфоновой кислоты, BF3•Et2O и др.) и азеотропной отгонкой на насадке Дина-Старка образующейся воды. Например, защита карбонильной группы изофорона
1,3-диоксоланы могут быть получены также при реакции этиленгликоля с карбонильными соединениями в присутствии триметилхлорсилана или комплекса диметилсульфат-ДМФА 1,3-диоксалана устойчивы к действию нуклеофилов и оснований. Легко регенерируют исходное карбонильное соединение в присутствии кислоты и воды.
- Как компонент жидкости «И», используемой для предотвращения обводнения авиационных топлив.
- В качестве криопротектора
- Для поглощения воды, для предотвращения образования гидрата метана (ингибитор гидратообразования), который забивает трубопроводы при добыче газа в открытом море. На наземных станциях его регенерируют путём осушения и удаления солей.
- Этиленгликоль является исходным сырьём для производства взрывчатого вещества нитрогликоля.
Этиленгликоль также применяется:
- при производстве конденсаторов
- при производстве 1,4-диоксана
- как теплоноситель в системах чиллер-фанкойл
- в качестве компонента крема для обуви (1—2 %)
- в составе для мытья стёкол вместе с изопропиловым спиртом
- при криоконсервировании биологических объектов (в крионике) в качестве криопротектора.
Очистка и осушение
Осушается молекулярным ситом 4А, полуводным сульфатом кальция, сульфатом натрия, Mg+I2, фракционной перегонкой под пониженным давлением, азеотропной отгонкой с бензолом. Чистота полученного продукта легко определяется по плотности.
Таблица плотности водных растворов этиленгликоля, 20°С
| Плотность, г/мл | 1,050 | 1,058 | 1,067 | 1,074 | 1,082 | 1,090 | 1,098 |
Меры безопасности
Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C. Температура самовоспламенения 380 °C. Температурные пределы воспламенения паров в воздухе, °С: нижний — 112, верхний — 124. Пределы воспламенения паров в воздухе от нижнего до верхнего, 3,8- 6,4 % (по объему).
Этиленгликоль токсичен. По степени воздействия на организм относится к веществам 3-го класса опасности. Летальная доза при однократном пероральном употреблении составляет 100—300 мл этиленгликоля (1,5-5мл на 1 кг массы тела).
Имеет относительно низкую летучесть при нормальной температуре, пары обладают не столь высокой токсичностью и представляют опасность лишь при хроническом вдыхании. Определённую опасность представляют туманы, однако при их вдыхании об опасности сигнализируют раздражение и кашель.
Противоядием при отравлении этиленгликолем являются этанол и 4-метилпиразол. В организме метаболизируется путём окисления до альдегида гликолевой кислоты и далее до гликолевой кислоты, которая затем распадается до муравьиной кислоты и диоксида углерода.
Также он частично окисляется до щавелевой кислоты, которая вызывает повреждения почечной ткани. Этиленгликоль и его метаболиты выводятся из организма с мочой.
Источник: http://formula-info.ru/khimicheskie-formuly/je/formula-etilenglikolya-strukturnaya-khimicheskaya
Гликоли
Гликоли – органическое соединение с двумя гидроксильными группами ОН. Альтернативное название – двухатомные спирты или диолы. Общая формула вещества – CnH2n(OH)2. Простейший представитель класса двухатомных спиртов – этиленгликоль, молекула которого имеет структурную формулу НО−СН2−СН2−ОН.
Первооткрыватель класса диолов – французский ученый Шарль Вюрц, который внес большой вклад в органическую химию.
Впервые гликоли синтезировали сложным методом ученые Уильямс и Берло. Результатом их исследований стало появление двухатомного спирта с высокими эксплуатационными характеристиками.
Жидкость с высокой температурой кипения и низкой температурой кристаллизации нашла применение в промышленности.
С момента открытия гликоли активно используются в системах охлаждения двигателей внутреннего сгорания, холодильных установках и климатическом оборудовании.
Физические и химические свойства гликолей

Этилен- и пропиленгликоль хорошо растворяются в воде и органических растворителях – карбоновых кислотах, кетонах, аминах, спиртах. Низшие гликоли используются в качестве растворителей для большинства органических соединений кроме высших предельных и ароматических углеводородов.
Химические свойства диолов схожи с одноатомными спиртами. При взаимодействии с металлами и их солями образуют алкоголяты, при соединении с кислотами – простые и сложные эфиры. Каждая полярная гидроксильная группа вступает в химическую реакцию независимо друг от друга, что приводит к образованию смеси продуктов.
Получение гликолей
Впервые этиленгликоль был получен путем окисления этилена. Этот способ до сих пор используется в промышленности. Кроме того, для получения двухатомных спиртов также применяют:
- Гидролиз дихлоралканов;
- Реакцию гидратации эпоксидов (оксиранов).
Применение гликолей в промышленности
Самая распространенная концентрация гликоля в водном растворе, при использовании в качестве теплоносителя – 40 %. Испытания показали, что водный раствор двухатомного спирта с добавлением карбоксилатных ингибиторов коррозии сохраняет свои эксплуатационные свойства до 10 лет и более лет.
Использование водных растворов диолов с пакетом противокоррозионных присадок в качестве теплоносителя исключает появление паровых пробок в отопительной системе, уменьшает кавитацию, снижает риск эрозии металла трубок и радиатора. В комплексе это значительно увеличивает эксплуатационный ресурс оборудования.
Водные растворы гликолей с различной концентрацией используются промышленности:
- Машиностроении;
- Приборостроении;
- Добывающей промышленности (нефть, газ, горнодобывающая и т.д.);
- Химической;
- Пищевой.
В качестве теплоносителя обычно применяются растворы этиленгликоля (ЭГ, МЭГ), и пропиленгликоля (ПГ).
Источник: https://hstream.ru/info/dictionary/glikoli/
Этиленгликоль ГОСТ 19710-83. Оптом со склада!

Таблица плотности Этиленгликоля и водных растворов
Этиленгликоль (1,2-этандиол, лат. варианты названий: 1,2-Etandiol, Etylenglykol, Dihydroxietan, Monoetylenglykol) — органическое соединение, предельный двухатомный спирт, получаемый гидратацией этиленоксида или 1,2-дихлорэтана. Химическая формула этиленгликоля – C2H4(OH)2.
Ограниченно растворим в диэтиловом эфире, четыреххлористом углероде, бензоле, толуоле, хлороформе.
Этиленгликоль практически не растворяет минеральные масла, поливинилхлорид, парафины, каучук; плохо растворяет растительные и животные масла.
Растворение этиленгликоля в воде сопровождается выделением теплоты и уменьшением объёма. Его водные растворы характеризуются низкими температурами замерзания.
Получение
В промышленности этиленгликоль получают путём гидрации оксида этилена при 10 атм и 190—200°С или при 1 атм и 50—100°С в присутствии 0,1—0,5 % серной или ортофосфорной кислоты, достигая 90% выхода. Побочными продуктами при этом являются этиленгликоль, триэтиленгликоль и незначительное количество высших полимергомологов этиленгликоля.
Наша компания производит на основе этиленгликоля в виде незамерзающих водных растворов, антифризов и теплоносителей для промышленных и бытовых систем отопления и холодоснабжения серию продуктов с различной концентрацией этиленгликоля: этиленгликоль 30%, этиленгликоль 40%, этиленгликоль 45%, этиленгликоль 50% и этиленгликоль 65% .
Таблица плотности водных растворов этиленгликоля, 20°С
| Концентрация % | 30 | 35 | 40 | 45 | 50 | 55 | 60 |
| Плотность, г/мл | 1,050 | 1,058 | 1,067 | 1,074 | 1,082 | 1,090 | 1,098 |
Применение
Благодаря своей дешевизне Этиленгликоль нашёл широкое применение в технике
- Как компонент автомобильных антифризов и тормозных жидкостей, что составляет 60 % его потребления. Смесь 60 % этиленгликоля и 40 % воды замерзает при −45 °С. Коррозионно активен, поэтому применяется с ингибиторами коррозии;
- В качестве теплоносителя в виде раствора в автомобилях, в системах жидкостного охлаждения компьютеров
- В производстве целлофана, полиуретанов и ряда других. Это второе основное применение;
- Как растворитель красящих веществ;
- В органическом синтезе:В составах для противообледенительной обработки лобовых стёкол и самолётов.
- Как компонент жидкости «И», используемой для предотвращения обводнения авиационных топлив.
- В качестве высокотемпературного растворителя.
- В качестве криопротектора.
- Для поглощения воды, для предотвращения образования гидрата метана, который забивает трубопроводы при добыче газа в открытом море. На наземных станциях его регенириуют путём осушения и удаления солей.
- Этиленгликоль является исходным сырьём для производства взрывчатого вещества нитрогликоля.
Этиленгликоль также применяется:
- при производстве конденсаторов
- при производстве 1,4-диоксана
- компонент в составе систем жидкостного охлаждения компьютеров
- как теплоноситель в чиллер-фанкойл
- в качестве компонента крема для обуви (1—2 %)
- в составе для мытья стёкол вместе с изопропиловым спиртом.
Этиленгликоль — густая бесцветная жидкость, без запаха, сладкая на вкус, ядовита. Температура плавления – 13.2°С, температура кипения 197.6°С. Плотность 1.11 г/см3.
Этиленгликоль обладает целым рядом уникальных свойств, благодаря которым применяется при производстве целого ряда незамерзающих жидкостей — водных растворов, теплоносителей и антифризов для систем отопления и промышленного холодоснабжения: 1) этиленгликоль хорошо растворяется в воде в любых соотношениях, с концентрацией от 0% и до 100%; 2) этиленгликоль придает водным растворам незамерзающие (низкозамерзающие) свойства и температура начала замерзания зависит от концентрации самого этиленгликоля в воде; 3) этиленгликоль обладает хорошими гигроскопическими свойствами — свойствами впитывать, поглощать влагу, воду из поверхностей и воздуха, осушая её; 4) этиленгликоль хорошо растворяет не растворимые или слабо растворимые друг в друге вещества — гидрофобные и гидрофильные соединения. Благодаря всем перечисленным свойствам этиленгликоль является незаменимым компонентом при производстве незамерзающих жидкостей.
Этиленгликоль является активным коррозионным веществом, относится к жирным органическим соединениям, в связи с чем при производстве водных растворов — незамерзающих жидкостей необходимо использовать присадки для защиты систем от коррозии и пенообразований.
Источник: https://regionhim.ru/etilenglikol/
Этиленгликоль: формула, свойства, получение, применение и класс опасность
Глицерин и этиленгликоль (ethylene glycol) являются самыми известными химическими веществами, которые применяют в различных сферах деятельности. Их исследование несколько веков назад показало, что схожих веществ не существует. Многоатомные спирты используют и в химических синтезах, и в отраслях промышленности, и в сферах человеческой деятельности.
Однако эти вещества имеют и отрицательные качества. Поэтому стоит тщательно разобрать состав этиленгликоля, его формулу и степень опасности для человека.
Что такое этиленгликоль
По определению этиленглико́ль (гликоль, 1,2-диоксиэтан, этандиол-1,2) — кислородсодержащее органическое соединение, двухатомный спирт, простейший представитель многоатомных спиртов. Если вещество очищено, то представляет собой прозрачную бесцветную жидкость маслянистой консистенции.
Изначально этиленгликоль использовался во времена Первой мировой войны в качестве глицерина. Однако со временем изменил свое направление. Его стали использовать в различных сферах химической промышленности.
Формула и класс вещества
Химическая формула гликоля — C2H6O2, рациональная — C2H4 (OH) 2, структурная — HO—CH2—CH2—OH . В основе молекулы лежит непредельный скелет этилена, который состоит из двух атомов карбона. На свободные валентные места присоединились две гидроксильные группы.
У этиленгликоля есть несколько названий, которые зачастую встречаются в составе продуктов химического производства:
- гликоль;
- этандиол-1,2;
- 1,2-диоксиэтан.
Молекула имеет подобие транс-конфигурации в размещении гидроксильных групп. Такое расположение соответствует самому удаленному расположению водородов, что дает максимальную устойчивость системы.
Как получают
Массовое получение 1.2-этандиола началось еще в тридцатые годы прошлого века. Сначала получали лишь одним методом, потом появились новые. Таким образом, гликоль можно получить несколькими способами, однако некоторые из них стали частью истории, а другие превзошли их качеством.
Изначально 1,2-диоксиэтан получали из дибромэтана. Двойная связь этилена разрывается, а свободные валентности занимаются галогенами — исходным веществом в данной реакции. Образование промежуточного соединения возможно благодаря замещению ацетатными группами, которые при гидролизе превращаются в спиртовые.
С улучшением технологий появился новый метод — получение этиленгликоля прямым гидролизом любых этанов и этиленов , которые замещены двумя галогенами соседних атомов карбона. С помощью различных водных растворов, карбонатов металлов, воды и диоксида свинца начинается реакция, которая возможна лишь при больших температурах и давлении. Побочные вещества — диэтиленгликоль и триэтиленгликоль.
Следующий способ позволил получать 1,2-диоксиэтан из эфира этиленхлоргидрина путем его гидролиза угольными солями. При 170 градусах выход целевого продукта достигал 90 %. Однако был значительный недостаток — гликоль необходимо извлекать из раствора соли. Ученые решили эту проблему. Они разбили процесс на две стадии, при этом оставив то же исходное вещество.
Гидролиз этиленгликоль ацетатов стал отдельным способом, когда получилось добыть исходный реагент путем окисления этилена в уксусной кислоте кислородом.
Свойства
1,2-диоксиэтан не имеет запаха, однако, имеет сладковатый вкус. Относят к умеренно токсичным легковоспламеняющимся веществам. Легко соединяется с водой. Это используют в промышленности, так как температура замерзания таких веществ очень низкая.
Физические
Еще в прошлом веке стало известно, что этиленгликоль обладает уникальными свойствами.
Характеристики:
- температура возгорания составляет от +112 ˚С до +124 ˚С;
- самовоспламениться может при нагреве до +380 ˚С;
- чистый этиленгликоль замерзает при -12 ˚С;
- раствор на водной основе может замерзать при температуре ниже -65 ˚С, а при более низком значении начинается образование кристаллов льда;
- точка кипения чистой жидкости достигается при +121 ˚С;
- плотность — 11,114 г/см³.
Такие характеристики дают возможность применять 1,2-диоксиэтан в различных сферах производства.
Химические
Вещество имеет несколько названий, но все они означают одно и то же. Собственно, и химические свойства у них одинаковы. Если массовая доля вещества достигает 99.8%, то оно высшего сорта.
Список химических свойств:
- молярная масса — 62,068 г/моль;
- коэффициент оптического преломления — 1,4318;
- константа диссоциации кислоты — 15,1±0,1;
- умеренно токсичный.
1.2-этандиол относят к третьей группе опасности, поэтому предельно допустимые концентрации в атмосфере по ГОСТу могут быть не более 5 миллиграмм/м³.
Применение
Этиленгликоль нашел свое призвание во многих отраслях. Незаменимым веществом является и в автомобилестроении. Его уникальные свойства позволяют создать высококачественные жидкости.
Может регенерировать исходное карбонильное соединение в присутствии воды и кислоты:
- Как компонент противоводокристаллизационной жидкости «И».
- В качестве криопротектора.
- Для поглощения воды, предотвращения образования гидрата метана, который забивает трубопроводы при добыче газа в открытом море. На наземных станциях его регенерируют путем осушения и удаления солей.
- Этиленгликоль является исходным сырьем для производства взрывчатого вещества нитрогликоля.
1,3-диоксоланы могут быть получены при реакции этиленгликоля с карбонильными соединениями в присутствии триметилхлорсилана. Такие соединения устойчивы к действию нуклеофилов и оснований.
В автомобилях
благодаря своей дешевизне этиленгликоль нашел широкое применение в технике.
он может быть использован:
- как компонент тормозных жидкостей и автомобильных антифризов;
- как теплоноситель с содержанием не более 50 % в системах отопления;
- в качестве теплоносителя в виде раствора в автомобилях и системах жидкостного охлаждения компьютеров;
- в производстве полиуретанов, целлофана и ряда других полимеров;
- как растворитель красящих веществ;
- в качестве высокотемпературного растворителя.
- для защиты карбонильной группы путем получения 1,3-диоксолана.
наиболее известное его направление — компонент автомобильных антифризов. эта отрасль составляет 60 % его потребления. такие смеси могут не замерзать при низких температурах, а также коррозийно устойчивы.
в других отраслях
кроме того 1,2-диоксиэтан является незаменим и в других отраслях промышленности.
1.2-этандиол также применяется:
- при производстве конденсаторов;
- при производстве 1,4-диоксана, пропиленгликоля;
- как теплоноситель в системах чиллер-фанкойл;
- в качестве компонента крема для обуви;
- в составе для мытья стекол вместе с изопропиловым спиртом;
- при криоконсервировании биологических объектов в качестве криопротектора;
- при производстве полиэтилентерефталата, пластика.
и хотя 1,2-диоксиэтан применяют в других отраслях, их процент применения довольно мал.
вред для человека
Однако 1.2-этандиол имеет и свои минусы. Неряшливое или неаккуратное его использование может привести к трагическим последствиям.
Класс опасности вещества
Класс опасности этиленгликоля — третья группа, то есть его контакт с окружающей средой должен быть как можно меньше. Если же 1.2-этандиол попадает в организм человека, в нем могут развиться необратимые негативные явления. При однократном употреблении внутрь 100 и более миллилитров наступает летальный исход.
Пары данного вещества же менее токсичны, однако систематическое вдыхание может привести к гибели. Если человек отравляется гликолем, ему следует принять препарат, который содержит 4-метилпиразол.
Симптомы отравления
В воспалительный процесс вовлекаются все системы органов. Скрытый период отравления этиленгликолем обычно равен 12 часам, но сроки могут изменяться в зависимости от количества употребленного спирта.
Симптомы отравления:
- Первый период проявляется всего несколько часов, но не более 12. Характеризуется легким опьянением. Появляется незначительная слабость и невнятная речь, но в целом самочувствие нормальное. В редких случаях беспокоит тошнота, периодическая рвота и боли в животе. От отравленного человека исходит сладковатый запах.
- Через 12 часов после отравления возникает головокружение и головные боли, жажда и тошнота. Появляется рвота, сильнейшие боли в желудке, боль в пояснице и мышцах.
- Немного позже появляются признаки поражения нервной системы: возбуждение и потеря сознания, многочисленные судороги, повышается температура тела. Отравление этиленгликолем проявляется нарушением работы сердца и сосудов: увеличивается частота биения, снижается артериальное давление.
- Нарушается работа дыхательной системы: постепенно появляется одышка, поверхностное дыхание и отек легких. Тяжелые больные теряют сознание.
- Приблизительно на пятые сутки развивается нарушение в работе печени и почек. Из-за почечной недостаточности возможен летальный исход в течение одной недели.
- Если произошло острое отравление, то наступает смерть из-за паралича дыхательного центра и отека легких.
Легкое отравление возможно при вдыхании паров 1.2-этандиола. Симптомами являются легкая тошнота, слабость.
Меры предосторожности при работе с этиленгликолем
Этиленгликоль является горючем веществом. Температурные пределы воспламенения паров в воздухе начинаются от 112 и заканчиваются 124 °С. Пределы воспламенения паров в воздухе от нижнего до верхнего — 3,8‒6,4 % от объема.
Летальная доза при однократном пероральном употреблении — 100‒300 мл этиленгликоля. Имеет относительно низкую летучесть при нормальной температуре. Опасность представляют туманы, однако при их вдыхании об опасности сигнализируют раздражение и кашель. П ри отравлении следует принять препараты, содержащие этанол или 4-метилпиразол.
Видео о получении вещества
В следующем видео расскажут о получении гликоля.
Источник: https://bibiauto.club/remont/autohimiya/etilenglikol.html
Физические и химические свойства этиленгликоля, формула
- Для простого человека, никаким образом не связанным с химией и её производными продуктами даже название соединений и веществ окажутся малознакомыми, но мало кто из автолюбителей или людей, кто занимается техникой или её обслуживанием, не слышал о том, что такое этиленгликоль.
- Этиленгликоль, также именуемый гликолем, этандиолом или диоксиэтаном – неотъемлемая и базовая часть антифризов разных марок, тормозных жидкостей, теплоносителей, а также применяется в функционировании охладительных систем компьютерной аппаратуры.
- Таким образом, это вещество обладает большой популярностью и востребованностью не только среди крупных промышленных производств, но среди автовладельцев, инженеров и даже домохозяек (этиленгликоль используется при изготовлении средств для мытья стёкол).
Строение и структура соединения. В качестве эфира
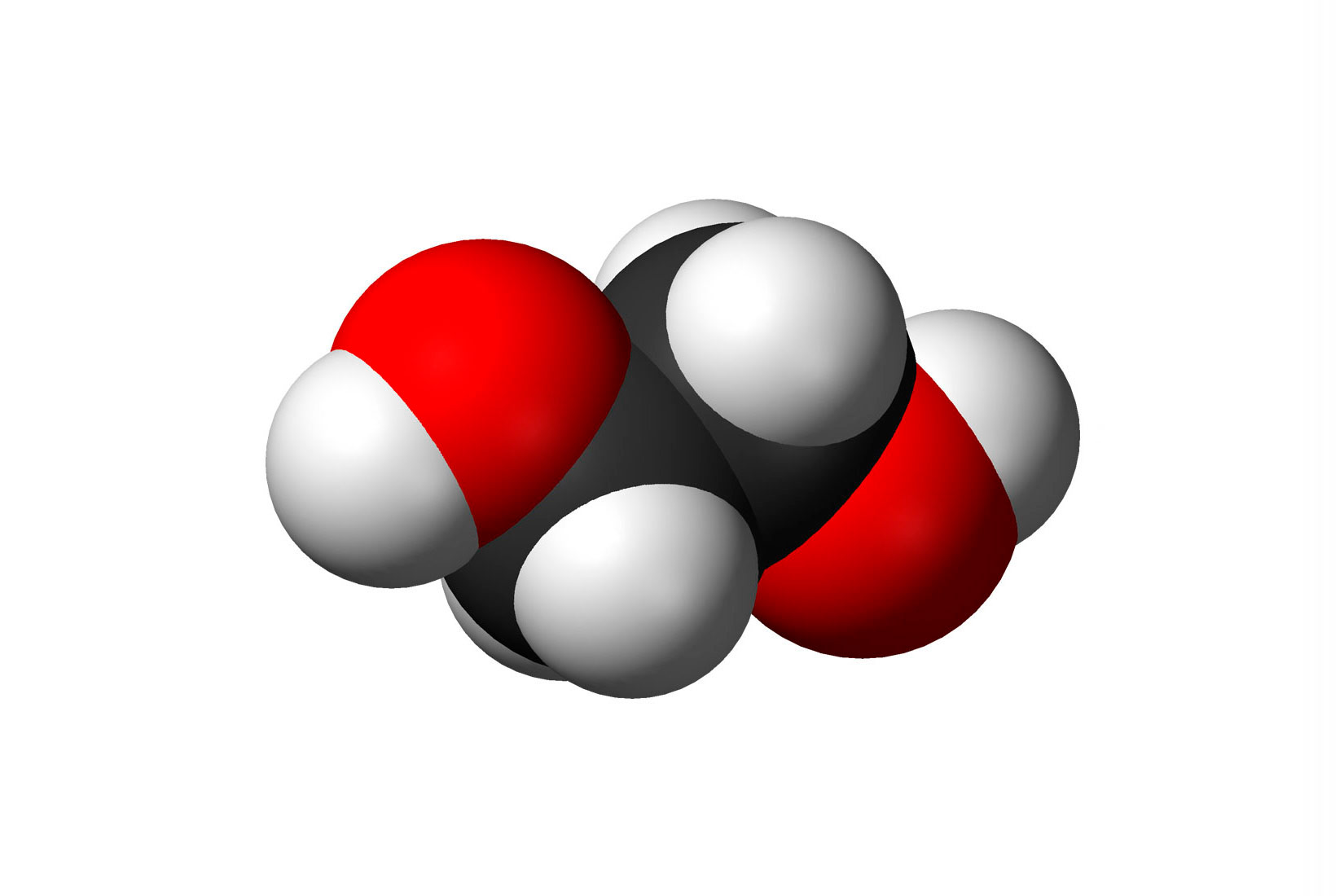
Этиленгликоль состоит из двух атомов спирта, что определяет его принадлежность к полиолам. По структуре и строению очень близок к глицерину и представляет собой жёсткую сцепку двух гидроксильной группы (OH и HO) с двумя соединенаиями этилена (CH2). Если расписывать это химической формулой строения, то это представляется следующим образом: HO—CH2—CH2—OH.
Формула
Для обозначения этиленгликоля используются сразу несколько формул, точно также, как и названий (систематических или традиционных).
Химическая формула этиленгликоля: C2H6O2, представляется более понятной для людей, изучавших в школе органическую химию, однако существует также и рациональная структурная формула этиленгликоля (C2H4(OH)2) – отображающая тоже самое, но имеющая больше смысла для профессионалов.
Характеристики. Свойства: плотность, свойства, температура
Способен сохранять тепло, впитывать жидкость, вступать в реакцию с коррозией, предотвращая её, а также, самое главное для всех владельцев автомашин – он очень плохо замерзает (при 45 градусах ниже ноля), что делает его незаменимым в производстве антифриза и схожих по назначению средств.
Химические свойства этиленгликоля: плотность этиленгликоля — 1,11 грамм на кубический сантиметр; этиленгликоль реагирует с самими разными веществами и соединениями, например с натрием при образовании алкоголята, также популярной является соединение этиленгликоль hbr, в ходе которого образуются дибромэтан и вода; температура кипения этиленгликоля: 197 с половиной градусов по Цельсию.
Способ получения
Этиленгликоль получают благодаря процессу гидратации (присоединение к элементу молекул воды) оксида этилена (бесцветного газа, оставляющего во рту сладкий привкус, характеризующийся также опасным влиянием на организм человека). Формула этандиола позволяет получать его без сложных приспособлений и в короткие сроки.
Область применения и цена. Этиленгликоль как антифриз, теплоноситель и охлаждающая жидкость в одном растворе
Чудодейственных двухатомный спирт применяется очень широко, в огромном количестве отраслей и в повседневной жизни встречается куда чаще, чем может показаться – от науки и химической промышленности (органический синтез) до более привычных вещей – жизненно необходимых любому водителю антифриза, тормозных жидкостей, при производстве целлофана, моющих средств и даже обувных кремов. Применение этиленгликоля безусловно удобно и окупает себя.
Производство этиленгликоля дело требует минимальных затрат, а поэтому и себестоимость, и цена оптом (а в других целях, кроме промышленного использования, закупать этиленгликоль в чистом виде не имеет большого смысла) весьма демократична – поставщики запрашивают за килограмм продукта чуть больше пятидесяти рублей и всё будет зависеть от доли воды раствора и количества).
Так, за двадцать килограмм придётся заплатить полторы тысячи, а за двести сорок – почти шестнадцать тысяч рублей. Для особо бережливых покупателей есть предложения заливке вещества в вашу тару, поэтому и цену можно регулировать исходя из потребности.
Антифризы с этиленгликолем (примерно 5 килограмм) от производителей Sintec или Sibiria встанут автовладельцам в зависимости от состава и веса в суммы от ста до восьмисот рублей.
Влияние этиленгликоля на организм человека
- Как уже было сказано, этиленгликоль чрезвычайно токсичен и может привести не только к тяжким последствиям для здоровья (включая даже мутагенные риски), но и к смерти неосторожного владельца.
- Чрезвычайно токсичны даже 100 миллиграмм вещества, если они попадают внутрь организма, пары этиленгликоля менее опасны, но за его концентрацией в помещении нужно пристально следить, чтобы избежать самых разнообразных последствий – от галлюцинаций до потери сознания, от простого кашля и рези в глазах до тяжёлых последствий репродуктивного плана.
Основы мер безопасности. Зачем избегать замерзание этого спирта?
Хранить этиленгликоль необходимо в специальной таре (такие ещё называют химическими) которую можно надёжно закрыть.
Тара, желательно, должна быть из стали, которую в свою очередь помещается в сухом неотапливаемом помещении.
Нужно отметить, что этандиол горюч, поэтому следует избегать обращение с огнём рядом с открытым веществом, а также продумать вероятность непредвиденных ситуаций, вроде короткого замыкания.
Закрытая тара и дополнительные меры предосторожности (например, наличие хорошей вентиляции помещения при обращении с веществом) помогут избежать вдыхания большой концентрации паров этиленгликоля.
Не допускайте попадания на слизистые и ни в коем случае не принимайте внутрь!
Требования ГОСТ 19710 к готовому гликолю
Межгосударственный стандарт устанавливает целый свод требований к этиленгликолю:
- Технические (массовая доля вещества не больше 99%, преломление от 1431—1432, пропускание света не больше 75 %, доли остатка от прокаливания – 1 тысячная, доля железа – не более 1 десятитысячной, для воды – не больше 1 десятой);
- Требования к безопасности (концентрация в атмосфере – не больше пяти мг на квадратный метр; произведённый по гост этиленгликоль относится к третьей степени опасности химических веществ ; хранилище должно быть вентилируемым; рабочие одеты спецодеждой; при попадании на землю или кожу этиленгликоль необходимо быстро смыть большим количеством воды);
- Правила приёмки (принимается по частям не более восьмисот тонн с пакетом документов, включающих в себя наименование производителя, продукта, вид продукта и его массу, номер партии и т.д.);
- К упаковке, маркированию, перемещению и хранению (наливаются в предварительно вымытые и высушенные бочки из алюминия или из антикоррозийной стали; перевозится в крытом транспорте или специализированных цистернах на поездах или грузовых автомашинах, или в пакетированном виде на специальных поддонах; бочки или пластиковые пакеты/бутыли должны храниться вертикально).
Источник: http://motorstory.ru/medicina/fizicheskie-i-ximicheskie-svojstva-etilenglikolya-formula/
Этиленгликоль, моноэтиленгликоль, МЭГ, 1,2-этандиол
Описание продукта (химическая формула, назначение):- Формула: HO-CH2-CH2-OH- Молекулярная масса: 62,07ГОСТ 19710-83 Этиленгликоль.Этиленгликоль получают при гидратации окиси этилена.
1. Технические характеристики.
№ Наименование показателя Норма высший сорт 1-й сорт
ОКП 24 2212 0120 ОКП 24 2212 01301. Массовая доля этиленгликоля, %, не менее 99,8 99,52. Массовая доля диэтиленгликоля, %, не более 0,05 1,03. Цвет, единицы Хазена, не более — В обычном состоянии 5 20 — После кипячения с соляной кислотой 20 не нормируется4. Массовая доля остатка после прокаливания, %, не более 0,001 0,0025. Массовая доля железа (Fe), %, не более 0,00001 0,00056. Массовая доля воды, %, не более 0,1 0,57. Массовая доля кислот в пересчете на уксусную кислоту, %, не более 0,0006 0,0058. Показатель преломления при 20 С 1,431 — 1,432 1,430 — 1,432
Настоящий стандарт распространяется на этиленгликоль, получаемый гидратацией окиси этилена, и устанавливает требования к этиленгликолю, изготовленному для нужд народного хозяйства и экспорта.
Этиленгликоль применяют в производстве синтетических волокон, смол, растворителей, низкозамерзающих и гидравлических жидкостей, косметике и для других целей.По внешнему виду этиленгликоль представляет собой прозрачную жидкость.
Моноэтиленгликоль — это двухатомный спирт, бесцветная, вязкая, сладковатая на вкус жидкость, с температурой кипения 197 oС, плотностью при 20 oС = 1,112-1,113 г/см3, температурой начала замерзания минус 12-13 oС.Этиленгликоль — основа охлаждающих жидкостей обладает уникальной возможностью не замерзать при пониженных температурах.
Исключительно важным свойством этиленгликоля является его способность понижать температуру замерзания водных растворов. При определенном соотношении системы «вода — этиленгликоль» можно получить жидкость с необходимой температурой замерзания от минус 1 до минус 70 oС.
Водные растворы этиленгликоля не расширяются при замерзании и не образуют сплошной твердой массы, а превращаются в кашицеобразную рыхлую массу, объем которой больше первоначального только на 0,25%-0,30%.
Чтобы разбавленный водой этиленгликоль стал охлаждающей автожидкостью, в него необходимо добавить еще около 7-8, а то и больше компонентов, и отсутствие какого-либо из них может не только существенно снизить качество антифриза, но и просто стать опасной для автомобильных систем охлаждения. 2.
Плотность этиленгликоля в зависимости от температуры
- оС кг/дм3 оС кг/дм3 оС кг/дм3
- -10 1,1352 12 1,1194 34 1,1042
- -9 1,1346 13 1,1188 35 1,1036
- -8 1,134 14 1,1182 36 1,103
- -7 1,1334 15 1,1176 37 1,1022
- -6 1,1328 16 1,117 38 1,1014
- -5 1,1322 17 1,1162 39 1,1006
- -4 1,1316 18 1,1154 40 1,0998
- -3 1,131 19 1,1146 41 1,099
- -2 1,1304 20 1,1138 42 1,0984
- -1 1,1298 21 1,113 43 1,0978
- 0 1,129 22 1,1124 44 1,0972
- 1 1,127 23 1,1118 45 1,0966
- 2 1,1266 24 1,1112 46 1,096
- 3 1,1261 25 1,1106 47 1,0954
- 4 1,1257 26 1,11 48 1,0948
- 5 1,1253 27 1,1092 49 1,0942
- 6 1,1249 28 1,1084 50 1,0936
- 7 1,1245 29 1,1076 51 1,093
- 8 1,124 30 1,1068 52 1,092
- 9 1,1227 31 1,106 53 1,091
- 10 1,1214 32 1,1054 54 1,09
- 11 1,12 33 1,1048 55 1,089
- Температура замерзания водно-гликолевой смеси
- Температура замерзания водно-гликолевого раствора
3. Сравнительная характеристика физико-химических свойств воды и моноэтиленгликоля
Показатель Вода МЭГ
Молярная масса 18,01 62,07 Плотность при 20оС, кг/м3 998,2 1113 Температура замерзания, оС 0 -12 Температуры кипения при 0,1 МПа, оС 100 197,7 Теплоемкость при 20оС, кДж/(кг*оС) 4,184 2,422 Коэффициент теплопроводности, кДж/(ч*м*оС) 2,179 0,955 Вязкость при 20оС, мм2/с 1,0 19-20 Теплота испарения, кДж/кг 2,258 0,800 Коэффициент объемного расширения (0-100оС) 0,00046 0,00062
4. Свойства водных растворов этиленгликоля
Концентрация этиленгликоля, Плотность кг/дм3, Температура замерзания, оС
% по массе при 20оС 26,4 1,0340 -10 36,4 1,0506 -20 45,6 1,0627 -30 52,6 1,0713 -40 58,0 1,0780 -50 63,1 1,0833 -60 66,0 1,0848 -65 66,7 1,0856 -73 72,1 1,0923 -60 78,4 1,0983 -50
Этиленгликоль в очищенном виде – это прозрачная бесцветная жидкость маслянистой консистенции без запаха.
Этиленгликоль применяют в качестве теплоносителя в системах нагрева и отопления, используют в системах охлаждения как холодоноситель в производстве антифризов, тосолов, гидравлических, тормозных жидкостей для автомобилей.
Еще несколько сфер использования этиленгликоля: производство смол, синтетических волокон, растворителей, полиуретанов, душистых и взрывчатых веществ, кожевенная промышленность и фармакология.
Особо отметим, что этиленгликоль как низкозамерзающая жидкость (антифриз) заменяет воду из-за низкой температуры замерзания и более высокой температуры кипения.
Этиленгликоль т.о., применяется, как охлаждающая жидкость в ДВС, антиобледенитель в авиации, хладоноситель в системах охлаждения.
Вернуться к списку…
Источник: https://proizvodstvo-avtohimii.ru/home/spravka/etilenglikol/




