![]()
![]()
![]()
![]()
Гексан, C6H14 – органическое вещество класса алканов. В природе содержится в природном газе, добываемом из газовых и газоконденсатных месторождений, в попутном нефтяном газе, в нефти.
- Гексан, формула, характеристики
- Физические свойства гексана
- Химические свойства гексана
- Применение и использование гексана
Гексан, формула, характеристики:
Гексан – органическое вещество класса алканов, состоящий из шести атомов углерода и четырнадцати атомов водорода.
Химическая формула гексана C6H14. Имеет пять изомеров: н-гексан, 2-метилпентан (изогексан), 3-метилпентан, 2,3-диметилбутан (диизопропил) и 2,2-диметилбутан (неогексан). Изомеры гексана различаются между собой по своим физическим свойствам.
Формула н-гексана CH3CH2CH2CH2CH2CH3, 2-метилпентана (изогексана) CH3CH(CH3)CH2CH2CH3, 3-метилпентана CH3CH2CH(CH3)CH2CH3, 2,3-диметилбутана (диизопропила) CH3CH(CH3)CH(CH3)CH3 и 2,2-диметилбутана (неогексана) CH3C(CH3)2CH2CH3.
Строение молекулы н-гексана:

Строение молекулы 2-метилпентана (изогексана):

Строение молекулы 3-метилпентана:

Строение молекулы 2,3-диметилбутана (диизопропила):
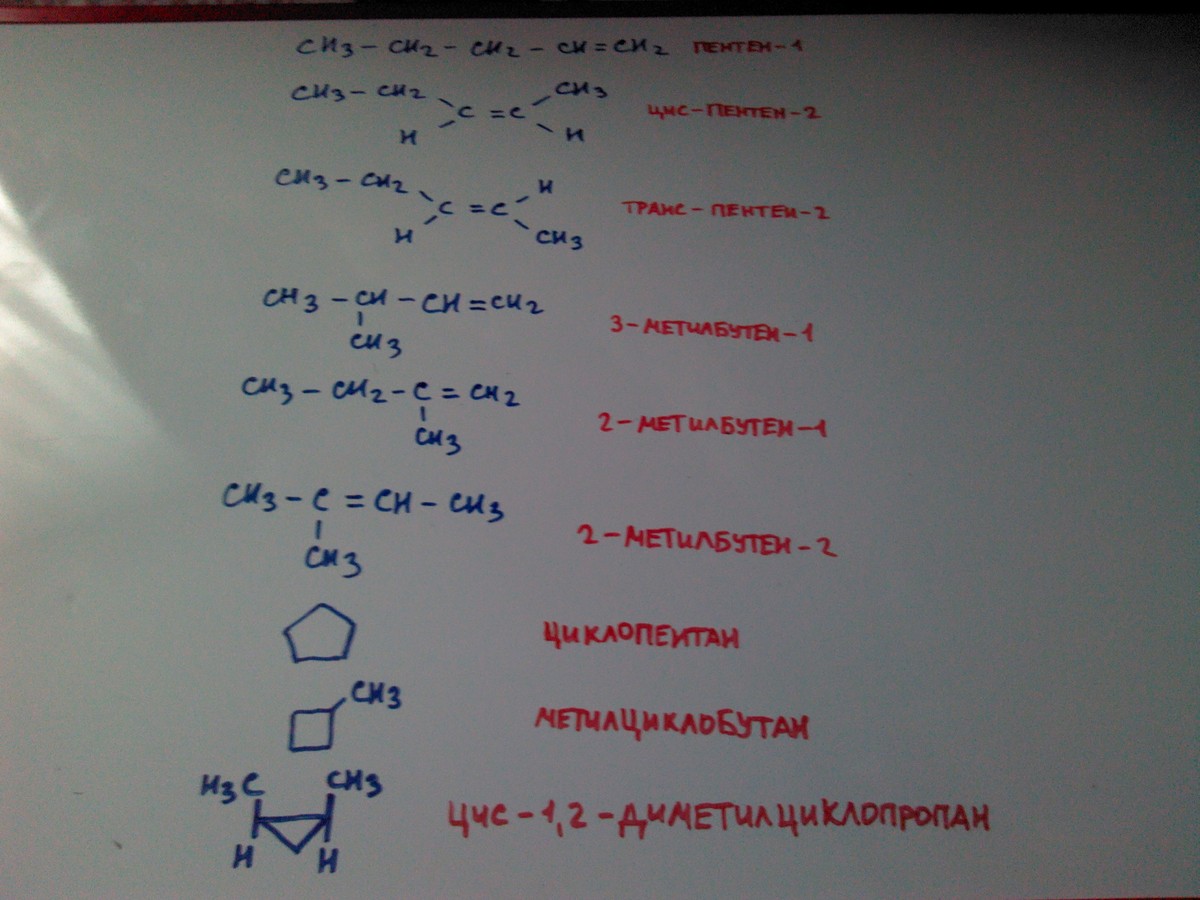
Строение молекулы 2,2-диметилбутана (неогексана):

Все изомеры гексана – бесцветная горючая жидкость со слабым запахом, который напоминает дихлорэтан.
В природе содержится в природном газе, добываемом из газовых и газоконденсатных месторождений, в попутном нефтяном газе, в нефти (в значительных количествах). Также содержится в сланцевой нефти, сланцевом газе.
Пожаро- и взрывоопасен.
Мало растворяется в воде. Растворяется в органических веществах (ацетон, бензол, хлороформ, диэтиловый эфир и другие).
Гексан по токсикологической характеристике относится к веществам 3-го класса опасности (умеренно опасным веществам) по ГОСТ 12.1.007.
Физические свойства гексана:
| Наименование параметра: | Значение: |
| Цвет | без цвета |
| Запах | слабый запахом, который напоминает дихлорэтан |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | жидкость |
| Плотность н-гексана (при 20 °C и атмосферном давлении 1 атм.), кг/м3 | 654,8 |
| Плотность н-гексана (при 0 °C и атмосферном давлении 1 атм.), кг/м3 | 677,4 |
| Температура плавления н-гексана, °C | -95,3 |
| Температура плавления 2-метилпентана (изогексана), °C | -153,7 |
| Температура плавления 3-метилпентана, °C | -118 |
| Температура плавления 2,3-диметилбутана (диизопропила), °C | -128,5 |
| Температура плавления 2,2-диметилбутана (неогексана), °C | -99,9 |
| Температура кипения н-гексана, °C | 68,7 |
| Температура кипения 2-метилпентана (изогексана), °C | 60,3 |
| Температура кипения 3-метилпентана, °C | 63,3 |
| Температура кипения 2,3-диметилбутана (диизопропила), °C | 58 |
| Температура кипения 2,2-диметилбутана (неогексана), °C | 49,73 |
| Температура самовоспламенения н-гексана, °C | 233 |
| Температура вспышки н-гексана, °C | -23 |
| Критическая температура н-гексана, °C | 234,7 |
| Критическое давление н-гексана, МПа | 3,032 |
| Взрывоопасные концентрации смеси газа н-гексана с воздухом, % объёмных | от 1,24 до 7,5 |
| Удельная теплота сгорания н-гексана, МДж/кг | 45,105 |
| Молярная масса, г/моль | 86,17848 |
Химические свойства гексана:
Химические свойства гексана аналогичны свойствам других представителей ряда алканов. Поэтому для него характерны аналогичные химические реакции.
См. Химические свойства бутана.
Применение и использование гексана:
- – входит в состав бензина,
- – при экстрагировании растительных масел,
- – входит в состав клеев,
- – как органический растворитель,
- – как сырье для производства бензола.
Примечание: © Фото //www.pexels.com, //pixabay.com
-

- карта сайта
- газовая газ редуктор газовый баллон метан гексан этан гексан пропен цена купить реакции 1 4 50 3 какой кислород вещество авто температура кг воздух вода
заправка баллонов гексаном
сколько литров стоимость сгорание уравнение реакций давление смесь расход объем литр гексана
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
- Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
- Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
- Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
- Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
- Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Источник: https://xn--80aaafltebbc3auk2aepkhr3ewjpa.xn--p1ai/geksan-svoystva-himicheskie-reaktsii/
Метанол — химические и физические свойства, общая характеристика


Метанол это химическое вещество, называемое древесным или метиловым спиртом. Его получение не является сложным, поскольку он относится к одноатомным продуктам. Использование в алкогольных напитках может привести к пищевому отравлению. Он также может образовывать взрывоопасные смеси при температуре 8 градусов по Цельсию.
Чтобы правильно понимать суть происходящего, стоит обратить внимание на название вещества. В его составе 4 атома водорода и по одному атому углерода и кислорода.

- Молекулярная формула выглядит так — CH3OH.
- Плотность находится на отметке 0,8101 г/см3.
- Структура отображается в таблице следующим образом:
| Название вещества | Число атомов | Процент содержания массы | Молярный вес каждого по отдельности |
| O2 — кислород | 1 | 49,9% | 16 |
| H2 — водород | 4 | 37,5% | 1,008 |
| С — углерод | 1 | 12,6% | 12,011 |
История открытия
Впервые это вещество обнаружил Роберт Бойль. В 1661 г. он успешно завершил первую сухую перегонку древесины. В чистом виде метанол получилось выделить только через 170 лет.
В 1834 г. два французских химика установили его химическую формулу. А еще через 23 года впервые получили через омыление метилхлорида.
Промышленность занимается его выпуском в крупных масштабах. Причем способов для этого довольно много. Одним из самых востребованных является синтезирование метана.
Процесс реакции связан с неполным окислением и образованием формы эфира. Еще один способ, разрешенный стандартами ГОСТ, связан с разложением солевых отложений муравьиной кислоты.
Применение метилового спирта
Органическая химия использует его как растворитель. Нефтегазовая и техническая промышленность с его помощью предотвращает появление кристаллических соединений. Это связано с низкой температурой порога замерзания.

В домашних условиях синтез подразумевает окрашивание с помощью лакокрасочных продуктов. Ведь их получение и начальная консистенция зависит от нескольких составляющих.
Насчет суррогатного алкоголя стоит понять одну простую вещь. При попадании в организм, вред неизбежен и необратим вообще. Вероятность отравления и смертельного исходя очень высока.
Физические свойства
По сути, метанол это бесцветная жидкость. Теплопроводные свойства древесного спирта в два раза меньше, чем у бензина. Участвует в образовании взрывоопасных веществ из-за собственной горючести. Температура кипения метанола 64,70С.

Температура горения начинается от 460 градусов. Смешивается с различными жидкостями без каких-либо проблем. Таким способом получения добиваются образования веществ на жидкой основе, не содержащих алифатические углеводы. Азеотропные смеси появляются после тщательного смешивания с ацетоном или дихлорэтаном. Очень токсичен.
Химические свойства и реакции
Как и горючие смеси, метанол имеет собственное октановое число, даже в газообразном состоянии. Оно равняется 111 единицам, что допускает использование в двигателях внутреннего сгорания. Причем это получается даже в состоянии метилового спирта.

Также возможен вариант замены водорода щелочными металлами. Сложные эфиры получаются при взаимодействии с карбоновыми кислотами или минеральными. Положительно реагирует на галогениды фосфора.
Нахождение в природе
Очень редко такое вещество можно обнаружить в свободном состоянии. Даже если удается случайно наткнуться, то количество будет крайне мало. Зато компоненты для производства находятся практически везде. Это растительные масла, различные породы деревьев, почвы и даже минералов.
Класс опасности древесного спирта
Для человека даже 10 мг уже смертельное отравление. А поскольку одним из результатов станет получение слепоты, то класс опасности (по ГОСТ 12.1.007-76) — 3. Не важно, жидкое состояние или газообразное. Классификационный код FT1, вторая группа упаковок.
Влияние на человеческий организм
Патологические изменения наступают после превышения допустимой нормы. Но слепота это только начало. Дальнейшие действия приведут к поражению участков головного мозга, полному нарушению работы мочевыводящих органов.

Моментальная смерть наступает при содержании в организме до 2 граммов на каждый килограмм веса. Это вызвано тем, что одноатомный спирт окисляется до яда формальдегид, который применялся раньше в качестве бесшумного убийцы. Он сразу парализует нервную систему и воздействует на белковые соединения. При этом токсический эффект появляется только через несколько часов.
Заключение
В высокоразвитых странах метанол добавляют в топливо для автомобилей. Ведь благодаря его свойствам и взаимодействию с горючими веществами, получается экологически чистый продукт. В Российской Федерации использование в качестве товаров для потребителей запрещено по закону. Очень много случаев отравления с летальным исходом.
Источник: https://nauka.club/khimiya/metanol.html
Ацетон
Ацетон (диметилкетон, пропанон-2) — органическое вещество, имеющее формулу CH3—C(O)—CH3 (C3H6O), простейший представитель насыщенных кетонов.
Своё название ацетон получил от лат. acetum — уксус. Это связано с тем, что ранее ацетон получали из ацетатов, а из самого ацетона получали синтетическую ледяную уксусную кислоту.
В 1848 году немецкий профессор медицины и химии Леопольд Гмелин ввёл термин в официальное употребление, использовав старое немецкое слово Aketon (кетон, ацетон), которое также берёт корни от латинского acetum.
Открытие
 — первым открыл ацетон
— первым открыл ацетон
Один из простейших и в то же время важнейших из кетонов — ацетон — впервые выявлен в 1595 году немецким химиком Андреасом Либавием в процессе сухой перегонки ацетата свинца. Однако точно определить его природу и химический состав удалось только в 1832 году Жану-Батисту Дюма и Юстусу фон Либиху. До 1914 года ацетон получали практически исключительно коксованием древесины, однако повышенный спрос на него в годы Первой мировой войны очень быстро стимулировал создание новых методов производства.
Физические свойства
Ацетон — бесцветная подвижная летучая жидкость (при н.у.) с характерным резким запахом. Во всех соотношениях смешивается с водой, диэтиловым эфиром, бензолом, метанолом, этанолом, многими сложными эфирами и так далее.
Основные термодинамические свойства ацетона:
- Поверхностное натяжение (20 °C): 23,7 мН/м
- Стандартная энтальпия образования ΔH (298 К): −247,7 кДж/моль (ж)
- Стандартная энтропия образования S (298 К): 200 Дж/моль·K (ж)
- Стандартная мольная теплоемкость Cp (298 К): 125 Дж/моль·K (ж)
- Энтальпия плавления ΔHпл: 5,69 кДж/моль
- Энтальпия кипения ΔHкип: 29,1 кДж/моль
- Теплота сгорания Qp: 1829,4 кДж/моль
- Критическое давление: 4,7 МПа
- Критическая плотность: 0,273 г/см3
- Динамическая вязкость жидкостей и газов:
- 0,36 мПа·с (10 °C)
- 0,295 мПа·с (25 °C)
- 0,28 мПа·с (41 °C)
Термохимические свойства:
- Температура вспышки в воздухе: (-20 °C)
- Температура самовоспламенения на воздухе: 465 °C
- Пределы взрывоопасных концентраций: 2,6-12,8 %
Оптические свойства:
- Показатель преломления (для D-линии натрия):
- 1,3591 (20 °C)
- 1,3588 (25 °C)
- Показатель диссоциации: pKa = 20 (20 °C, вода)
- Диэлектрическая проницаемость (20 °C): 20,9
- Дипольный момент молекулы (20 °C): 2,84 Дебай
Ацетон хорошо растворяет многие органические вещества, в частности, ацетил- и нитроцеллюлозы, воски, алкалоиды и так далее, а также ряд солей.
Ацетон образуется при ацетоновом (ацетон-бутиловом) брожении углеводов, вызываемом Clostridium acetobutylicus. В результате образуется ацетон и бутанол-1, а также ряд побочных примесей. В качестве промышленного такой метод получения ацетона был популярен в XIX — начале XX вв., но был вытеснен технологиями химического синтеза.

Ацетон является одним из наиболее реакционноспособных кетонов. Так, он один из немногих кетонов образует бисульфитное соединение:
(CH3)2CO + NaHSO3 ⟶ (CH3)2C(OH)SO3Na
Под действием щелочей вступает в альдольную самоконденсацию, с образованием диацетонового спирта:
2(CH3)2CO →OH− (CH3)2C(OH)CH2C(O)CH3
Восстанавливается цинком до пинакона:
2(CH3)2CO →Zn (CH3)2C(OH)C(OH)(CH3)2
При пиролизе (700 °C) образует кетен:
(CH3)2CO ⟶ CH2=C=O + CH4
Легко присоединяет циановодород с образованием ацетонциангидрина:
(CH3)2CO + HCN ⟶ (CH3)2C(OH)CN
Атомы водорода в ацетоне легко замещаются на галогены. Под действием хлора (иода) в присутствии щёлочи образует хлороформ (йодоформ).
- Hal2 + 2NaOH ⟶ NaHal + NaOHal + H2O
- (CH3)2CO + 3NaOHal ⟶ CH3−CO−CHal3 + 3NaOH
- CH3−CO−CHal3+NaOH ⟶ CHHal3↓ + CH3COONa
Качественной реакцией на диметилкетон есть наличие интенсивно-красной окраски с нитропруссидом натрия в щелочной среде. При добавлении CH3COOH окраска переходит в красно-фиолетовую.
(CH3)2CO + Na2[Fe(CN)5NO] + 2NaOH ⟶ Na4[Fe(CN)5ON=CHCOCH3] + 2H2O
Получение
Мировое производство ацетона составляет более 6,9 миллионов тонн в год (по данным на 2012 г.) и устойчиво растёт.
В промышленности получается напрямую или косвенно из пропена.
Кумольный способ
Основную часть ацетона получают как сопродукт при получении фенола из бензола по кумольному способу. Процесс протекает в 3 стадии.
На первой стадии бензол алкилируется пропеном с получением кумола, на второй и третьей (реакция Удриса — Сергеева) полученный кумол окисляется кислородом воздуха до гидропероксида, который при действии серной кислоты разлагается на фенол и ацетон:
C6H6 + CH3CH=CH2 ⟶ C6H5CH(CH3)2C6H5CH(CH3)2 + O2 ⟶ C6H5C(OOH)(CH3)2C6H5C(OOH)(CH3)2 ⟶ C6H5OH + (CH3)2COИз изопропанола
По данному методу изопропанол окисляют в паровой фазе при температурах 450—650 °C на катализаторе (металлические медь, серебро, никель, платина). Ацетон с высоким выходом (до 90 %) получают на катализаторе «серебро на пемзе» или на серебряной сетке:
(CH3)2CH-OH + O2 ⟶ (CH3)2CO + H2O2Метод окисления пропена
Ацетон получают также прямым окислением пропена в жидкой фазе в присутствии PdCl2 в среде растворов солей Pd, Cu, Fe при температуре 50-120 °C и давлении 50-100 атм:
CH3CH=CH2 + PdCl2 + H2O ⟶ (CH3)2CO + Pd + 2HCl2Pd + 4HCl + O2 ⟶ 2PdCl2 + 2H2O
Некоторое значение имеет метод брожения крахмала под действием бактерий Clostridium acetobutylicum с образованием ацетона и бутанола. Метод характеризуется малыми выходами. Используются также методы получения из изопропилового спирта и ацетилена.

Применение
Ацетон применяется как сырьё для синтеза многих важных химических продуктов, таких как уксусный ангидрид, кетен, диацетоновый спирт, окись мезитила, метилизобутилкетон, метилметакрилат, дифенилпропан, изофорон, бисфенол А и так далее; пример:
(CH3)2CO + 2C6H5OH ⟶ (CH3)2C(C6H4OH)2
Последний широко применяется при синтезе поликарбонатов, полиуретанов и эпоксидных смол.
Ацетон также является популярным растворителем. В частности он используется как растворитель
- в производстве лаков;
- в производстве взрывчатых веществ;
- в производстве лекарственных препаратов;
- в составе клея для киноплёнок как растворитель ацетата целлюлозы и целлулоида;
- компонент для очистки поверхностей в различных производственных процессах;
- как очиститель инструмента и поверхностей от монтажной пены — в аэрозольных баллонах.
Без ацетона невозможно хранить в компактном (сжиженном и в баллоне) состоянии ацетилен, который под давлением в чистом виде крайне взрывоопасен. Для этого используют ёмкости с пористым материалом, пропитанным ацетоном. 1 литр ацетона растворяет до 250 литров ацетилена.
Ацетон используется также при экстракции многих растительных веществ.
Ацетон служит также сырьём для синтеза уксусного ангидрида, кетена, диацетонового спирта и многих других соединений.
Лабораторное применение
В органической химии ацетон применяется в качестве полярного апротонного растворителя, в частности, в реакции алкилирования
ArOH + RCl + K2CO3 ⟶ ArOR + KCl + KHCO3
для окисления спиртов в присутствии алкоголятов алюминия по Оппенауэру
RR′CH-OH + (CH3)2CO ⟶ RR′CO + (CH3)2CH-OH
- Ацетон применяется для приготовления охлаждающих бань в смеси с «сухим льдом» и жидким аммиаком (охлаждает до температуры −78 °C).
- В лабораториях используется для мытья химической посуды благодаря низкой цене, малой токсичности, высокой летучести и лёгкой растворимости в воде, а также для быстрой сушки посуды и неорганических веществ.
- Для очистки в лабораторных условиях ацетон перегоняют в присутствии небольшого количества перманганата калия (до слабо-розовой окраски раствора).
Обнаружение
- В химико-токсикологическом анализе для обнаружения ацетона применяют реакции с растворами йода, нитропруссида натрия, фурфурола, ο-нитробензальдегида и метод микродиффузии.
- Реакция на образование йодоформа.
- При взаимодействии ацетона с раствором йода в щелочной среде образуется трииодметан (йодоформ):
I2 + 2OH− ⟶ IO− + I− + H2O3IO− + CH3COCH3 ⟶ I3C-CO-CH3 + 3OH−I3C-CO-CH3 + OH− ⟶ CHI3 + CH3COO−
К 1 мл исследуемого раствора прибавляют 1 мл 10%-го раствора аммиака и несколько капель раствора йода в йодиде калия (йодной настойки).
В присутствии йода образуется желтый осадок трииодметана с характерным запахом, а его кристаллы имеют характерную гексалучевую форму. Предел обнаружения — 0,1 мг ацетона в пробе.
Реакция с нитропруссидом натрия (проба Легаля).
Ацетон с нитропруссидом натрия в щелочной среде дает интенсивно-красную окраску. При подкислении уксусной кислотой окраска переходит в красно-фиолетовую.
Кетоны, в молекулах которых отсутствуют метильные группы, непосредственно связанные с кетоновыми (СО—) группами, не дают такой реакции.
Соответственно такие кетоны как метилэтилкетон, метилпропилкетон и другие — также дадут красную окраску с нитропруссидом.
CH3COCH3 + Na2[Fe(CN)5NO] + 2NaOH ⟶ Na4[Fe(CN)5ON=CHCOCH3] + 2H2O
К 1 мл исследуемого раствора прибавляют 1 мл 10%-го раствора гидроксида натрия и 5 капель 1%-го свежеприготовленного раствора нитропруссида натрия. При наличии ацетона в пробе появляется красная или оранжево-красная окраска.
При прибавлении 10%-го раствора уксусной кислоты до кислой реакции через несколько минут окраска переходит в красно-фиолетовую или вишнёво-красную. Следует заметить, что бутанон дает аналогичную окраску с нитропруссидом натрия.

Пожароопасность
Одна из основных опасностей при работе с ацетоном — его легковоспламеняемость. Температура самовоспламенения +465 °C, температура вспышки −20 °C.
Воздушные смеси, содержащие от 2,5 % до 12,8 % (по объёму), взрывоопасны.
С этим необходимо считаться, так как ацетон быстро испаряется, и образующееся облако может распространиться до места воспламенения (нагрев или искра) вдали от места работы с ним.
Метаболизм и токсикология
Ацетон является естественным метаболитом, производимым организмами млекопитающих, в том числе и человеческим организмом.
Некоторое количество вещества выводится с выдыхаемым воздухом и выделениями кожи, некоторое — с мочой. В медицине ацетон относят к кетоновым телам.
Нарушение нормального метаболизма, например, при сахарном диабете, приводит к так называемой ацетонурии — избыточному образованию и выведению ацетона.
В крови в норме содержится 1-2 мг/100 мл ацетона, в суточном количестве мочи — 0,01-0,03 г. При нарушениях обмена веществ, например, при сахарном диабете, в моче и крови повышается содержание ацетона.
Незначительная часть ацетона превращается в оксид углерода (IV), который выделяется с выдыхаемым воздухом.
Некоторое количество ацетона выделяется из организма в неизменном виде с выдыхаемым воздухом и через кожу, а некоторое — с мочой.
Ацетон ядовит, но относится к малоопасным веществам (класс опасности IV, категория безопасности для здоровья по NFPA — 1). Сильно раздражает слизистые оболочки: длительное вдыхание больших концентраций паров приводит к возникновению воспаления слизистых оболочек, отёку лёгких и токсической пневмонии.
Пары оказывают слабое наркотическое действие, сопровождаемое, чаще всего, дисфорией.
При попадании внутрь вызывает состояние опьянения, сопровождаемое слабостью и головокружением, нередко — болями в животе; в существенных количествах возникает выраженная интоксикация, хотя, как правило, отравления ацетоном не смертельны.
Возможно поражение печени (токсический гепатит), почек (уменьшение диуреза, появление крови и белка в моче) и коматозное состояние. При ингаляционном воздействии ацетон выводится гораздо медленнее (в течение нескольких часов), чем поступает, и поэтому может накапливаться в организме.
Источник: https://chem.ru/aceton.html
ацетон
Алф. указатель: 1-9 A-Z А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Щ Э Я
диметилкетон пропанон бесцветн. жидкость 56,05 °C (температура кипения азеотропа, давление 1 атм) аллилбромид 8% ацетон 92% ацетон: смешивается бензол: смешивается вода: смешивается диэтиловый эфир: смешивается метанол: смешивается хлороформ: растворим этанол: смешивается Источник информации: Гитис С.С., Глаз А.И., Иванов А.В. «Практикум по органической химии: Органический синтез» М.: Высшая школа, 1991 стр. 49
Для высушивания ацетон помещают в колбу с обратным холодильником, закрытым хлоркальциевой трубкой, добавляют безводный хлорид кальция (120 г на 1 л) и кипятят, дважды заменяя осушитель через каждые 5-6 часов. Переливать ацетон на свежий осушитель следует как можно быстрее, так как ацетон очень жадно поглощает влагу. Окончательно ацетон перегоняют над хлоридом кальция.
Плотность:
0,7908 (20°C, г/см3) 0,7899 (25°C, г/см3)
Показатель преломления (для D-линии натрия):
1,3591 (20°C) 1,3588 (25°C) pKa (1) = 20 (20 C, вода) 20,9 (20°C) 2,84 (20°C) 0,295 (25°C) 0,28 (41°C) 0,36 (10°C) 23,7 (20°C) -247,7 (ж) 200 (ж) 125 (ж) 5,69 29,1 -18 465 1829,4 -216,5 (г)
Клиническая картина отравления: При попадании внутрь и вдыхании паров — состояние опьянения, головокружение, слабость, шаткая походка, тошнота, боли в животе, коллапс, коматозное состояние. Возможны поражения печени (токсический гепатит) и почек (снижение диуреза, появление белка и эритроцитов в моче). При выходе из коматозного состояния часто развивается пневмония.
Лечение: При пероральном приеме — промывание желудка, при ингаляционном — промывание глаз водой, ингаляция кислорода. Ощелачивание мочи. Форсированный диурез. Лечение острой сердечно-сосудистой недостаточности, нефропатии, пневмонии.
Аналитические
Критическая температура (в °C):
235,5
Критическое давление (в МПа):
4,7
Критическая плотность (в г/см3):
0,273
Применение:
Широко применяемый растворитель органических веществ, в первую очередь нитратов и ацетатов целлюлозы. Сырье для синтеза уксусного ангидрида, кетена, диацетонового спирта, окиси мезитила, метилизобутилкетона, метилметакрилата, дифенилолпропана, изофорона и многих других соединений.
Мировое производство около 3 000 000 т/год (1980).
История:
Название от латинского acetum — уксус.
Дополнительная информация:
Входит в список IV (прекурсоры) наркотических и психотропных веществ.
Образует кристаллические соединения с гидросульфитами щелочных металлов. Сильными окислителями (щелочной раствор перманганата калия или хромовая кислота) окисляется до муравьиной и уксусной кислот и далее до углекислого газа и воды.
Каталитически восстанавливается до изопропанола; амальгамами магния и цинка, а также цинком в уксусной кислоте — до пинакона. Атомы водорода легко замещаются при галогенировании, нитрозировании. Действием хлора в щелочи превращается в хлороформ, который взаимодействует с избытком ацетона с образованием хлорэтона.
Окисляет вторичные спирты в присутствии алкоголятов алюминия до кетонов (реакция Оппенгауэра). Вступает в альдольную конденсацию с образованием диацетонового спирта, а также в кротоновую конденсацию с образованием окиси мезитила, форона и мезитилена.
В присутствии сильной минеральной кислоты алкилирует фенол с образованием дифенилолпропана. Присоединяет цианид-ион с образованием ацетонциангидрина. При пиролизе (700 С) дает кетен и метан.
- «Неотложная помощь при острых отравлениях: Справочник по токсикологии» под ред. Голикова С.Н. М.:Медицина, 1977 стр. 261
- «Химическая энциклопедия» т.1 М.: Советская энциклопедия, 1988 стр. 230-231
- Бабаян Э.А., Гаевский А.В., Бардин Е.В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: МЦФЭР, 2000 стр. 147
- Гордон А., Форд Р. «Спутник химика» М.: Мир, 1976 стр. 186
- Рабинович В.А., Хавин З.Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 127
Алф. указатель: 1-9 A-Z А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Щ Э Я
Еще по теме:
- АЦЕТОН — химическая энциклопедия
- Ацетон — Токсикологическая химия

Источник: http://www.xumuk.ru/spravochnik/27.html
Ацетилацетон
Главная → Продукция → Химическое сырье и реактивы → Химреактивы полный перечень → Ацетилацетон
Описание
Цена
 Ацетилацетон (диацетилметан, пентан-2,4-дион) СН3-СО-СН2-СО-СН3 — органическое соединение, относящееся к классу кетонов с формулой C5H8O2. Этот дикетон имеет формальное название 2,4-пентандион. Он является прекурсором для синтеза ацетилацетонатов (асас), распространенный бидентантный лиганд. Также является билдинг блоком для синтеза гетероциклических соединений.
Ацетилацетон (диацетилметан, пентан-2,4-дион) СН3-СО-СН2-СО-СН3 — органическое соединение, относящееся к классу кетонов с формулой C5H8O2. Этот дикетон имеет формальное название 2,4-пентандион. Он является прекурсором для синтеза ацетилацетонатов (асас), распространенный бидентантный лиганд. Также является билдинг блоком для синтеза гетероциклических соединений.
Физические свойства
- Бесцветная жидкость с запахом ацетона и уксусной кислоты.
- Кето и енольная форма ацетилацетона сосуществуют в растворе; эти формы являются таутомерами. C2v симметрия для енола показанного на левой части схема была проверена разными методами в том числе и микроволновой спектроскопией. Водородная связь в еноле уменьшает стерическое отталкивание между карбонильными группами. В газовой фазе К, точнее её отрицательный логарифм pKa равен 11,7. Константа равновесия стремится к увеличению в неполярных растворителях: циклогексан — 42, толуол — 10, ТГФ 7.2, ДМСО (рK=2), и в воде (рK=0.23).Енольная форма является винилогическим аналогом карбоксильной кислоты.
Получение
- Ацетилацетон получается индустриально термической перегруппировкой изопропенил ацетата.
CH2C(CH3)OC(O)Me → MeC(O)CH2C(O)Me
- Лабораторные пути к ацетилацетону начинаются на ацетоне. Ацетон и уксусный ангидрид при добавке BF3 в качестве катализатора:
(CH3CO)2O + CH3C(O)CH3 → CH3C(O)CH2C(O)CH3
- Второй синтез включает катализируемая основаниями конденсация ацетона и этилацетата, с последующим подкислением.
NaOEt + EtO2CCH3 + CH3C(O)CH3 → NaCH3C(O)CHC(O)CH3 + 2 EtOH
NaCH3C(O)CHC(O)CH3 + HCl → CH3C(O)CH2C(O)CH3 + NaCl
- Благодаря лёгкости этих синтезов известно много аналогов ацетилацетонатов. Некоторые примеры включают C6H5C(O)CH2C(O)C6H5 (dbaH) (CH3)3CC(O)CH2C(O)CC(CH3)3. Гексафторацетилацетонаты (F3CC(O)CH2C(O)CF3) широко используются для получения летучих комплексов металлов.
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 100,13 г/моль |
| Плотность | 0,98 г/см³ |
| Термические свойства | |
| Т. плав. | -23 °C |
| Т. кип. | 140 °C |
| Т. всп. | 34 °C |
| Т. свспл. | 340 °C |
| Давление пара | 9 гПа |
| Химические свойства | |
| pKa | 9 |
| Растворимостьв воде | 16 г/100 мл |
| Растворимость в орг. растворители | смешивается |
| Оптические свойства | |
| Показатель преломления | 1,4609 |
| Скачать прайс-лист | в PDF формате |
| Ацетилацетон |
Источник: http://www.lab.kh.ua/products/sewerage/ximreaktivy-polnyj-perechen/acetilaceton
Ацетон — это… Что такое Ацетон?
Ацето́н (диметилкето́н, систематическое наименование: пропан-2-о́н) — простейший представитель кетонов. Формула: CH3-C(O)-CH3. Бесцветная легкоподвижная летучая жидкость с характерным запахом.
Полностью смешивается с водой и большинством органических растворителей. Ацетон хорошо растворяет многие органические вещества (ацетилцеллюлозу и нитроцеллюлозу, воск, резину и др.), а также ряд солей (хлорид кальция, иодид калия).
Является одним из метаболитов, производимых человеческим организмом.
Получение
Мировое производство ацетона составляет более 6,9 миллионов тонн в год (по данным на 2012 г.[1]) и устойчиво растёт.[1]
В промышленности
В промышленности получается напрямую или косвенно из пропена.
Основную часть ацетона получают как сопродукт при получении фенола из бензола по кумольному способу, заключающемуся в следующих трёх этапах:[2]
- Бензол алкилируется пропеном с получением кумола
C6H6+ CH3CH=CH2 → C6H5CH(CH3)2Следующие два этапа известны как реакция Удриса-Сергеева
- Полученный кумол окисляется кислородом воздуха до гидропероксида
C6H5CH(CH3)2 + O2 → C6H5C(OOH)(CH3)2 - Гидропероксид разлагается в присутствии серной кислоты на фенол и ацетон
C6H5C(OOH)(CH3)2 → C6H5OH + OC(CH3)2
- Прямым окислением пропена в жидкой фазе в присутствии PdCl2 в среде растворов солей Pd, Cu, Fe при температуре 50-120 °C и давлении 50-100 атм:
- CH3CH=CH2 + PdCl2 + H2O → CH3C(O)CH3 + Pd + 2HCl
- Pd+2HCl + 0.5O2 → PdCl2 + H2O
Некоторое значение имеет метод брожения крахмала под действием бактерий Clostridium acetobutylicum с образованием ацетона и бутанола[3]. Метод характеризуется малыми выходами. Используются также методы получения из изопропилового спирта и ацетилена.
Химические свойства
- Ацетон является одним из наиболее реакционноспособных кетонов. Так, он один из немногих кетонов образует бисульфитное соединение
- CH3C(O)CH3 + NaHSO3 → (CH3)2C(OH)-SO3Na
- Вступает в альдольную самоконденсацию под действием щелочей, с образованием диацетонового спирта.
- 2CH3C(O)CH3 → (CH3)2C(OH)CH2C(O)CH3
- Восстанавливается цинком до пинакон.
- 2CH3C(O)CH3 + Zn → (CH3)2C(OH)C(OH)(CH3)2
- При пиролизе (700 °C) образует кетен.
- CH3C(O)CH3 → CH2=C=O + 2H2
- Легко присоединяет циановодород с образованием ацетонциангидрина.
- CH3C(O)CH3 + HCN → (CH3)2C(OH)CN
Атомы водорода в ацетоне легко замещаются на галогены.
Под действием хлора (иода) в присутствии щёлочи образует хлороформ (йодоформ).
Ацетон, как и другие кетоны, в щелочной среде способен изомерироваться в пропаналь, последний — до пропенового спирта. В кислой среде и в присутствии ионов двухвалентной ртути, пропеновый спирт изомерируется сразу в ацетон. Между этими веществами всегда существует таутомерное равновесие:
CH3C(O)CH3 ↔ С2Н5СОН ↔ СН2=С(ОН)-СН3
Диметилкетон
Биохимия
В крови в норме содержится 1-2 мг/100 мл ацетона, в суточном количестве мочи — 0,01-0,03 г. При нарушениях обмена веществ, например, при сахарном диабете, в моче и крови повышается содержание ацетона.
Незначительная часть ацетона превращается в оксид углерода (IV), который выделяется с выдыхаемым воздухом.
Некоторое количество ацетона выделяется из организма в неизменном виде с выдыхаемым воздухом и через кожу, а некоторое — с мочой.
Применение
Ацетон применяется как сырьё для синтеза многих важных химических продуктов, таких как уксусный ангидрид, кетен, диацетоновый спирт, окись мезитила, метилизобутилкетон, метилметакрилат, дифенилпропан, изофорон, бисфенол А и др.; пример:
(CH3)2CO + 2 C6H5OH → (CH3)2C(C6H4OH)2 + H2O.
Последний широко применяется при синтезе поликарбонатов, полиуретанов и эпоксидных смол.
Ацетон также является популярным растворителем, значительно превосходящим в плане безопасности бензин, скипидар и отчасти керосин. В частности как растворитель используется он:
Без ацетона невозможно хранить в компактном (сжиженном и в баллоне) состоянии ацетилен, который не может храниться под давлением в чистом виде из-за опасности взрыва. Для этого используют ёмкости с пористым материалом, пропитанные ацетоном. 1 литр ацетона растворяет до 250 литров ацетилена.
Лабораторное применение
В органической химии ацетон применяется в качестве полярного апротонного растворителя, в частности в реакции алкилирования
ArOH + RHal + K2CO3 → ArOR + KHal + KHCO3,
для окисления спиртов в присутствии алкоголятов алюминия по Оппенауэру
RR`CHOH + CH3C(O)CH3 → RR`C=O + CH3CH(OH)CH3,
- Также незаменим для приготовления охлаждающих бань в смеси с «сухим льдом» и жидким аммиаком (охлаждает до температуры −78 °C).
- Очень полезен для мытья химической посуды, благодаря низкой цене, малой токсичности, высокой летучести и лёгкой растворимости в воде, а также для быстрой сушки посуды и неорганических веществ.
- Для очистки в лабораторных условиях ацетон перегоняют в присутствии небольшого количества перманганата калия (до слабо-розовой окраски раствора).
Безопасность
Пожароопасность =
Одна из основных опасностей при работе с ацетоном — его легковоспламеняемость. Температура воспламенения +465 °C, температура замерзания ~+ −20 °C.
Воздушные смеси, содержащие от 2,5 % до 12,8 % (по объёму) взрывоопасны.
С этим необходимо считаться, так как ацетон быстро испаряется, и образующееся облако может распространиться до места воспламенения (нагрев или искра) вдали от места работы с ним.
Токсичность
Считается, что ацетон малотоксичен, также считается, что он не вызывает хронических болезней при использовании основных методов предосторожностей при работе с ним.
Ацетон обладает возбуждающим и наркотическим действием (что особенно хорошо проявляется при хроническом воздействии на людей, часто работающих с ацетоном как с растворителем), поражает центральную нервную систему, способен накапливаться в организме[источник не указан 64 дня], в связи с чем токсическое действие зависит не только от его концентрации, но и от времени воздействия на организм. ЛД50 для мышей при вдыхании в течение 4-х часов — 44 г/м³. Для человека ЛД50 оценивается в 1,159 г/кг. ПДК 200 мг/м³.
Ацетон при высоких концентрациях (при более чем кратковременном воздействии) раздражает органы дыхания и вызывает жжение в глазах, при более длительном воздействии происходит кратковременный глазной отёк. Вероятно, способен вызывать головокружение, тошноту и дезориентацию при воздействии паров высоких концентраций.
Экология
Из-за высокой летучести, значительная часть ацетона испаряется в атмосферу, где период полураспада под действием ультрафиолета составляет 22 дня. ЛД50 для рыб 8,3 г/л в течение 96 часов, а период полураспада в данной среде от 1 до 10 суток. Ацетон может вызывать значительное понижение уровня кислорода в воде из-за потребления его микроорганизмами.[источник не указан 64 дня]
Однако ацетон в небольших концентрациях, быстро поглощается рядом бактерий, использующих его в качестве питательной среды.
Примечания
Источник: https://dic.academic.ru/dic.nsf/ruwiki/795100
Карбонильная группа. Альдегиды и кетоны
Слово альдегид было придумано как сокращение латинского alcohol dehydrogenatus — дегидрированный спирт, самый популярный альдегид — формальдегид, из него делают смолы, синтезируют лекарства и как консервант. Формула альдегида — R-CHO, соединение, в котором карбонильная группа соединена с водородом и радикалом.
Слово кетон произошло от слова ацетон, младшего соединения из семейства кетонов. Кетоны используются как растворители, лекарства и для синтеза полимеров. Формула кетона — R-C(O)-R, соединение, в котором карбонильная группа соединена с двумя радикалами.
Структура и свойства карбонильной группы
Карбонильная группа основана на связи атома углерода и атома кислорода посредством α- и π-связей.
Резонансная структура группы определяет высокую полярность соединения и электронное облако сдвинуто в сторону кислорода: Cδ+=Oδ-.
Введение электроотрицательных элементов в уменьшает полярность связи, повышая положительный заряд молекулы. Нуклеофильные заместители увеличивают отрицательный заряд кислорода.
Атом углерода в карбонильной группе является сильным электрофилом (присоединяет электроны), поэтому большинство реакций альдегидов и кетонов осуществляется нуклеофильными реактивами (основания Льюиса). Логично, атом кислорода является сильным нуклеофилом, и реакции с атомом кислорода возможны с применением электрофилов (кислот Льюиса).
Реакция карбонильной группы с основанием Льюиса (R)(R)Cδ+=Oδ- + B: → (R)(R)C(B)-O Реакция карбонильной группы с кислотой Льюиса (R)(R)Cδ+=Oδ- + Y: → (R)(R)C-O-Y
В дополнение, неразделённые электроны кислорода наделяют его слабыми свойствами основания, поэтому те альдегиды и цетоны, которые не растворяются в воде, растворяются в концентрированной серной кислоте.
Физические свойства карбонильной группы
Высокая полярность связи C=O образует высокий дипольный момент, из-за чего носители карбоксильной группы имеют более высокую температуру кипения, по сравнению с углеводородами.
Неразделённые электроны в атоме кислорода образуют водородную связь с молекулами воды, поэтому, начиная с пяти атомов углерода в радикалах, альдегиды и кетоны плохо растворяются в воде или не растворяются вовсе.
Альдегиды и кетоны, имеющие до 12 атомов углерода — жидкости. Алифатические соединения с карбонильной группой имеют плотность примерно 0.8, поэтому плавают на поверхности воды, циклогексанон имеет плотность около единицы, ароматические альдегиды и кетоны имеют плотность чуть больше, чем плотность воды.
Реакции альдегидов и кетонов
Присоединение воды
В процессе реакции воды с альдегидами и кетонами образуются диолы (гликоли, двухатомные спирты). Реакция протекает с использованием катализатора — кислотой или основанием и является двусторонней:
RR-CO + H-OH ↔ RRC/OH-OH
Присоединение нуклеофильных углеродов
Важные нуклеофильные соединения, реагирующие с альдегидами и кетонами — металлорганические соеденинения (органические соединения, в молекулах которых существует связь атома металла с атомом/атомами углерода). Одни из представителей металлорганических соединений — реактивы Гриньяра (общая формула — R-Mg-X), в реакциях с альдегидами и кетонами образуют спирты:
RH-C=O + R-C-H2-Mg+-Cl- → RH-С-(O-MgCl)(CH2-R) RH-С-(O-MgCl)(CH2-R) + H-OH → RH-C-CH2R + OH-Mg-Cl
Окисление альдегидов и кетонов
При окислении, альдегиды находятся на промежуточном этапе между спиртами и карбоновыми кислотами:
В присутствии водорода и кислорода: R-CH2-OH ↔ R-C(=O)-H ↔ R-COOH
Альдегиды легко окисляются, что позволяет использовать более мягкие окислители, чем простой кислород. Ароматические альдегиды подвергаются окислению легче, чем алифатические. Проблема окисления альдегидов — в образовании побочных продуктов.
Кетоны окисляются с трудом, для окисления кетонов необходимо использовать сильные окислители и большое количество тепла. В результате окисления разрывается связь C-C и образовывается кислота (есть исключение):
В присутствии KMnO4, H и большого количества тепла: CH3-C(=O)-CH2CH3 → CH3-C(=O)-OH + CH3CH2-C(=O)-OH
Исключением является окисление диоксидом селена, SeO2, метил-группа, следующая за карбонильной, окисляется, преобразовываясь в другую карбонильную группу. Например, метилэтилкетон окисляется в диацетил:
Окисление метилэтилкетона в диацетил: CH3CH2-C(=O)-CH3 + SeO2 → CH3-C(=O)-C(=O)-CH3 + H2O + Se
Лёгкость, с которой окисляются альдегиды, позволяет легко отличить их от кетонов, для этого используются мягкие окислители, такие как: реактив Толленса (гидроксид диамминсеребра, Ag(NH3)2OH), реактив Фелинга (алкалиновый раствор ионов меди Cu в Сегнетовой соли KNaC4H6O6·4H2O) и раствор Бенедикта (ионы меди с цитратом и карбонатом натрия). Ароматические альдегиды реагируют с реактивом Толленса, но не реагируют с реактивами Бенедикта и Фелинга, что используется для определения количества алифатических и ароматных альдегидов.
Полимеризация альдегидов
Паральдегид
Ацетальдегид имеет температуру кипения 20°C, что затрудняет его хранение и применение. При обработке ацетальдегида кислотой при низкой температуре, ацетальдегид соединяется в цикличную тройную молекулу — паральдегид, с температурой кипения 120°C. Паральдегид при небольшом нагреве деполимеризуется, высвобождая три молекулы ацетальдегида.
Формальдегид
Для удобства транспортировки и хранения, формальдегид продаётся не в форме газа, а в виде формалина — водного раствора с содержанием 37-40% параформальдегида, OH(CH2O)nH, со средним значением n=30.
Параформальдегид — белое аморфное вещество, твёрдое, получаемое медленным выпариванием формалина при низком давлении.
Полимеризация происходит за счёт присоединения друг к другу молекул формальдегида:
CH2=O + H2O ↔ [HOCH2OH] [HOCH2OH] + n[HCHO] → HO-(CH2O)n+1-H
Полимер Дерлин (полиоксиметилен) является хорошим линейным пластиком с высокой молекулярной массой, дерлин обладает отличными характеристиками прочности и эластичности.
Нажмите на молекулу в списке и 3D-модель появится в чёрном окне
Источник: https://k-tree.ru/articles/himiya/organicheskaya_himiya/karbonilnaya_gruppa
Бутанон
Бутанон
C4H8O
Метилэтилкетон (систематическое наименование: бутанон) — химическое соединение класса кетонов, второй член гомологического ряда алифатических кетонов. Формула: CH3-C(O)-CH2-CH3.
Это бесцветная подвижная легколетучая жидкость с запахом, напоминающим запах ацетона.
Обладает всеми химическими свойствами, характерными для алифатических кетонов, используется как растворитель и сырьё в органическом синтезе
Метилэтилкетон ( Бутанон) — это химическое соединение класса кетонов, бесцветная легколетучая жидкость с запахом, напоминающим запах ацетона. Метилэтилкетон обладает всеми химическими свойствами, характерными для алифатических кетонов, используется как растворитель и сырьё в органическом синтезе.
Физические свойства метилэтилкетона:
С водой смешивается ограниченно, в любых пропорциях смешивается с большинством органических растворителей. Образует азеотропную смесь с водой (Ткип. 73,41 °С; 88,7 % по массе метилэтилкетона). Температура всп. −2,2 °C, КПВ 1,97-10,2 %. Взрывоопасен в смеси с воздухом при концентрации 1,97-10,2 %.
Применение метилэтилкетона
Метилэтилкетон применяется как растворитель перхлорвиниловых, нитроцеллюлозных, полиакриловых лакокрасочных материалов и клеев, типографских красок, депарафинизации смазочных масел и обезмасливания парафинов (удаление смеси масла и низкоплавкого парафина); промежуточный продукт в производстве пероксида метилэтилкетона (отвердитель полиэфирных смол), втор-бутиламина и др. Также применяется для производства чернил и разбавителя при каплеструйной технологии печати при использовании каплеструйных принтеров для маркировки продукции (дата произ-ва, срок годности, партия и т.д). Является прекурсором, требует наличия соответствующей лицензии на использование, хранение и закупку.
Сфера применения метилэтилкетона (бутанона) тем или иным образом связана с лакокрасочной или химической промышленностью. В первой он используется в виде растворителя соединений с перхлорвинилом, нитроцеллюлозой, им разбавляют полиакриловыми лакокрасочными материалы и клея, типографские краски.
Пожарная опасность:
Относят к легко воспламяняющимся веществам, Температура вспышки: -2,2 град.С, КПВ 1,97-10,2%.
Взрывоопасен в смеси с воздухом при концентрации 1,97-10,2 %. При температуре выше -9°C могут образоваться взрывоопасные смеси пар/воздух. е допускать открытого огня, искр и курения.
Пар тяжелее воздуха и может стелиться по земле; возможно возгорание на расстоянии.
Реагирует бурно с сильными окислителями и неорганическими кислотами с опасностью пожара и взрыва. Агрессивно в отношении некоторых пластиков.
Источник: http://himmax.ru/index.php/produktsiya/30-reaktivy/4629-butanon




