Презентацию на тему «Структура ячейки на примере атома железа» можно скачать абсолютно бесплатно на нашем сайте. Предмет проекта: Химия.
Красочные слайды и иллюстрации помогут вам заинтересовать своих одноклассников или аудиторию.
Для просмотра содержимого воспользуйтесь плеером, или если вы хотите скачать доклад — нажмите на соответствующий текст под плеером. Презентация содержит 30 слайд(ов).
 Слайд 1
Слайд 1
- Структура ячейки на примере атома железа
- Обозначение элемента
- Порядковый номер элемента
- Относительная атомная масса (Аr)
- Название элемента
 Слайд 2
Слайд 2
Периоды Группы 1 3 4 5 6 7 I II III IV V VII VIII VI малые большие А Б
 Слайд 3
Слайд 3
Условная граница от бора до астата.
Бор Кремний Мышьяк Теллур Астат Металлы Неметаллы

 Слайд 5
Слайд 5
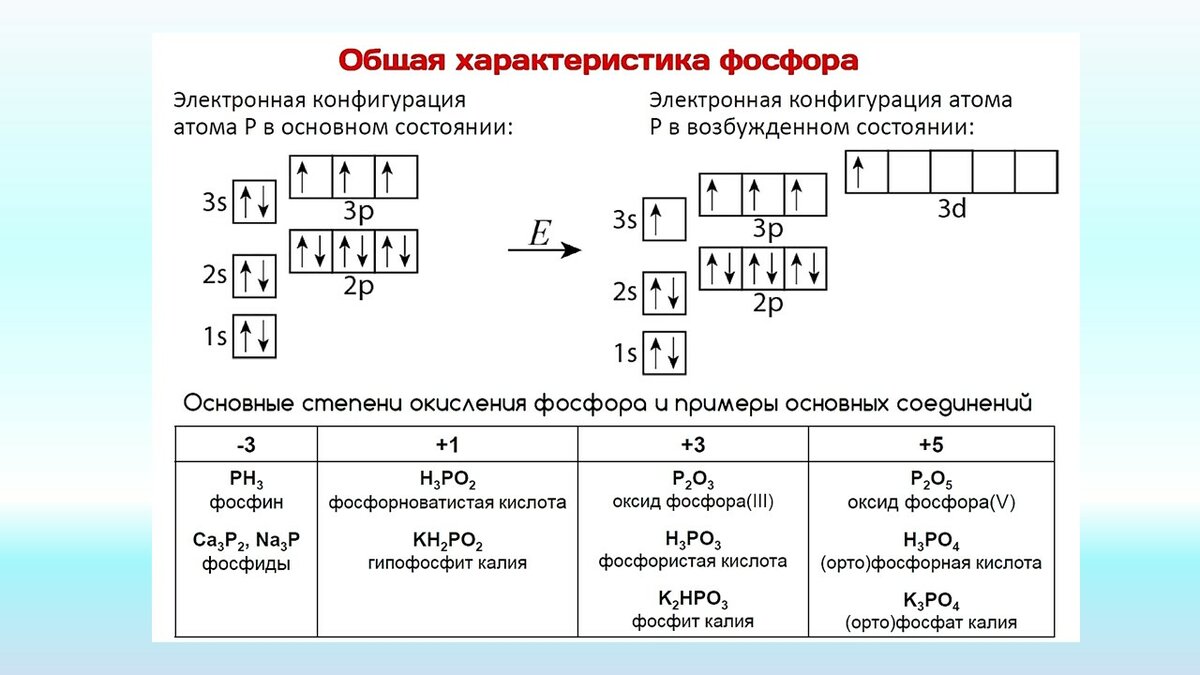
Летучие водородные соединения
 Слайд 6
Слайд 6
Металлические свойства в группах
+
 Слайд 7
Слайд 7
Металлические свойства в периодах.
 Слайд 8
Слайд 8
Неметаллические свойства в группах
 Слайд 9
Слайд 9
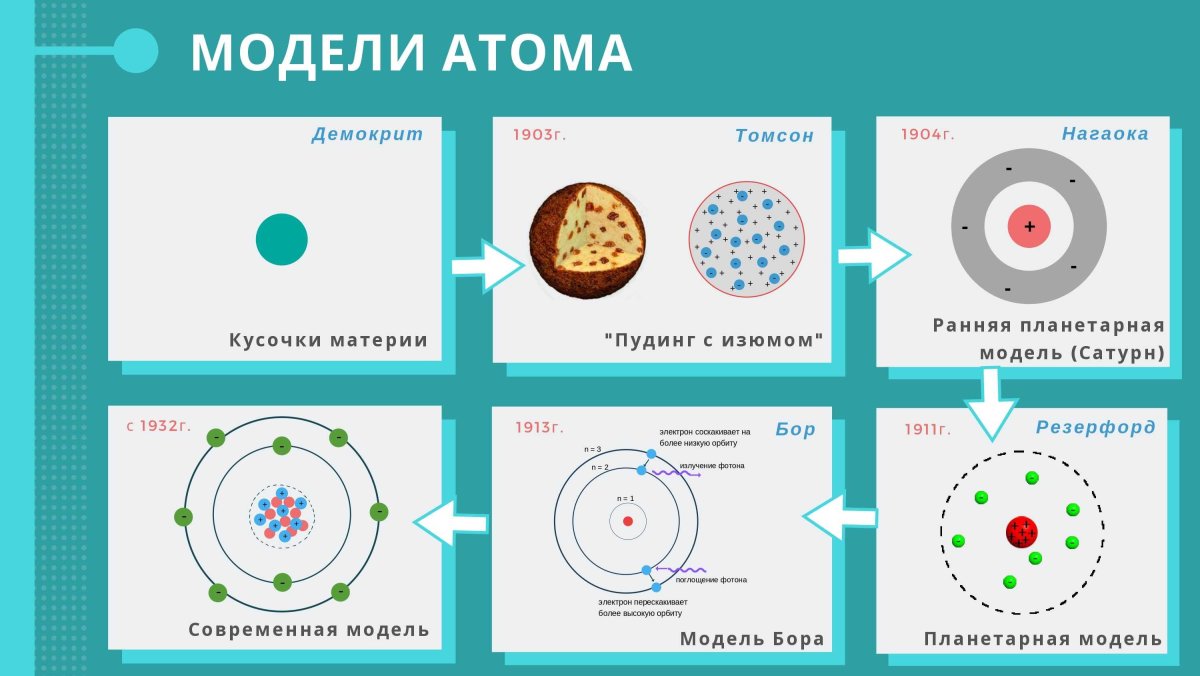
Неметаллические свойства в периодах
 Слайд 10
Слайд 10
легкие Ме НеМе другие Ве Мg 12
Слайд 16
Последний элемент, встречающийся в природе — уран. Все стоящие за ним получены искусственно в лабораториях.
Слайд 18
Щелочные металлы
элементы главной подгруппы I группы ( по новой классификации – 1 группа): литий Li, натрий Na, калий K, рубидий Rb, цезий Cs и франций Fr
Слайд 19
Щелочноземельные металлы
химические элементы 2-й группы главной подгруппы, кроме бериллия и магния: кальций Ca, стронций Sr, барий Ba и радий Ra.
Слайд 20
Переходные металлы
Переходные металлы— элементы побочных подгрупп Периодической системы химических элементов.
Слайд 21
Постпереходные металлы
вторая группа побочная подгруппа (по новой классификации 12 группа (подгруппа цинка) кроме коперниция) — цинк Zn, кадмий Cd и ртуть Hg.
Слайд 22
Легкие металлы.
металлы 3-5 период главных подгрупп: алюминий Al, галлий Ga, индий In, таллий Tl, олово Sn, свинец Pb, висмут Bi (кроме сурьмы Sb и германия Ge) + элементы 113 унунтрий, 114 унунквадий, 115 унунпентий, 116 унунгексий.
Слайд 23
Лантан + лантаноиды (лантаниды) (58-71)
семейство из 14 химических элементов III группы 6-го периода периодической таблицы. Семейство состоит из церия Ce, празеодима Pr, неодима Nd, прометия Pm, самария Sm, европия Eu, гадолиния Gd, тербия Tb, диспрозия Dy, гольмия Ho, эрбия Er, тулия Tm, иттербия Yb и лютеция Lu. Лантан La часто рассматривается вместе с этими элементами для удобства сравнения, хотя к лантаноидам он не относится
Слайд 24
Актиний + актиноиды (актиниды) (90-103)
семейство, состоящее из 14 радиоактивных химических элементов III группы 7-го периода периодической системы.
Семейство состоит из тория Th, протактиния Pa, урана U, нептуния Np, плутония Pu, америция Am, кюрия Cm, берклия Bk, калифорния Cf, эйнштейния Es, фермия Fm, менделевия Md, нобелия No и лоуренсия Lr.
Актиний Ac часто для удобства сравнения рассматривается вместе с этими элементами, однако к актиноидам он не относится.
Слайд 25
Редкоземельные металлы
группа из 17 элементов, включающая лантан La, скандий Sc, иттрий Y и лантаноиды.
Слайд 26
Благородные металлы
металлы, не подверженные коррозии и окислению, что отличает их от большинства металлов. Все они являются также драгоценными металлами, благодаря их редкости. Основные благородные металлы — золото Au, серебро Ag, а также платина Pt и остальные 5 металлов платиновой группы — (рутений Ru, родий Rh, палладий Pt, осмий Os, иридий Ir).
Слайд 27
Платиновые металлы (платиноиды)
платина Pt и остальные 5 металлов платиновой группы — (рутений Ru, родий Rh, палладий Pt, осмий Os, иридий Ir). Иногда, металлы платиновой группы подразделяют на две триады: рутений Ru, родий Rh и палладий Pd — лёгкие платиновые металлы, а платина Pt, иридий Ir и осмий Os— тяжёлые платиновые металлы.
Слайд 28
Галогены
химические элементы главной подгруппы VII группы (по новой классификации 17-й группы) периодической таблицы химических элементов : фтор F, хлор Cl, бром Br, йод I, астат At, 117 элемент унунсептий.
Слайд 29
Инертные газы
химические элементы главной подгруппы VIII группы ( по новой классификации18-й группы) периодической таблицы химических элементов. В группу входят гелий He, неон Ne, аргон Ar, криптон Kr, ксенон Xe, радон Rn, 118 элемент унуноктий.
Слайд 30
Полуметаллы (металлоиды)
химические элементы, расположенные в периодической системе на границе между металлами и неметаллами : германий Ge, сурьма Sb, полоний Po (металлы) и бор В, кремний Si, мышьяк As, теллур Te (неметаллы).
Источник: https://prezentacii.org/prezentacii/prezentacii-po-himiy/128837-struktura-jachejki-na-primere-atoma-zheleza.html
Индий In
Индий в таблице менделеева занимает 49 место, в 5 периоде.
| Символ | In |
| Номер | 49 |
| Атомный вес | 114.8180000 |
| Латинское название | Indium |
| Русское название | Индий |
Как самостоятельно построить электронную конфигурацию? Ответ здесь In: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p1 Короткая запись:
In: [Kr] 5s2 4d10 5p1
- Порядок заполнения оболочек атома индия (In) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
- На подуровне ‘s’ может находиться до 2 электронов, на ‘s’ — до 6, на ‘d’ — до 10 и на ‘f’ до 14
- Индий имеет 49 электронов, заполним электронные оболочки в описанном выше порядке:
- 2 электрона на 1s-подуровне
- 2 электрона на 2s-подуровне
- 6 электронов на 2p-подуровне
- 2 электрона на 3s-подуровне
- 6 электронов на 3p-подуровне
- 2 электрона на 4s-подуровне
- 10 электронов на 3d-подуровне
- 6 электронов на 4p-подуровне
- 2 электрона на 5s-подуровне
- 10 электронов на 4d-подуровне
- 1 электрон на 5p-подуровне
Степень окисления индия
Атомы индия в соединениях имеют степени окисления 3, 2, 1.
Степень окисления — это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается, то степень окисления положительная.
Ионы индия
Валентность In
Атомы индия в соединениях проявляют валентность III, II, I.
Валентность индия характеризует способность атома In к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа In
Квантовые числа определяются последним электроном в конфигурации, для атома In эти числа имеют значение N = 5, L = 1, Ml = -1, Ms = ½
Видео заполнения электронной конфигурации (gif): 

Источник: https://k-tree.ru/tools/chemistry/periodic.php?element=In
Индий
- Главная
- Справочник
- Химия
- Химические элементы
- Индий
(Indium) In – химический элемент 13-й (IIIa) группы периодической системы, атомный номер 49, атомная масса 114,82.
Строение внешней электронной оболочки 5s25p1. Известно 37 изотопов индия с 98In по 134In. Среди них лишь один стабильный 113In. В природе два изотопа: 113In (4,29%) и 115 In (95,71%) с периодом полураспада 4,41·1014 лет.
Наиболее устойчивая степень окисления в соединениях: +3.
Открытие индия произошло в эпоху бурного развития спектрального анализа – принципиально нового (в те времена) метода исследования, открытого Кирхгоффом и Бунзеном. Французский философ О.Конт писал, что у человечества нет никакой надежды узнать, из чего состоят Солнце и звезды.
Прошло несколько лет, и в 1860 спектроскоп Кирхгоффа опроверг это пессимистичное предсказание. Последующие пятьдесят лет были временем наиболее крупных успехов нового метода.
После того как было установлено, что у каждого химического элемента есть свой спектр, являющийся столь же характерным для него свойством, как дактилоскопический отпечаток – признаком человека, началась «погоня» за спектрами.
Помимо выдающихся исследований Кирхгоффа (едва не приведших его к полной слепоте) элементного состава Солнца, не менее триумфальными были наблюдения спектров земных объектов: в 1861 были открыты цезий, рубидий и таллий.
В 1863 профессор Фрейбергской минералогической школы (Германия) Фердинанд Рейх (1799–1882) и его ассистент Теодор Рихтер (1824–1898) спектроскопически исследовали образцы цинковой обманки (минерала сфалерита, ZnS), чтобы обнаружить в них таллий.
Из образца сфалерита действием соляной кислоты Рейх и Рихтер выделили хлорид цинка и поместили его в спектрограф с надеждой зарегистрировать появление ярко-зеленой линии, характерной для таллия. Профессор Ф.Рейх страдал дальтонизмом и не мог различать цвета спектральных линий, поэтому все наблюдения регистрировал его ассистент Рихтер.
Обнаружить присутствие таллия в образцах сфалерита не удалось, но каково же было удивление Рейха, когда Рихтер сообщил ему о появлении в спектре ярко-синей линии (4511Å). Было установлено, что линия не принадлежала ни одному из известных до этого элементов и отличалась даже от ярко-синей линии спектра цезия.
В силу сходства цвета характеристической полосы в эмиссионном спектре с цветом красителя индиго (латинское «indicum» – индийская краска) открытый элемент был назван индием.
Так как новый элемент был обнаружен в сфалерите, первооткрыватели сочли его аналогом цинка и приписали ему неверную валентность, равную двум. Они определили и атомный вес эквивалента индия, который оказался 37,8.
Исходя из валентности 2, был неверно установлен атомный вес элемента (37,8 × 2 = 75,6). Только в 1870 Д.И.
Менделеев на основании периодического закона установил, что индий имеет валентность, равную трем, и является, таким образом, аналогом алюминия, а не цинка.
Таким образом, в 1871 индий стал 49-ым элементом периодической системы.
Химические элементыТеория Химия 8 класс Химический элемент
Не можешь написать работу сам?
Доверь её нашим специалистам
от 100 р.стоимость заказа 
Если материал понравился Вам и оказался для Вас полезным, поделитесь им со своими друзьями!
- Rh
- Pd
- Ag
- Cd
- Sn
- Sb
- Te
- I
- Конвертер текста в юникодКонвертер для перевода любого текста (не только кириллицы) в Юникод.
- Сколько в ампере ватт, как перевести амперы в ватты и киловаттыМощность – это скорость расходования энергии, выраженная в отношении энергии ко времени: 1 Вт = 1 Дж/1 с. Один ватт равен отношению одного джоуля (единице измерения работы) к одной секунде.
- Ведро́ — сосуд для хранения жидких и сыпучих материалов и транспортировки их на небольшие расстояния.
- Основные тригонометрические тождестваТригонометрические тождества — это равенства, которые устанавливают связь между синусом, косинусом, тангенсом и котангенсом одного угла, которая позволяет находить любую из данных функций при условии, что будет известна какая-либо другая.
- Согласно нормам Всемирной Организацией Здравоохранения (ВОЗ)
- Лошадиная сила — единица мощности. Она примерно равна значению в 75 кгс/м/с., что соответствует усилию, которое необходимо затратить для подъёма груза в 75 кг. на высоту одно метра за одну секунду.
- 1 Ампер это сила тока, при которой через проводник проходит заряд 1 Кл за 1 сек.
Источник: https://calcsbox.com/post/indium.html
ПОИСК
Фосфор, мышьяк или сурьма (имеющие электронное строение внешнего энергетического уровня s pЗ и проявляющие валентность 5), будучи введенными в кристаллические решетки германия или олова (электронное строение внешнего уровня 5 р валентность 4) ведут себя как донорные примеси, т. е. отдают электроны и создают проводимость п-типа.
Если же в германий или кремний ввести бор, алюминий, галлий или индий (электронное строение внешнего уровня 5 р, валентность 3), то атомы примеси захватывают четвертый электрон и полупроводник обнаруживает проводимость р-типа. [c.186] Элементы бор, алюминий, галлий, индий и таллий.
Строение их атомов и внешняя электронная оболочка. Отличие бора от других элементов группы. [c.219]
В Периодической системе элементов Д. И. Менделеева кадмий находится в побочной подгруппе П группы (5-й период) между цинком и ртутью его соседи по периоду — серебро и индий.
Строение электронных оболочек этих элементов приведено в табл. 1 [383, стр. 321]. [c.8]
Многочисленные известные людям металлы химики делят на четыре типа в соответствии с электронным строением металлы (щелочные, щелочноземельные, магний и бериллий), р-металлы (алюминий, галлий, индий, таллий, олово, свинец, сурьма, висмут, полоний), ё- и / металлы (которые иногда объединяют термином переходные металлы ). А какие металлы относятся к черным, цветным и малым [c.210]
Размещению известных Менделееву европия, гадолиния, тербия, гольмия, эрбия, тулия в девятом ряду препятствовало полное несходство их с серебром, кадмием, индием, оловом, сурьмой, теллуром и йодом, под которыми были оставлены места (см. табл. 2).
Не зная электронного строения элементов, нельзя было определить, что лантаноиды не являются аналогами элементов главных подгрупп и d-переходных металлов, а образуют самостоятельные третьи подгруппы /-переходных металлов.
Открытие лютеция и гафния привело к перемещению иттербия во Пс подгруппу, а церия из подгруппы титана в IV подгруппу. Совершенно так же открытие советским ученым Н. И. Флеровым с сотрудниками в 1964 г.
элемента № 104, являющегося аналогом гафния, исключает возможность размещения тория, протактиния и урана в подгруппах d-переходных металлов под гафнием, танталом и вольфрамом, поскольку нельзя в клетку, где поме- [c.24]
Алюминий — основной представитель металлов главной подгруппы III группы периодической системы химических элементов Д. И. Менделеева. Атомный номер 13, относительная атомная масса 26,98154. У алюминия единственный устойчивый изотоп А1. Свойства аналогов алюминия — галлия, индия и таллия — во многом напоминают свойства алюминия.
Этому причина — одинаковое строение внешнего электронного слоя элементов — s p, вследствие которого все они проявляют степень окисления +3. Другие степени окисления нехарактерны, за исключением соединений одновалентного таллия, по свойствам близким к соединениям элементов I группы.
В связи с этим будут рассмотрены свойства только одного элемента — алюминия и его соединений. [c.150]
Радиусы атомов рутения (1,30), родия (1,34) и палладия (1,37) больше, чем металлов подгруппы железа, что создает геометрические предпосылки для образования более сложных силицидов. Строение электронных оболочек этих металлов характеризуется заканчивающимся заполнением Л 4с -слоя и началом заполнения (кроме палладия) ОдЗ-слоя.
Следующие за ними пять элементов (серебро, кадмий, индий, олово, сурьма) не образуют силицидов, а теллур и йод дают лишь малостойкие соединения с кремнием. Можно предполагать, что теплоты образования и температуры плавления силицидов рассматриваемых металлов должны понижаться от рутения к палладию.
Отсутствие соответствующих термодинамических данных о силицидах металлов группы палладия и диаграмм состояния систем Ки—51 и КЬ—51 лишают возможности более подробно выявить имеющиеся здесь закономерности. Судя по диаграмме состояния системы Рс1—51, температуры плавления силицидов рутения и родия должны быть относительно невысокими (едва ли выше 1400—1500°).
Все изученные силициды рутения, родия и палладия образуются с уменьшением объема (см. табл. 2). [c.205]
Кроме уже отмеченных выше исключений из общего правила увеличения ионизационного потенциала в рядах периодической системы, существуют также и другие отклонения. Так, весьма заметные и довольно неожиданные отклонения наблюдаются у кислорода и серы. Другие отклонения, причины которых достаточно хорошо объясняются электронным строением элементов, наблюдаются у галлия, индия и таллия. [c.106]
К р-элементам 1ИА-подгруппы периодической системы относятся элементы бор (В), алюминий (А1), галлий (Оа), индий (1п), таллий (Т1). Строение внешних электронных оболочек их атомов (см. 4.4) ns p (в невозбужденном состоянии) и п р р (в возбужденном состоянии). Бор (первый р-элемент), галлий, индий, таллий объединяются в подгруппу галлня. [c.270]
Введение в ионообменную хроматографическую систему комплексообразующих реагентов кардинально расширило возможности метода.
В образовании комплексных соединений проявляются тонкие особенности электронного строения атомов элементов, более полно выявляется индивидуальность их свойств, поэтому резко повысилась степень однократного разделения смесей, во многом определяющая эффективность хроматографического опыта в целом.
Образование многими металлами отрицательно заряженных комплексов не только позволило облегчить перемещение многозарядных катионов по слою катионита, но и широко использовать аниониты.
Не случайно поэтому именно хроматографические системы с комплексообразующими реагентами привлекли особое внимание как специалистов в области комплексных соединений [7], так и аналитиков. В качестве иллюстрации достаточно упомянуть хроматографическое разделение смесей, включающих цинк, кадмий, индий, галлий, титан, цирконий, торий [8—И]. Заслуживают также упоминания систематические исследования хроматографических свойств практически всех метал,лов в растворах фто- [c.231]
Атомы элементов третьей группы являются электронными аналогами, так как все они имеют одинаковое строение внешнего уровня s p (и одинаковое число электронов на нем).
Металлические свойства у них выражены слабее, чем у элементов I и II главной подгрупп, а у бора, характеризующегося малым радиусом и наличием двух квантовых слоев, преобладают неметаллические свойства.
За исключением неметалла бора, все они могут находиться в водных растворах в виде гидратированных положительно трехзарядных ионов. В этой подгруппе, как и в других, с увеличением порядкового номера металлические свойства сверху вниз усиливаются.
Бор является кислотообразующим элементом оксиды и гидроксиды алюминия, галлия и индия обладают амфо-терными свойствами, а оксид таллия имеет основной характер. [c.78]
Подгруппа П1А. Элементы больших периодов подгруппы ТПА являются по своему строению аналогами алю миния. Существует, однако, принципиальное отличие химии галлия, индия и таллия от химии алюминия возможность устойчивого существования соединений этих элементов со степенью окисления -Ы, которая не характерна для алюминия.
Устойчивость этого состояния возрастает в ряду Оа—1п—Т1, а для таллия она более стабильна, чем степень окисления +3. Современное объяснение такой особенности основано на концепции инертной пары -электронов и уменьшении прочности связей нижних членов групп.
Для рассмотрения надо привлечь особенность электронного состояния II группы, где появляющаяся -электронная пара имеет довольно устойчивый характер и с трудом поддается отщеплению. Так, ртуть, несмотря на то, что это жидкий металл, окисляется с трудом из-за высокого потенциала ионизации (10, 43 эВ) б5 -орбитали.
У нее же впервые проявляется тенденция к существованию стабильной степени окисления -Ы и иона У алюминия велика разница между потенциала- [c.316]
Элементы бор В, алюминий А1, галлий Са, индий 1п и таллий Т1 составляют ША-группу Периодической системы Д.И. Менделеева. Строение валентного электронного уровня у атомов этих элементов одинаково — пз пр , поэтому для этих элементов характерна степень окисления +111.
Электроотрицательность данных элементов невысока. По химическим свойствам бор — неметалл алюминий, галлий и индий — амфотерные элементы, причем при переходе от А1 к 1п основные свойства усиливаются, а таллий проявляет металлические свойства (для него более устойчиво состояние ТГ1, чем ТГ 1).
[c.182]
В устойчивых соединениях элементы этой группы проявляют степень окисления +3, находясь в состоянии /гsV -возбуждения. Исключение составляет таллий, для которого характерна также степень окисления 1. В природе они встречаются только в виде соединений, причем галлий, индий, таллий относятся к редким элементам.
В свободном виде их получают электролизом из расплавов соединений. Металлы этой группы легкоплавкие, имеют серебристо-белый цвет. Галлий, индий и таллий очень мягкие, режутся ножом.
Наблюдаемое нарушение закономерного изменения некоторых свойств при переходе от А1 к Оа возникает вследствие различия в строении предпоследнего электронного уровня атомов алюминия (8), галлия (18). [c.229]
Свойства атомов. Энергии ионизации изменяются в 1ПА-подгруппе немонотонно (табл. 17.2). Это объясняется строением электронных оболочек атомов. Хотя электронные формулы валентных подуровней одинаковы для всех элементов подгруппы пв пр , строение электронных остовов их атомов сильно различается.
В отличие от металлов 1А- и ПА-подгрупп, у которых атомные остовы описываются электронными формулами, характерными для атомов благородных газов, в ША-подгруппе такие остовы имеют только бор и алюминий. У галлия и индия атомные остовы завершаются заполненными ( -подуровнями, а у таллия — ( -и /-подуровнями.
[c.310]
Подгруппа галлия. Металлы галлий, индий и таллий часто объединяют в подгруппу галлия, так как их атомы характеризуются одинаковым строением последнего и предпоследнего квантовых слоев три электрона в наружном слое (s p ) и 18 электронов в предпоследнем [c.239]
Можно было бы ожидать, что эти элементы будут образовывать с тремя лигандами плоские молекулы, подобно галогенидам бора.
Однако для них характерна ярко выраженная тенденция притягивать на свои незаполненные валентные оболочки дополнительные электронные пары, и поэтому их соединения существуют главным образом в виде тетраэдрических или октаэдрических комплексов.
Трифенилгаллий и трифенилиндий представляют собой плоские тригональные молекулы, по-видимому образующие друг с другом слабые межмолекулярные связи металл— углерод, чтЬ приводит к тригонально-бипирамидальной координации вокруг каждого атома металла.
У молекулы А1Ы(51(СНз)з)2]з, как и предполагалось, найдена плоская тригональная конфигурация. Согласно спектральным данным, в парах хлоридов, бромидов и йодидов алюминия, галлия и индия при высоких температурах присутствуют плоские молекулы типа АХ3.
Доказано также, что трийо-дид галлия существует в виде мономера и имеет плоскую треугольную конфигурацию. Интересное предположение состоит в том, что трифториды таллия и индия (возможно, и хлориды) могут иметь пирамидальное, а не плоское строение по той же причине, которая выдвигалась для объяснения изогнутой (угловой) формы молекулы ВаРз в газовой фазе. [c.155]
Галлий Оа (1,7-10 % по массе), индий 1п (10 %) и таллий Т1 (3-10 ч- 3-10 %). Строение электронных оболочек атомов этих элементов отличается от строения оболочек В и А1. Второй снаружи энергетический уровень их атомов содержит 18 электронов. В свободном состоянии это металлы серебристо-белого цвета.
Максимальная валентность их плюс 3. Образуют они и соединения низшей валентности. Прочность соединений высшей валентности падает в ряду Са 1п Т1, а прочность одновалентных соединений в том же ряду возрастает. В связи с этим галлий и индий нри взаимодействии с кислотами образуют ионы 1п +, а таллий — ионы Т1+ [c.
247]
Некоторые свойства этих элементов даны в табл. 2. Из таблицы видно, что особенно отличаются свойства высокотемпературного бора от свойств легкоплавких, типичных металлов — алюминия, галлия, индия и таллия.
У бора величина первого ионизационного потенциала, характеризующая энергию связи внешних / -электронов, наибольшая (строение внешних орбит у элементов III Б группы s p). У остальных элементов-аналогов величина первого ионизационного потенциала значительно меньше, чем у бора, и почти одинакова.
Бор обладает наибольшей величиной электроотрицательности и малыми размерами кристаллохимических радиусов. [c.8]
Исследования элементов при высоких давлениях, кардинальным образом изменяющих строение и степень перекрытия внешних электронных оболочек, привели к обнаружению неизвестных ранее модификаций рубидия, цезия, бария, галлия, индия, таллия, кремния, германия, олова, свинца, сурьмы, висмута, титана, циркония и других элементов. Круг полиморфных металлов расширился настолько, что можно полагать, что в природе вообще не существует элементов, сохраняющих одну и ту же структуру в достаточно широком диапазоне давлений и температур. [c.196]
Гал.лий, индий и таллий по своему атомному строению соответствуют бору и алюминию, поскольку у них у всех одинаковая конфигурация внешней электронной оболочки (два s-электрона и один р-электрон).
От бора и алюминия они, однако, отличаются, поскольку у них вслед за уровнем s p следует не уровень (оболочка инертного газа), а уровень (см. табл. II в приложении).
Эта особенность строения влияет на свойства и поведение как свободных элементов, так и их соединений. [c.363]
I, 2, 4 и 1, 2, 3. Спектры фракций № 3, 4 похожи друг на друга. Основные максимумы поглощения этих фракций и расшифровка индивидуальных углеводородов по электронным спектрам поглощения приведены в табл. 2.
Появление плеча 2756—2770 А во фрак-щии № 6 говорит о присутствии тетраметилбензолов типа 1, 2, 4,5.. Максимум поглощения 2728 А во фракции № 9 свидетельству-.ет о присутствии тетраметилбензолов строения 1, 2, 3, 4.
Так как максимумы поглощеиия индановых углеводородов в ультрафиолетовой области в большинстве случаев совпадают с длинами волн максимумов алкилбензолов, а интенсивность поглощения инданов лишь в 2—3 раза выше интенсивности поглощения бензолов, то в смеси углеводородов инданы могут быть обнаружены лишь в количествах более 10— 20% от общего количества углеводородов. [c.34]
Общая характеристика. Эти элементы редкие, за исключением алюминия, на долю которого приходится 8,8% массы земной коры (третье место — за кислородом и кремнием). Во внешнем электронном уровне их атомов по три электрона а в возбужденном состоянии Проявляют высшую валентность 111 Э2О3, Э(ОН)з, ЭС1з и т. д.
Связи с тремя соседними атомами в соединениях типа ЭХд осуществляются за счет перекрывания трех гибридных облаков поэтому молекулы имеют плоское трехугольное строение, дипольный момент нуль.
Из-за того, что в атомах галлия, индия и таллия предпоследний уровень содержит по 18 электронов, алюминия 8 и бора 2, нарушаются закономерные различия некоторых свойств при переходе от алюминия к галлию температур плавления элементарных веществ, радиусов атомов, энтальпий и свободных энергий образования оксидов, свойств гидроксидов и пр. (табл. 23). Таков же характер изменения различий при переходе от магния к цинку. [c.279]
Эти элементы дают ярко окрашенные соединения, являются энергичными окислителями и восстановителями. Возможно, что с особенностями строения электронных оболочек связана и каталитическая активность соединений этих металлов.
Наоборот, элементы с постоянной валентностью отличаются меньшихм разнообразием химических соединений и редко образуют окрашенные соединения. Из редких металлов лишь немногие относятся к этому типу—литий, рубидий, бериллий, отчасти галлий, индий и таллий.
[c.16]
Хорошо растворимы в магнии и в твердом, и в жидком состояниях металлы с плотно застроенной ( -оболочкой, к которым, например, oтнoJ сятся цинк, кадмий, свинец, олово, висмут, таллий, индий.
Наибольшей взаимной растворимостью отличаются магний и кадмнй, у которых наименьшее различие в атомных диаметрах и строении электронных оболочек.
Перечисленные металлы образуют с магнием ряд соединений, которые в случае металлов IV и V групп подчиняются правилам валентности (например, МдгБп, М гВ и др.). С металлами 11 и III [c.102]
Чрезвычайно ярко проявляются отклонения, обусловленные различием строения внутренних электронных оболочек, в аналитическом поведении элементов подгруппы Illa. Бор, который обладает электронной конфигурацией ls 2s 2j3 имеет преобладаюш ие электроотрицательные свойства и образует кислоты (Н3ВО3 и др.), проявляя себя в качестве типичного аниона.
Алюминий, ион которого АР+, имеет внешнюю конфигурацию 2s 2j9 , образует слабо основную и труднорастворимую гидроокись, выделяющуюся при действии сульфида аммония. На этом основании и по другим признакам алюминий относится к III аналитической группе, возглавляя первую ее подгруппу (см. табл. 19 и 20).
Галлий и индий, ионы которых Ga + и 1п + имеют внешние конфигурации 3d и обычно [c.103]
Источник: https://www.chem21.info/info/1181830/
Индий
-
Химический элемент №49 In (индий)
-
Электронная формула: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p1
-
5IIIA; 5 – номер периода, соответствует числу энергетических уровней (5); III – номер группы, определяет число валентных электронов и высшую валентность; А – главная подгруппа; 49 – порядковый номер, определяет заряд ядра и количество электронов. Эффект провала электрона отсутствует.
-
5s2 5p1 – валентные электроны. Индий принадлежит к p-элементам, т.к. последний валентный электрон находится на p-подуровне.
-
Набор квантовых чисел для валентных электронов:
-
| n | 5 | 5 | 5 |
| l | 0 | 0 | 1 |
| ml | 0 | 0 | -1 |
| ms | +0.5 | -0.5 | +0.5 |
-
Индий представляет собой серебристо-белый металл. Проявляет максимальную степень окисления +3.
5s 5s
Возбужденное состояние.
-
При образовании бинарных соединений In проявляет sp2-гибридизацию, например InF3. У индия (в возбужденном состоянии) 3 неспаренных электрона (1s и 2p) и при образовании соединения, они гибридизуются, и тип гибридизации- sp2.
-
Свойства соединений данного химического элемента.
-
Оксид: In2O3 – амфотерный (т.к. ∆Э.О.=Э.О.O2 — Э.О.In =3.5-1.5=2)
-
Гидроксид: In(OH)3- амфотерный.
- In(OH)3
+ 3HCl = InCl3
+ 3H2O - H3InO3
= HInO2
+ H2O - HInO2
+ NaOH = NaInO2
+ H2O
-
Молекула InF3 плоская и имеет форму плоского треугольника F
In
F F
-
K+[In(OH)4]- — тетрагидроксоиндиат калия; In3+-комплексообразователь, (OH)—лиганд, 4-координационное число.
K[In(OH)4]=
K+ +
[In(OH)4]-
[In(OH)4]- In3+
+ 4(OH)-
In3+ — акцептор, т.к.
имеет свободную АО (5р); т.к. Э.О.
O2
> Э.О. H2,
то O2- донор, т.к.
имеет двухэлектронную орбиталь.
Кн=(СIn3+
* COH-)/C[In(OH)4]-
-
Состояние электролита в растворе.
3.1 Гидролиз NaInO2 идет
по аниону, т.к. эта соль образована
сильным основанием и слабой кислотой
(NaOH и HInO2).
- NaInO2
+ aq → Na+aq
+ (InO2)-aq - (InO2)-
+ H2O
→ HInO2 +
(OH)- - H+
+ (OH)- - NaInO2
+ H2O
→ HInO2 +
NaOH
pH=14+0.5lg(Kводы*С(InO2)-
/ КHInO2)=-0,5lg(10-14*1.9/(6.7*10-14))=13.7
Гидролиз In(NO3)3
идет по катиону т.к. эта соль образована
слабым основанием и сильной кислотой
(In(OH)3
и HNO3).
- In(NO3)3
+ aq → In3+aq
+ 3(NO3)-aq - In3+
+ H2O
→InOH2+
+ H+ - H+
+ (OH)- - In(NO3)3
+ H2O
→ InOH(NO3)2
+ HNO3
pH=-0.5lg(Kводы*СIn3+
/ К
In(OH)3)=-0.5lg(10-14*1.9/(4.5*10-3))=5.7
Реакция гидролиза эндотермическая,
поэтому, в соответствии с принципом
Ле-Шателье о сдвиге равновесия, нагревание
способствует гидролизу.
4. Окислительно-восстановительные
процессы.
4.1 Индий, как металл может проявлять
только восстановительные (Red)
свойства :
In0
– 3e → In3+
φ
In3+/
In0=-0.34В
(ст.усл)
In0
–e → In+
φ
In+/
In0=-0.25В
(ст.усл)
Ионы индия могут быть как окислителями
так и восстановителями. Они проявляют
восстановительные свойства в кислой
среде окислительные – в щелочной.
- pH7: In3+
+ 3e → In0
φ
In3+/
In0=-0.34В - In+
+ e → In0
φ
In+/
In0=-0.25В - In2+
+ e → In+
φ
In2+/
In+=-0.35В - 4.2
1) In0
+ Fe3+Cl3
+ H2O
→ In3+2O3
+ Fe2+ - 1 2In0
– 6e + 3H2O
→ In3+2O3
+ 6H+ - 6 Fe3+
+ e → Fe2+ - 2In0
+ 6 Fe3+
+ 3H2O
→ In2O3
+ 6 Fe2+
+6H+ - 2In0
+ 6 FeCl3
+ 3H2O
→ In2O3
+ 6 FeCl2
+6HCl
E0
= φFe3+/Fe2+
— φIn2O3/In0
= 0.77 – (-1.03) =1.8
Так как E0>0, то
реакция самопроизвольно идет в прямом
направлении, т.е. концентрации исходных
веществ будут уменьшаться, а продуктов
реакции – увеличиваться.
- 2) InCl3
+ Zn0
+KOH → In0
+ [Zn(OH)4]2-
+ … - 2 In3+
+ 3e → In0 - 3 Zn0 –
2e + 4(OH)-
→ [Zn(OH)4]2- - 2In3+
+ 3Zn0
+ 12(OH)-
→ 2In0
+ 3[Zn(OH)4]2- - 2InCl3
+ 3Zn0
+ 12 KOH → 2In0
+ 3K2[Zn(OH)4]
+ 6KCl
E0
= φIn3+/In0
– φZn0/[Zn(OH)4]2-
= -0.34 + 1.2=0.86В
- Реакция идет в прямом направлении.
- 3) In0
+ KMnO4
+ HCl → In3+
+ Mn2+
+ … - 5 In0
– 3e → In3+ - 3 MnO4-
+ 5e + 8H+
→ Mn2+
+ 4H2O - 5In0
+ 3 MnO4-
+24H+
→ 5In3+
+ 3Mn2+
+ 12H2O - 5In0
+ 3KMnO4
+24HCl → 5InCl3
+ 3MnCl2
+ 12H2O
+ 3KCl
E0
= φMnO4-/Mn2+
– φIn3+/In0
= 1.5 + 0.34=1.84В
Реакция идет в прямом направлении.
5.Электрохимические свойства.
5.1 VIn2O3/2VIn
= 1.04 – оксидная пленка плохо защищает
металл от дальнейшего окисления. Tok/Tпл
= 1.3 – металл не теплостойкий. ∆Gin-O2=-832
кДж/моль – металл склонен к самопроизвольному
окислению.
- Взаимодействие с водой (pH=7):
- 2In
+ 6H2O
→ 3H2↑
+ 2In(OH)3 - 2 In0
– 3e → In3+ - 3 2H2O
+ 2e → H2↑
+ 2(OH)-
φH2O/
H2=-0.059pH=-0.41
φ
In3+/
In0=-0.34В
Ep
= φH2O/
H2
– φIn3+/In0
= -0.41+0.34=-0.07В
- Индий водой не окисляется.
- Взаимодействие с кислотами. Взаимодействие
с неокислительными кислотами (HCl): - 2In
+ 6HCl → 3H2↑
+ 2InCl3 - 2 In0
— 3e → In3+ - 3 2H+
+ 2e → H2↑
φH+/H2=-0.059pH=-0.059*0=0
φ
In3+/
In0=-0.34В
Ep
= φH+/H2–
φIn3+/In0
= 0+0.34=0.34В
- Неокислительной (соляной) кислотой
окисляется. - Взаимодействие с окислительными
кислотами (HNO3): - При нагревании:
- In + 6HNO3(конц)
→ In(NO3)3
+ 3H2O
+ 3NO2↑
Ep
= φNO3-/
NO2–
φIn3+/In0
= 0.8+0.34=1.14В
8In + 30HNO3(оч.оч.разб)
→ 8In(NO3)3
+ 9H2O
+ 3NH4NO3
Ep
= φNO3-/
NH4+–
φIn3+/In0
= 0.87+0.34=1.21В
На холоду:
8In + 3HNO3(оч.оч.разб)
+ 3H2O
→ 4In2O3
+ 3NH4NO3
Ep
= φNO3-/
NH4+–
φIn3+/In0
= 0.87+0.34=1.21В
- Взаимодействие с щелочами:
- 2In + 2NaOH + 2H2O
→ 3H2↑
+ 2NaInO2 - 4In + 3O2(г)
+ 4NaOH → 4NaInO2
+ 2H2O
5.2 Электролит
In(NO3)3,
H2O;
pH=4.6
- Анод (+) из C:
- Анодная реакция в общем виде: RedA
– Ze → OxA - Конкурирующие частицы: (NO3)-,
H2O
φO2/H2O=1.23
– 0.059pH + ηO2/In=2.1
(ηO2/In=1.12)
- Катод (-) из С:
- Катодная реакция в общем виде: OxК
+ Ze → RedК - Конкурирующие частицы: In3+,
H2O
φH2O/H2=-0.059pH-
ηH2/In=0.43
(ηH2/In=-0.7)
– самый положительный на катоде
- φ
In3+/
In0=-0.34В - A: 2H2O
– 4e = O2↑
+ 4H+ - K:H2O
+ 2e = H2↑
+ 2(OH)- - Продукты электролиза на аноде HNO3
в диссоциированном виде и газ O2,
а на катоде газ - H2
и In(OH)3(тв). - 5.3
- K Ag||AgClтв|Cl-||In3+|In A
- φAgClтв/Ag=0.22-
предположительно катод - φK
=
φAgClтв/Ag
, тогда
φA=
φIn3+/In0 ЭДС=
φK
– φA - Снимаются показания потенциометра
(ЭДС) и находится φA
по формуле: φA=
φK–
ЭДС.
5.4 φSn2+/Sn=-0.14;
φ
In3+/
In0=-0.34
Значит In – анод,
а Sn — катод
(т.к.
φ In3+/
In0< φSn2+/Sn)
1) Без аэрации, pH=7
- A: In | H2O
| Sn :K - (OH)-
- A:
2 In0
— 3e → In3+ - K: 3 2H2O
+ 2e → H2↑
+ 2(OH)- - 2In0
+ 6H2O
= 3H2↑
+ 2In3+
+ 6(OH)- - 2In(OH)3
φK
= -0.059pH=-0.41В
- φA=
φ In(OH)3/
In0=-1.07В - Eкор=
φK
– φA=0.66В - Процесс коррозии идет интенсивно.
- 2) С аэрацией, pH=7
- e
- A: In | O2,
H2O |
Sn :K - (OH)-
- A:
4 In0
— 3e → In3+ - K: 3 O2
+ 4e + 2H2O
→ 4(OH)- - 2In0
+ 3O2
+ 6H2O
= 4In3+
+ 12(OH)- - 4In(OH)3
φK
= 1.23-0.059pH=0.82В
- φA=
φ In3+/
In0=-0.34
В - Eкор=
φK
– φA=1.16
В - Процесс коррозии протекает очень
активно.
In0
| In3+||
(MnO4)-
| (MnO4)2-
φ
In3+/
In0=-0.34;
φ(MnO4)-/
(MnO4)2-=.056
Значит In – анод,
а (MnO4)2— катод
(т.к.
φ In3+/
In0< φ(MnO4)-/ (MnO4)2-)
- A: In0
— 3e → In3+ - K: (MnO4)-
+ e → (MnO4)2- - In0
+ 3(MnO4)-
= In3+
+ 3(MnO4)2-
5.6 E=
φK
– φA=0.56+0.34=0.9В
- Дан раствор соли In(SCN)3,
Cг/л=7,5 г/л, ρ=1,1
г/см3,М=115+(32+12+14)*3=289г/моль - А) С%= Cг/л/10
ρ=7,5/11=0,68 - Б)СМ= Cг/л/М=7,5/289=2,6*10-2М
- В)СН= Cг/л/1000=7,5*10-3
г-экв/л - Г)Т= Cг/л/1000=7,5*10-3
г/см3 - Министерство образования и науки
Российской Федерации
«МАТИ»-РГТУ им. К.Э.Циолковского
- Кафедра «Общая
химия, физика и химия композиционных
материалов» - Курсовая работа
по неорганической и аналитической химии - «Свойства металла
и его соединений».
Студент: Васильев А.А.
Факультет № 1
Группа: 1ОМД-1ДС-066
Преподаватель: Клеменьтьева В.С.
Отметка о сдаче
Источник: https://studfile.net/preview/862954/




